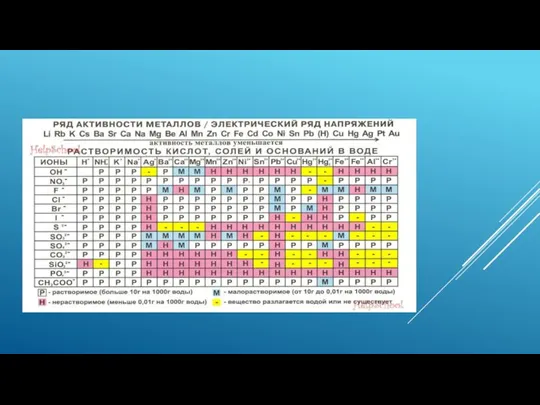
Слайд 2РЕАКЦИИ ИОННОГО ОБМЕНА
Уравнения ионных рекций моржно записать в полном и сокращённом виде.

Слайд 3 СОКРАЩЁННОЕ УРАНЕНИЕ ПОКАЗЫВАЕТ КАКИЕ ИМЕННО ИОНЫ УЧАСТВУЮТ В РЕАКЦИИ.

Слайд 6Если в составе соли имеются ионы, которые могут связываться с ионами Н+

или ионами ОН-, то соли будут реагировать с водой.
Процесс взаимодействия солей с водой называется ГИДРОЛИЗОМ («гидро»- вода, «лизис»- разложение.
Гидролиз –это взаимодействие ионов соли с водой с обра
зованием малодиссоциирующих электролитов.
Слайд 7С водой реагируют соли, образованные или слабым основанием и сильной кислотой, или

сильным основанием и слабой кислотой.
Соли образованные сильным основанием и сильной кислотой не реагируют с водой.
Слайд 8ГИДРОЛИЗ СОЛЕЙ.
Гидролиз не возможен
Соль, образованная сильным основанием и сильной кислотой (KBr, NaCl, NaNO3), гидролизу

подвергаться не будет, так как в этом случае слабый электролит не образуется.
рН таких растворов = 7. Реакция среды остается нейтральной.
Слайд 93). Гидролиз по аниону (в реакцию с водой вступает только анион)
Соль, образованная сильным

основанием и слабой кислотой (КClO, K2SiO3, Na2CO3, CH3COONa) подвергается гидролизу по аниону, в результате чего образуется слабый электролит, гидроксид-ион ОН- и другие ионы.
K2SiO3 + НОH <=>KHSiO3 + KОН
2K+ +SiO32- + Н+ + ОH-<=> НSiO3- + 2K+ + ОН-
рН таких растворов > 7 (раствор приобретает щелочную реакцию).
Слайд 10Совместный гидролиз (в реакцию с водой вступает и катион и анион)
Соль, образованная

слабым основанием и слабой кислотой (СН3СООNН4, (NН4)2СО3, Al2S3), гидролизуется и по катиону, и по аниону. В результате образуются малодиссоциирующие основание и кислота. рН растворов таких солей зависит от относительной силы кислоты и основания. Мерой силы кислоты и основания является константа диссоциации соответствующего реактива.
Реакция среды этих растворов может быть нейтральной, слабокислой или слабощелочной:
Al2S3 + 6H2O =>2Al(OH)3↓+ 3H2S↑
Гидролиз - процесс обратимый.
Гидролиз протекает необратимо, если в результате реакции образуется нерастворимое основание и (или) летучая кислота
Слайд 15Рассмотрим на примере гидролиза сульфита натрия (Na2SO3) – двухосновной соли, образованной слабой

кислотой – сернистой (H2SO3) и сильным основанием – гидроксидом натрия (NaOH):
Na2SO3 ↔ SO32- + 2Na+ (диссоциация соли);
SO32- + 2Na++ H2O ↔ HSO3—+ OH— + 2Na+ (полное ионное уравнение);
SO32- + H2O ↔ HSO3—+ OH— (сокращенное ионное уравнение);
Na2SO3 + H2O ↔ NaHSO3+ NaOH (молекулярное уравнение
Слайд 16Теоретически возможна вторая ступень гидролиза:
NaHSO3↔Na+ + HSO3—(диссоциация соли);
Na+ + HSO3— + H2O

↔H2SO3 + OH— + Na+ (полное ионное уравнение);
HSO3— + H2O ↔ H2SO3 + OH—(сокращенное ионное уравнение);
NaHSO3+ H2O↔H2SO3 +NaOH (молекулярное уравнение).
Присутствие гидроксид-ионов свидетельствует о том, что реакция среды водного раствора сульфита натрия будет щелочной, а окраска индикатора лакмуса – синей.















 Типы кристаллических решеток
Типы кристаллических решеток Судын оксидтермен реакциясы
Судын оксидтермен реакциясы Ионная химическая связь
Ионная химическая связь Классы неорганических соединений
Классы неорганических соединений Истина - дочь времени, а не авторитета
Истина - дочь времени, а не авторитета Презентация на тему Виды кристаллических решеток
Презентация на тему Виды кристаллических решеток 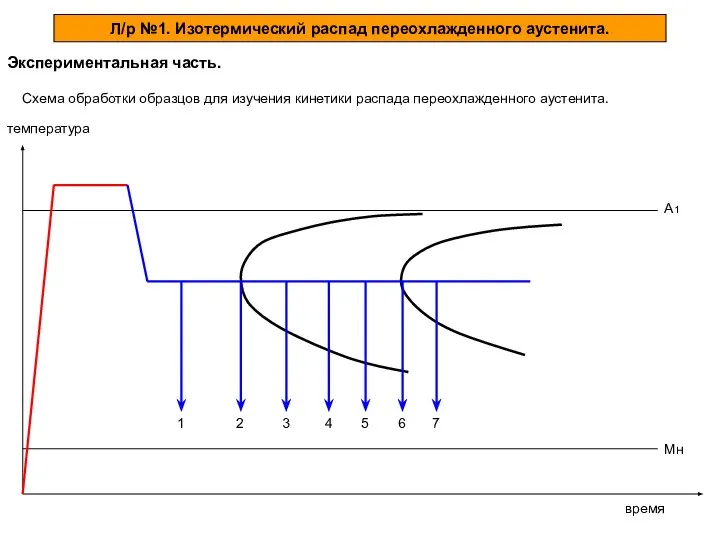 Изотермический распад переохлажденного аустенита. Экспериментальная часть
Изотермический распад переохлажденного аустенита. Экспериментальная часть Содержание варианта ЕГЭ
Содержание варианта ЕГЭ 11_.21
11_.21 Использование комплексно-ориентированных заданий на уроках
Использование комплексно-ориентированных заданий на уроках Окислительно-восстановительные реакции (ОВР)
Окислительно-восстановительные реакции (ОВР) Реакции окисления-восстановления в химическом анализе. (Лекция 7.2)
Реакции окисления-восстановления в химическом анализе. (Лекция 7.2) Алканы
Алканы Химия и автомобиль
Химия и автомобиль Общая характеристика элементов подгруппы углерода. Углерод – его строение и свойства
Общая характеристика элементов подгруппы углерода. Углерод – его строение и свойства Природный каучук
Природный каучук Классификация оксидов
Классификация оксидов Химические реакции
Химические реакции Образование и получение веществ. 6 класс
Образование и получение веществ. 6 класс Металлы
Металлы Закон сохранения массы веществ. Уравнения химических реакций.
Закон сохранения массы веществ. Уравнения химических реакций. Сравнительная характеристика стиральных порошков
Сравнительная характеристика стиральных порошков Валентность. Определение валентности по формулам
Валентность. Определение валентности по формулам Кроссворд. Плотность
Кроссворд. Плотность Алкены
Алкены Коррозия металлов
Коррозия металлов Вещества с атомной кристаллической решеткой
Вещества с атомной кристаллической решеткой Cкорость химических реакций
Cкорость химических реакций