Содержание
- 2. это процессы, в результате которых из одних веществ образуются другие, отличающиеся от них по составу и
- 3. По числу и составу реагирующих и образующихся веществ По тепловому эффекту По фазовому составу Классификация химических
- 4. I. По числу и составу реагирующих и образующихся веществ: Реакции, идущие без изменения состава веществ. В
- 5. I. По числу и составу реагирующих и образующихся веществ: Реакции, идущие с изменением состава вещества 1.
- 6. I. По числу и составу реагирующих и образующихся веществ: Реакции, идущие с изменением состава вещества 2.
- 7. Получение кислорода из перманганата калия: Классификация химических реакций
- 8. I. По числу и составу реагирующих и образующихся веществ: Реакции, идущие с изменением состава вещества 3.
- 9. Взаимодействие натрия с водой: Классификация химических реакций
- 10. I. По числу и составу реагирующих и образующихся веществ: Реакции, идущие с изменением состава вещества 4.
- 11. VI. По тепловому эффекту: 1. Экзотермические реакции протекают с выделением энергии: Классификация химических реакций 4P +
- 12. Горение фосфора в кислороде: Классификация химических реакций
- 13. VI. По тепловому эффекту: 2. Эндотермические реакции протекают с поглощением энергии: Классификация химических реакций N2 +
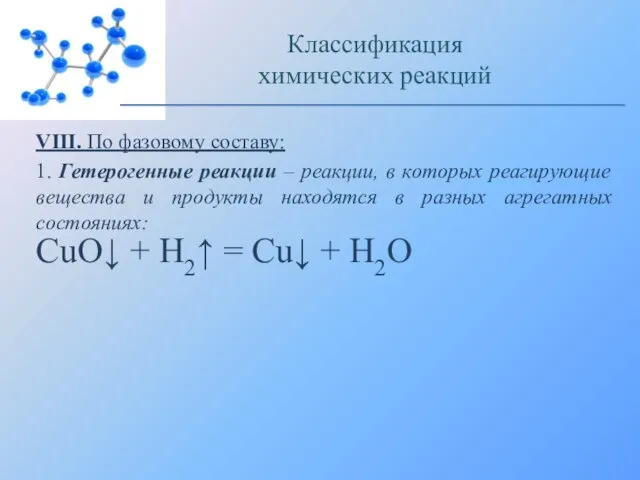
- 14. VIII. По фазовому составу: 1. Гетерогенные реакции – реакции, в которых реагирующие вещества и продукты находятся
- 15. Восстановление оксида меди (II) водородом: Классификация химических реакций
- 17. Скачать презентацию













 Викторина. Химический элементарий. Д.И. Менделеев – гордость русской науки
Викторина. Химический элементарий. Д.И. Менделеев – гордость русской науки Охрана родников Ногликского района и анализ воды из этих родников
Охрана родников Ногликского района и анализ воды из этих родников каталитические системы на основе металлоценов и метилалюмоксана в реакциях непредельных соединений с изобутиланами
каталитические системы на основе металлоценов и метилалюмоксана в реакциях непредельных соединений с изобутиланами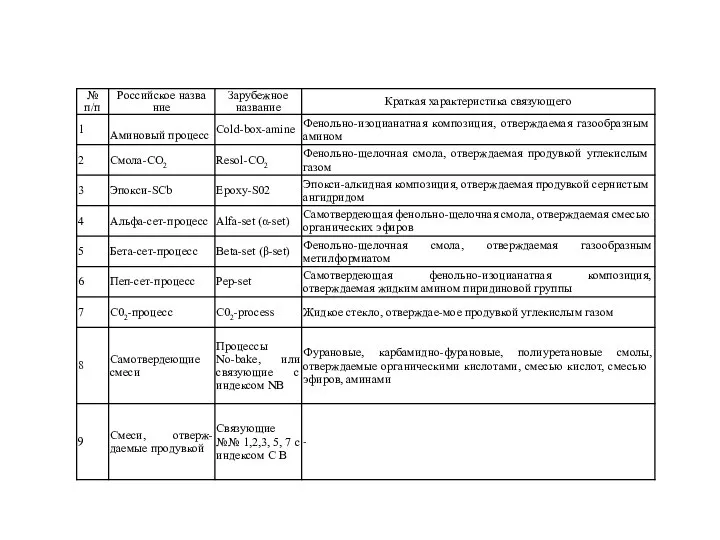 Фенольно-изоцианатная композиция
Фенольно-изоцианатная композиция Растворы. Определение
Растворы. Определение Как решить задания тестов ЕГЭ по химии, если знания на базовом уровне. Метод исключения
Как решить задания тестов ЕГЭ по химии, если знания на базовом уровне. Метод исключения Положение кислорода и серы в Периодической системе химических элементов, строение атомов. Строение простых веществ. Аллотропия
Положение кислорода и серы в Периодической системе химических элементов, строение атомов. Строение простых веществ. Аллотропия Электролитическая диссоциация веществ Реакции ионного обмена и условия их протекания
Электролитическая диссоциация веществ Реакции ионного обмена и условия их протекания Техника безопасности при использовании различных видов топлива. Практическая работа № 3
Техника безопасности при использовании различных видов топлива. Практическая работа № 3 Алкины. Строение, номенклатура, изометрия, физические свойства
Алкины. Строение, номенклатура, изометрия, физические свойства Практикум по химии и технологии нефти и газа
Практикум по химии и технологии нефти и газа Атомы химических элементов
Атомы химических элементов Общая характеристика элементов подгруппы углерода. Углерод как простое вещество
Общая характеристика элементов подгруппы углерода. Углерод как простое вещество Синтез-газ
Синтез-газ Галогеналканы и реакции отщепления
Галогеналканы и реакции отщепления Бинарные соединения – оксиды и летучие водородные соединения. 8 класс
Бинарные соединения – оксиды и летучие водородные соединения. 8 класс Структура металлов, сплавов, интерметаллидов и квазикристаллов
Структура металлов, сплавов, интерметаллидов и квазикристаллов Формула аспирина. Решение задач
Формула аспирина. Решение задач Окислительно-восстановительные реакции
Окислительно-восстановительные реакции Презентация на тему Комплексные соединения
Презентация на тему Комплексные соединения  Терпеноиды. Эфирные масла
Терпеноиды. Эфирные масла Практическая работа №1. Определение содержания нитратов в овощах и фруктах
Практическая работа №1. Определение содержания нитратов в овощах и фруктах Альдегиды и кетоны
Альдегиды и кетоны Квантовая химия
Квантовая химия Химия и сельское хозяйство
Химия и сельское хозяйство Алкины
Алкины Химия в нашей жизни
Химия в нашей жизни Альдегиды, свойства, получение, применение
Альдегиды, свойства, получение, применение