Слайд 2Изучаем темы
Химические свойства щелочей:
взаимодействие с кислотными оксидами,
кислотами,

растворами солей.
Получение щелочей на примере реакции гашения извести.
Составление уравнений соответствующих реакций.
Слайд 3Щелочи
Растворимые в воде сильные основания (основания щелочных и щелочноземельных металлов) называют

щелочами, например: NaOH, Ba(OH)2, KOH, LiOH, Ca(OH)2.
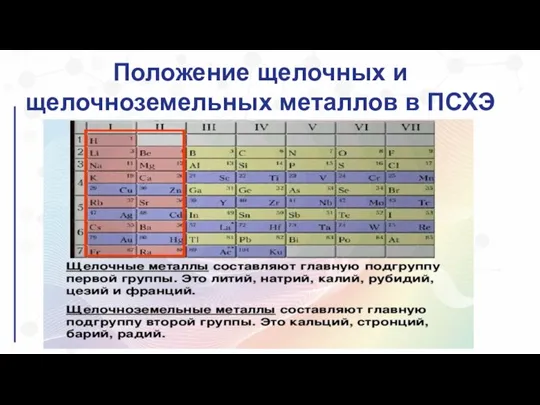
Слайд 4Положение щелочных и щелочноземельных металлов в ПСХЭ
Слайд 10Хранение щелочных и щелочноземельных металлов

Слайд 11Ca(OH)2
Не следует путать силу основания и его растворимость.
Например, гидроксид кальция, Ca(OH)2

– сильное основание, хотя его растворимость в воде невелика. В данном случае сильным основанием (щелочью) называют ту часть гидроксида кальция, которая растворена в воде (известковая вода).
Слайд 13Физические свойства щелочей
Щелочи – это твердые кристаллические вещества, растворимые в воде.

Их растворы мылки на ощупь. Гидроксиды щелочных металлов (NaOH, KOH) гигроскопичны (поглощают из воздуха водяные пары и расплываются).
Слайд 14Физические свойства щелочей
Щелочи вызывают сильные химические ожоги при попадании на кожу

или в глаза, поэтому при работе с ними требуется жесткое соблюдение правил безопасности: работать с концентрированными растворами щелочей следует аккуратно, обязательно использовать защитные очки.
Слайд 16Химические свойства щелочей
1. Растворы щелочей действуют на индикаторы, изменяя их окраску:
лакмус становится

синим, метилоранж – жёлтым, фенолфталеин - малиновым
Слайд 17Химические свойства щелочей
2. Взаимодействие с кислотами по реакции обмена
(реакция нейтрализации):
Щелочь +

Кислота = Соль + Вода
Слайд 18Химические свойства щелочей
Примеры:
3NaOH + H3PO4 = Na3PO4 + 3H2O
Cа(OH)2 + 2HCl =

CаCl2 + 2H2O
Слайд 19Химические свойства щелочей
3. Взаимодействуют с кислотными оксидами:
Щелочь + Кислотный оксид = Соль

+ Вода
Слайд 20Химические свойства щелочей
Примеры:
2KOH + CO2 → K2CO3 + H2O
Ba(OH)2 + SO3 →

BaSO4↓ + H2O
Слайд 21Химические свойства щелочей
Примеры:
2KOH + N2O5 = 2KNO3 + H2O
6NaOH + P2O5 =

2Na3PO4+ 3Н2О
Слайд 22Химические свойства щелочей
Примеры:
2KOH + SiO2 = K2SiO3 + H2O
Ca(OH)2 + Cl2O7 =

Ca(ClO4)2 + H2O
Слайд 23Химические свойства щелочей
Ca(OH)2 + CO2 = CaCO3↓ + H2O
Реакция взаимодействия гидроксида кальция

с углекислым газом (CO2) является качественной реакцией на углекислый газ.
Качественная реакция – реакция, которая позволяет обнаружить тот или иной ион, вещество или функциональную группу.
Слайд 24Химические свойства щелочей
4. Взаимодействуют с cолями, если в результате образуется малорастворимое или

газообразное соединение:
Щелочь + Соль = Соль + Основание
Слайд 25Химические свойства щелочей
4. Взаимодействуют с cолями, если в результате образуется нерастворимая соль:
Примеры:
Ba(OH)2

+ K2SO4 → 2KOH + BaSO4↓
Ba(OH)2 + Li2SO4 → 2LiOH + BaSO4↓
Слайд 26Химические свойства щелочей
4. Взаимодействуют с cолями, если в результате образуется нерастворимая соль:
Примеры:

Ca(OH)2 + K2CO3 → 2KOH + CaCO3↓
Слайд 27Химические свойства щелочей
4. Взаимодействуют с cолями, если в результате образуется нерастворимое основание:
Примеры:

2NaOH + CuSO4 → Cu(OH)2↓ + Na2SO4
Слайд 28Химические свойства щелочей
4. Взаимодействуют с cолями, если в результате образуется нерастворимое основание:
Примеры:

Слайд 29Химические свойства щелочей
4. Взаимодействуют с cолями, если в результате образуется нерастворимое основание:
Примеры:

6NaOH + Cr2(SO4)3 → 3Na2SO4 + 2Cr(OH)3↓
Слайд 30Химические свойства щелочей
4. Взаимодействуют с cолями, если в результате образуется газообразное вещество:

Ca(OH)2 + NH4Cl → NH3↑ + H2O +NaCl
Слайд 31Получение щелочей
1. Реакции активных металлов (щелочных и щелочноземельных) с водой:
2Na

+ 2H2O → 2NaOH + H2↑
Ca + 2H2O → Ca(OH)2 + H2↑
2K + 2H2O → 2KOH + H2↑
Слайд 32Получение щелочей
2. Взаимодействие оксидов активных металлов с водой:
Примеры:
CaO + H2O →Ca(OH)2

– реакция гашения извести
Na2O + H2O → 2NaOH
BaO + H2O → Ba(OH)2
Слайд 33Получение щелочей
3. Электролиз водных растворов солей:
2NaCl + 2H2O –эл-з→ 2NaOH +

H2↑ + Cl2↑
Слайд 34Выводы
Щелочи – твердые кристаллические вещества, растворимые в воде.
- Щелочи образуют только щелочные

и щелочноземельные металлы.
- Получают щелочи реакцией щелочных и щелочноземельных металлов, а также их оксидов с водой; электролизом растворов солей активных металлов.
- Щелочи взаимодействуют с кислотами, с кислотными оксидами. А также с растворами некоторых солей.


































 Гидролиз неорганических солей
Гидролиз неорганических солей Блеск и сила волос с точки зрения химии
Блеск и сила волос с точки зрения химии Выделение и модификация древесных полимеров с получением биоактивных полимеров и матриц
Выделение и модификация древесных полимеров с получением биоактивных полимеров и матриц Алканы
Алканы Тест для подготовки к ГИА по химии
Тест для подготовки к ГИА по химии Типы химической связи
Типы химической связи Способы получения металлов. Сплавы металлов
Способы получения металлов. Сплавы металлов Растворение
Растворение Карбоновые кислоты
Карбоновые кислоты Соединения серы. Сернистая и серная кислоты
Соединения серы. Сернистая и серная кислоты Составление химических формул по валентности
Составление химических формул по валентности Классы неорганических веществ
Классы неорганических веществ Значение и применение спиртов
Значение и применение спиртов Вывод формул химических веществ
Вывод формул химических веществ Свойства нефти
Свойства нефти Свойства растворов и их взаимодействие с газовой фазой
Свойства растворов и их взаимодействие с газовой фазой Строение атома
Строение атома Капроновая (гексановая) кислота
Капроновая (гексановая) кислота Квантовая химия
Квантовая химия Основные положения теории строения органических соединений А. М. Бутлерова. Многообразие органических соединений
Основные положения теории строения органических соединений А. М. Бутлерова. Многообразие органических соединений Турнир Деда Мороза. Викторина по химии
Турнир Деда Мороза. Викторина по химии Алкены (этиленовые углеводороды)
Алкены (этиленовые углеводороды) Химический состав живых организмов. Метаболизм
Химический состав живых организмов. Метаболизм Ароматические соединения. Галогенпроизводные
Ароматические соединения. Галогенпроизводные Электролитическая диссоциация
Электролитическая диссоциация Сплавы металлов
Сплавы металлов Презентация на тему Таблица Менделеева и строение атома
Презентация на тему Таблица Менделеева и строение атома  Курсовая работа. Синтез адипиновой кислоты
Курсовая работа. Синтез адипиновой кислоты