Содержание
- 2. Формула соляной кислоты - HCL
- 3. Физические свойства Хлороводород – бесцветный газ с резким запахом, ядовитый, тяжелее воздуха. Легко растворяется в воде
- 4. Соляная кислота – раствор хлороводорода в воде; сильная одноосновная кислота. Концентрированная соляная кислота – бесцветный раствор,дымит
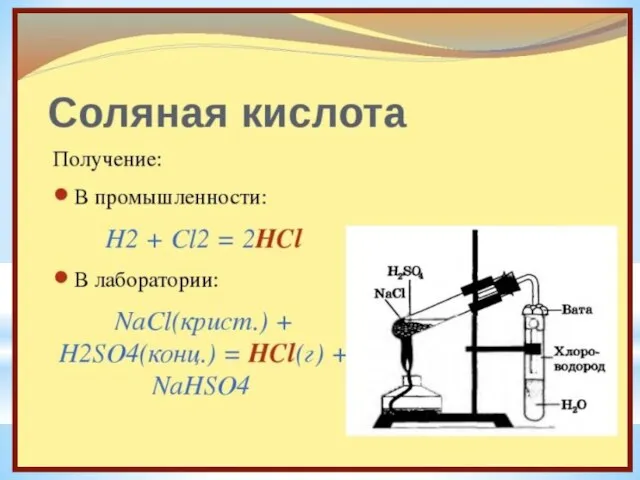
- 5. Получение 1) Промышленный способ H2 + Cl2 = 2HCl 2) Лабораторный способ NaCl(тв.) + H2SO4(конц.) =
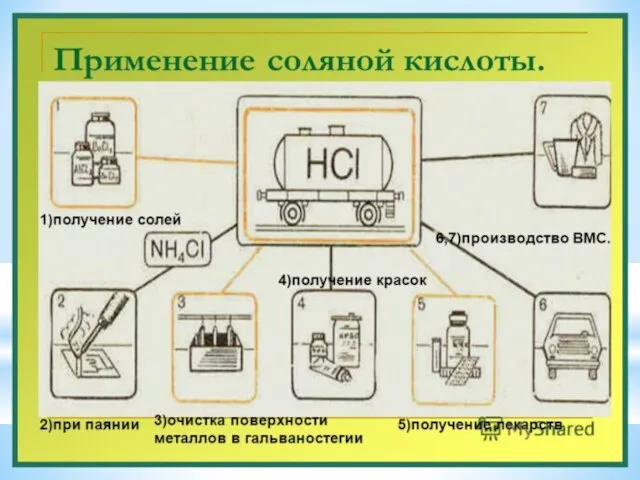
- 7. Химические свойства соляной кислотой 1. Изменение окраски индикаторов. HCl→H + Cl 2. Взаимодействие с металлами, стоящими
- 8. Качественная реакция на хлорид-ион HCl + AgNO3 → AgCl↓ + HNO3 белый творожистый осадок
- 11. Скачать презентацию






 Методы повышения надежности. Резервирование сложных ХТС
Методы повышения надежности. Резервирование сложных ХТС Окислительно-восстановительные реакции. 8 класс
Окислительно-восстановительные реакции. 8 класс Кристаллы и минералы
Кристаллы и минералы Лайфхаки на кухне
Лайфхаки на кухне Наука Химия на Великой Отечественной войне
Наука Химия на Великой Отечественной войне Презентация на тему Привычная и удивительная поваренная соль
Презентация на тему Привычная и удивительная поваренная соль  Химия. Электролитическая диссоциация. (9 класс)
Химия. Электролитическая диссоциация. (9 класс) Карбоцепные полимеры
Карбоцепные полимеры Цельное молоко: полезно или опасно для здоровья? (сравнительная характеристика качества восстановленного и цельного молока)
Цельное молоко: полезно или опасно для здоровья? (сравнительная характеристика качества восстановленного и цельного молока) ЛБ 1 ОВР (1)
ЛБ 1 ОВР (1) Строение атома
Строение атома Обратимые и необратимые химические реакции. Химическое равновесие
Обратимые и необратимые химические реакции. Химическое равновесие Технологические процессы получения кислорода
Технологические процессы получения кислорода Углеводороды: изомерия
Углеводороды: изомерия Ковалентная химическая связь
Ковалентная химическая связь Классификация гетероциклических соединений на основе их химического строения. Противоопухолевые средства
Классификация гетероциклических соединений на основе их химического строения. Противоопухолевые средства Валентность. Составление формул по валентности
Валентность. Составление формул по валентности Алкины
Алкины История и методология химии
История и методология химии Теория электролитической диссоциации
Теория электролитической диссоциации Термодинамическое равновесие между фазами
Термодинамическое равновесие между фазами Составление формул по валентности
Составление формул по валентности Гликоген. Синтез гликогена
Гликоген. Синтез гликогена Карбоновые кислоты
Карбоновые кислоты Стехиометрические законы химии
Стехиометрические законы химии Минералы
Минералы Презентация на тему Всё об алюминии
Презентация на тему Всё об алюминии  Использование ИКТ в преподавании химии. Современный урок
Использование ИКТ в преподавании химии. Современный урок