Содержание
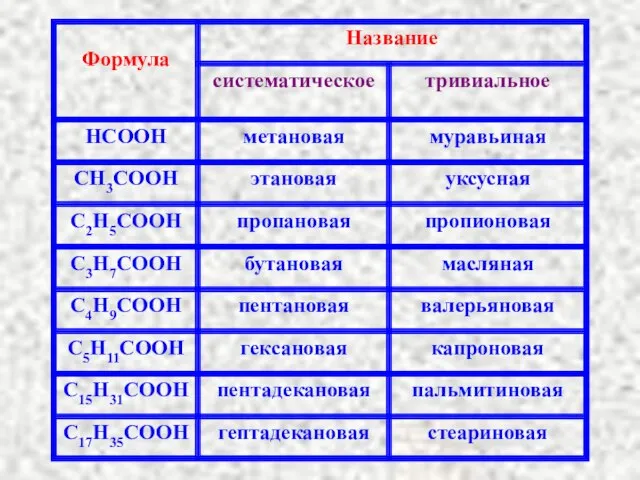
- 2. Karboksüülhapped – карбоновые кислоты Rasvhapped - жирные кислоты Aminohapped - аминокислоты Kaksikioon – биполярный ион Piptiidside
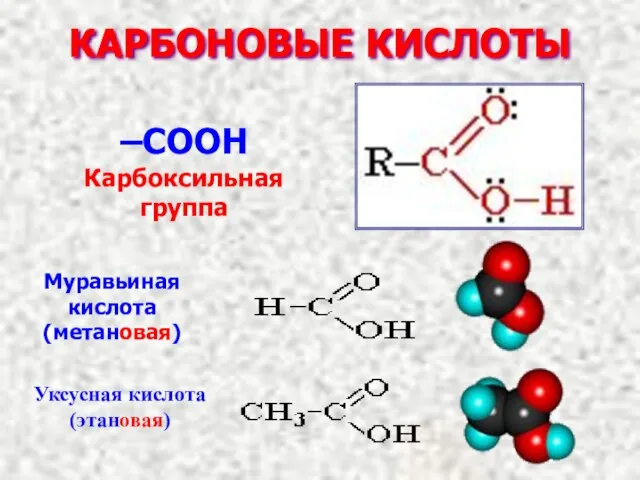
- 3. КАРБОНОВЫЕ КИСЛОТЫ –COOH Карбоксильная группа
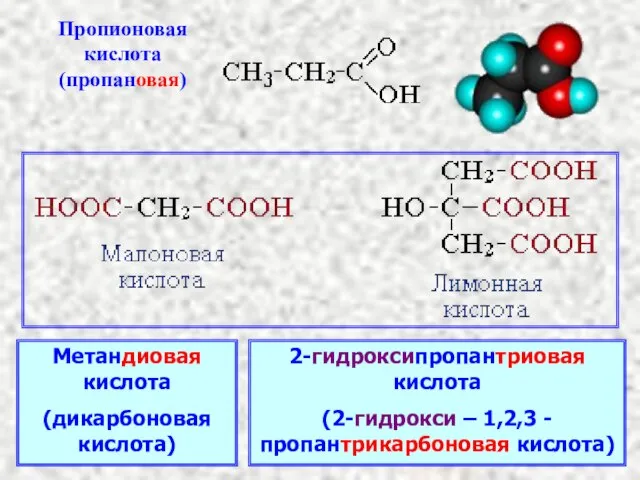
- 4. Метандиовая кислота (дикарбоновая кислота) 2-гидроксипропантриовая кислота (2-гидрокси – 1,2,3 -пропантрикарбоновая кислота)
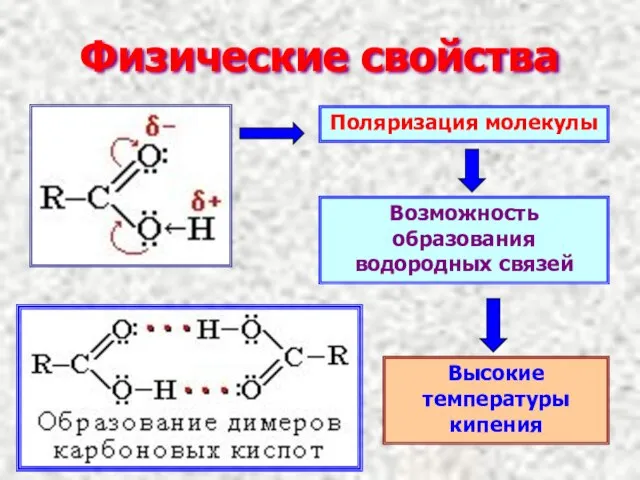
- 6. Физические свойства Поляризация молекулы Возможность образования водородных связей Высокие температуры кипения
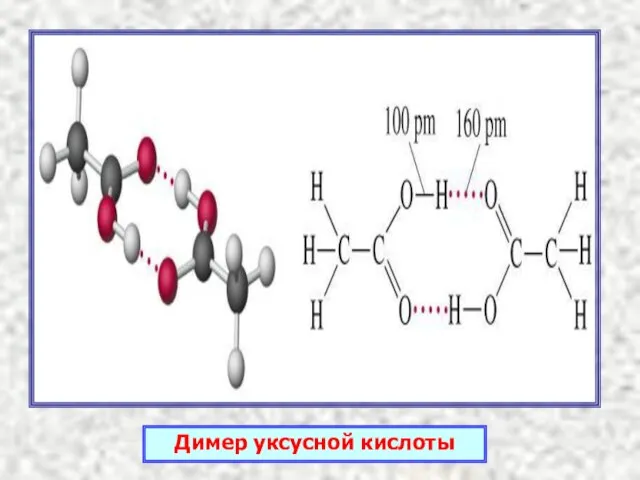
- 7. Димер уксусной кислоты
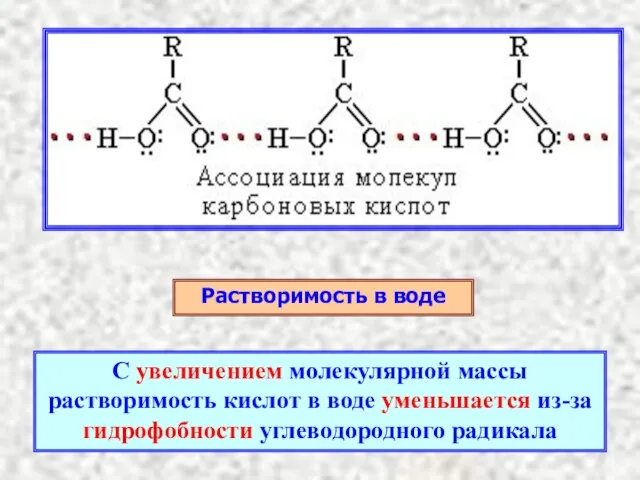
- 8. Растворимость в воде С увеличением молекулярной массы растворимость кислот в воде уменьшается из-за гидрофобности углеводородного радикала
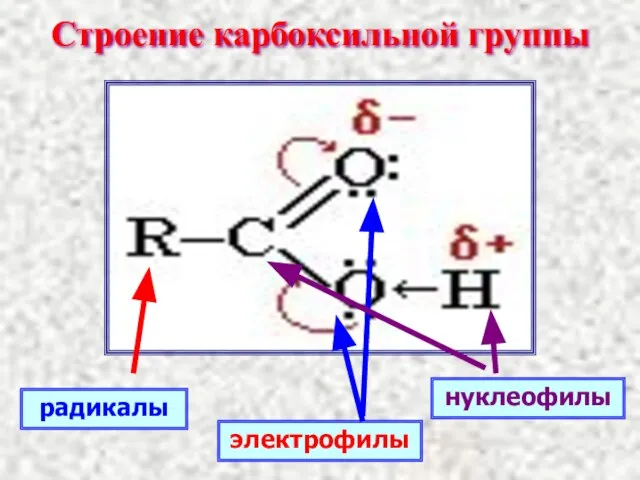
- 9. Строение карбоксильной группы радикалы нуклеофилы электрофилы
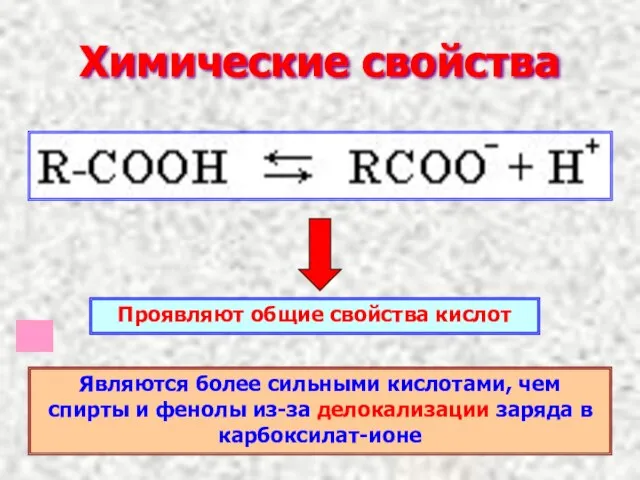
- 10. Химические свойства Проявляют общие свойства кислот Являются более сильными кислотами, чем спирты и фенолы из-за делокализации
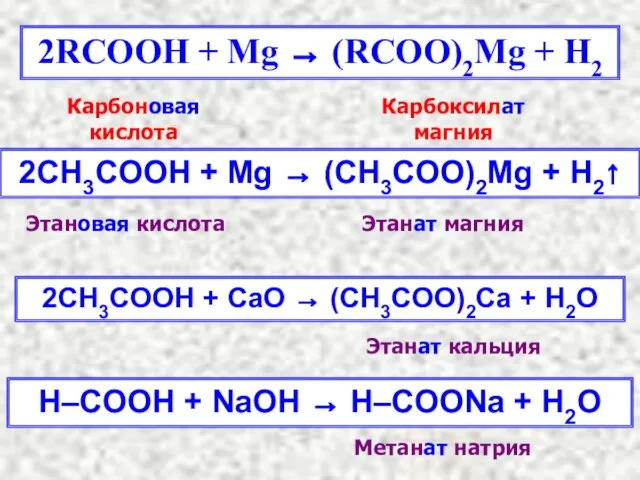
- 11. 2RCOOH + Mg → (RCOO)2Mg + H2 2СH3COOH + Mg → (CH3COO)2Mg + H2↑ Карбоновая кислота
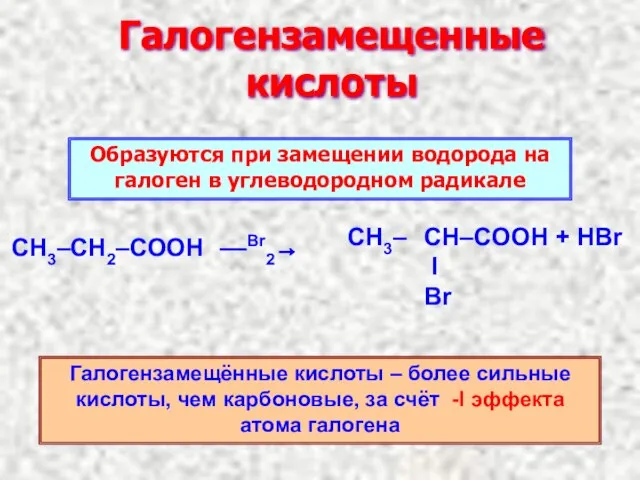
- 12. Галогензамещенные кислоты ––Br2→ Образуются при замещении водорода на галоген в углеводородном радикале Галогензамещённые кислоты – более
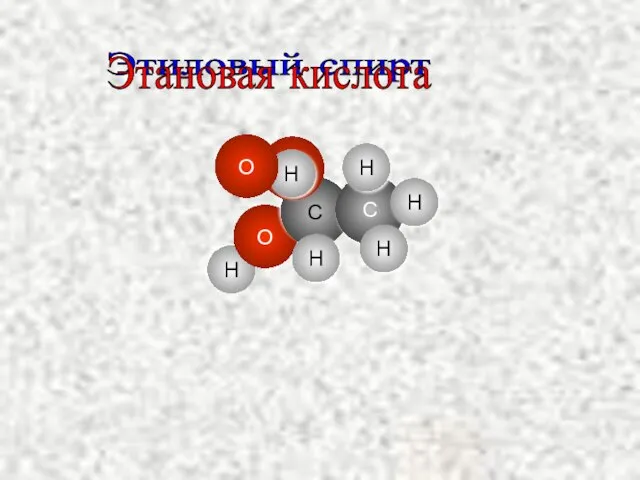
- 13. H O C O C H H H Этиловый спирт H H Этановая кислота O
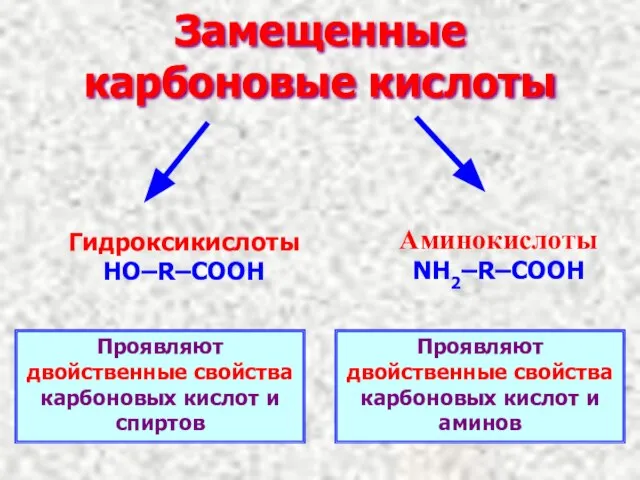
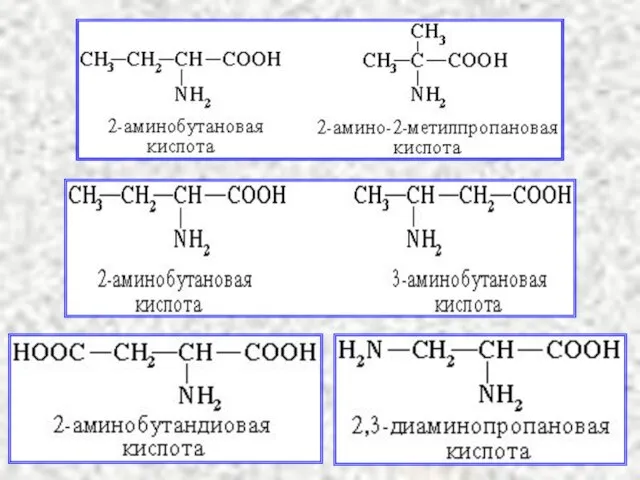
- 14. Замещенные карбоновые кислоты Гидроксикислоты HO–R–COOH Аминокислоты NH2–R–COOH Проявляют двойственные свойства карбоновых кислот и спиртов Проявляют двойственные
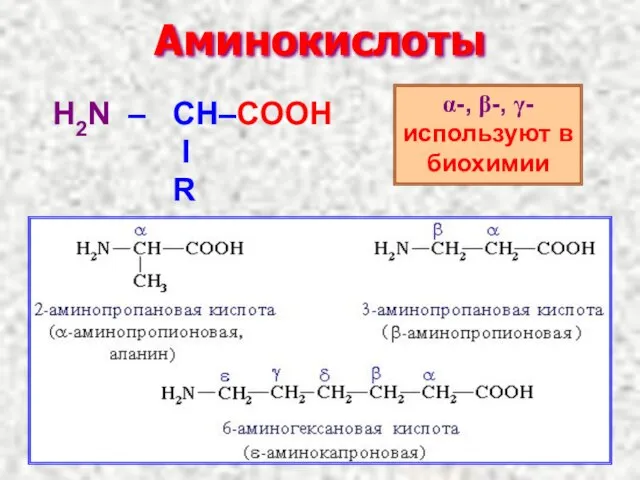
- 15. Аминокислоты α-, β-, γ- используют в биохимии
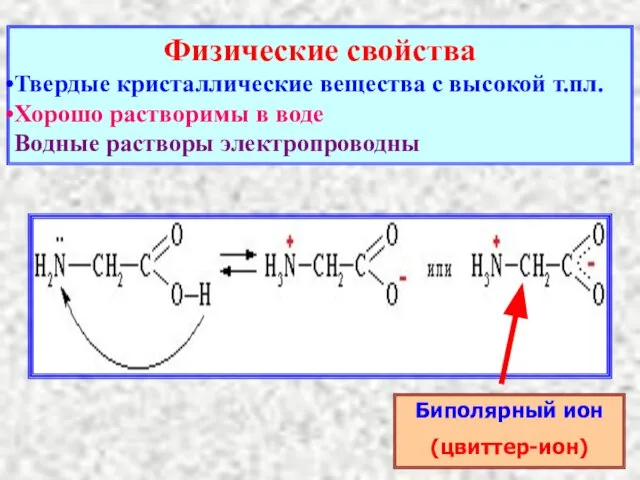
- 17. Физические свойства Твердые кристаллические вещества с высокой т.пл. Хорошо растворимы в воде Водные растворы электропроводны Биполярный
- 18. Химические свойства Аминокислоты являются амфотерными соединениями H2N–CH2–COOH + HCl → Cl− [H3N–CH2–COOH]+ Как основание H2N–CH2–COOH +
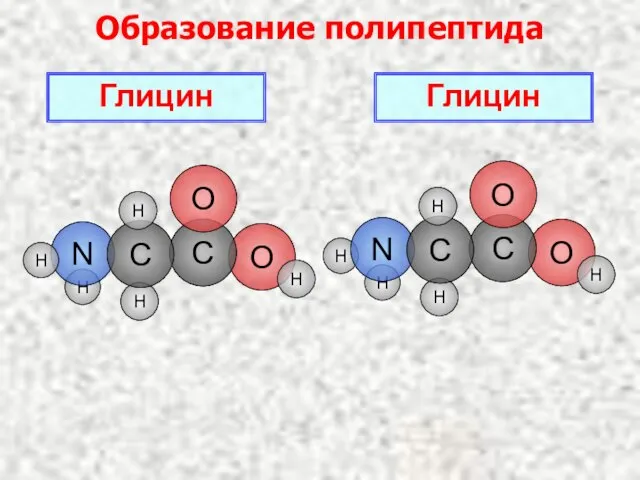
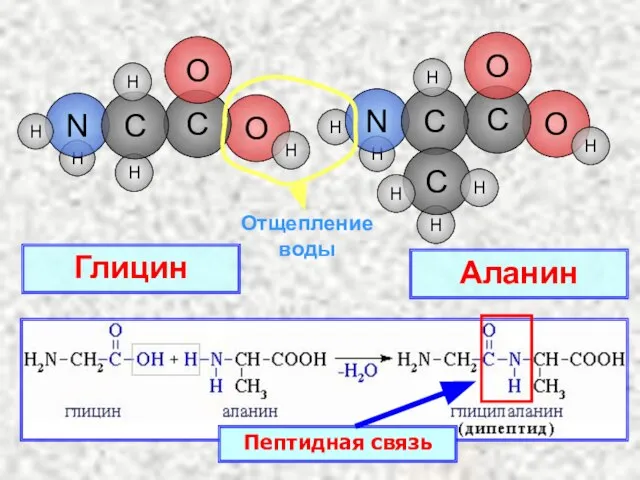
- 19. Образование полипептида Глицин H O H H Глицин
- 20. H O H H H H O C N O C H H C H H
- 22. Скачать презентацию

![Химические свойства Аминокислоты являются амфотерными соединениями H2N–CH2–COOH + HCl → Cl− [H3N–CH2–COOH]+](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/480101/slide-17.jpg)
 Перманганатометрия и комплексонометрия
Перманганатометрия и комплексонометрия Классификация неорганических соединений и реакций
Классификация неорганических соединений и реакций Системно-деятельностный подход в обучении химии
Системно-деятельностный подход в обучении химии Ртуть
Ртуть Великие ученые общей и неорганической химии
Великие ученые общей и неорганической химии Изучение микроклимата коровника с целью создания системы очистки воздуха от аммиака
Изучение микроклимата коровника с целью создания системы очистки воздуха от аммиака История открытия водорода. Получение и физические свойства водорода
История открытия водорода. Получение и физические свойства водорода Развитие химии
Развитие химии Электролитическая диссоциация
Электролитическая диссоциация Презентация на тему Бром
Презентация на тему Бром  Карбоновые кислоты и их гетерофункциональные производные: гидрокси- и оксокарбоновые кислоты
Карбоновые кислоты и их гетерофункциональные производные: гидрокси- и оксокарбоновые кислоты Электролитическая диссоциация
Электролитическая диссоциация Спирты и их производные. Применение метанола и этанола
Спирты и их производные. Применение метанола и этанола Галогенпроизводные углеводородов
Галогенпроизводные углеводородов 1.2. Измерения веществ
1.2. Измерения веществ Необходимые навыки для составления уравнений ОВР
Необходимые навыки для составления уравнений ОВР Изготовление индикаторной бумаги
Изготовление индикаторной бумаги Химические и физические явления
Химические и физические явления Презентация на тему Cкорость химических реакций
Презентация на тему Cкорость химических реакций  Минерал дунит
Минерал дунит Алмазы
Алмазы Алкины
Алкины Алкены.Номенклатура
Алкены.Номенклатура Жаропрочные и жаростойкие стали
Жаропрочные и жаростойкие стали Массовая доля элемента в веществе
Массовая доля элемента в веществе Получение алканов
Получение алканов Алкоголь и мозг
Алкоголь и мозг Удивительные свойства латекса и его применение
Удивительные свойства латекса и его применение