Содержание
- 2. Как повысить скорость химической реакции: А2(г)+ 3В2(г) = 2АВ3 в 81 раз?
- 3. Скорость химических реакций - 2
- 4. Задачи урока: 1) повторение понятий «скорость химических реакций», «факторы, оказывающие влияние на скорость химических реакций», 2)
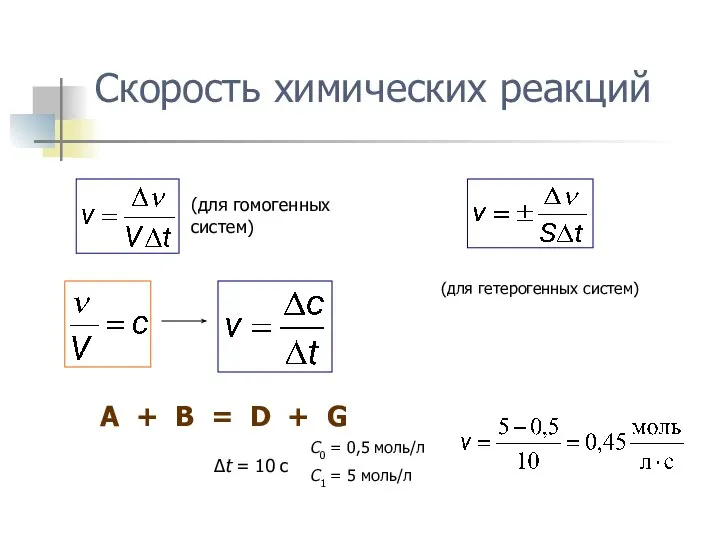
- 5. Скорость химических реакций (для гомогенных систем) A + B = D + G C0 = 0,5
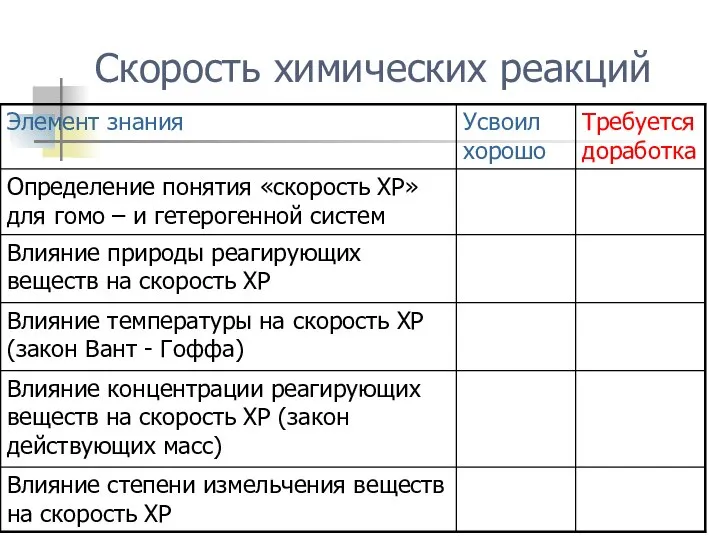
- 6. Факторы, от которых зависит скорость реакции Природа реагирующих веществ Концентрация веществ в системе (давление в газовой
- 7. Закон действующих масс A + B → D + F v = Като Гульдберг (1836-1902) Петер
- 8. Закон действующих масс A + B → D + F v = k · c (A)
- 9. Влияние температуры Правило Вант-Гоффа - температурный коэффициент Вант-Гоффа v = Якоб Вант-Гофф (1852-1911)
- 10. Влияние температуры Правило Вант-Гоффа При нагревании системы на 10 ˚С скорость реакции возрастает в 2-4 раза
- 11. Катализ ввел термин «катализ» в 1835 г. Катализатор – вещество, изменяющее скорость реакции, участвует в промежуточных
- 12. Катализ Йенс Якоб Берцелиус ввел термин «катализ» в 1835 г. Катализатор – вещество, изменяющее скорость реакции,
- 13. Теперь к вопросам ЕГЭ!
- 14. A20-2012 Скорость гомогенной химической реакции пропорциональна изменению: 1)количества вещества в единице объема 2) массы вещества в
- 15. A20-2012 В системе А + В =АВ концентрация вещества А по истечении 5 сек изменилась от
- 16. A20-2012 Какой из факторов не оказывает влияния на скорость химической реакции в растворах? 1) концентрация вещества
- 17. A20-2012 На скорость химической реакции между раствором серной кислоты и железом не оказывает влияния 1) концентрация
- 18. A20-2012 Для увеличения скорости химической реакции Mg (тв.) + 2H+ = Mg2+ + H2(г.) необходимо 1)
- 19. A20-2012 C наибольшей скоростью при обычных условиях протекает реакция 1) 2Ba + O2 = 2BaO 2)
- 20. A20-2012 Для увеличения скорости реакции 2CO + O2 = 2CO2 + Q необходимо 1) повысить температуру
- 21. A20-2012 Быстрее при комнатной температуре будет протекать реакция между 10%- ным раствором соляной кислоты и 1)
- 22. A20-2012 С наименьшей скоростью при обычных условиях протекает реакция: 1) Fe + O2 2) CaCO3 +
- 23. A20-2012 При увеличении температуры от 10 до 30 0С скорость реакции, температурный коэффициент которой равен 3,
- 24. A20-2012 При увеличении концентрации СО в 2 раза в системе: 2СО + О2 = 2 СО2,
- 25. A20-2012 При увеличении давления в системе N2 + 3H2 = 2NH3 в 3 раза скорость прямой
- 26. Самостоятельная работа по теме «Скорость химической реакции» по материалам и в форме ЕГЭ
- 27. Самостоятельная работа Вариант 1 Вариант 2 1. 1 1. 3 2. 4 2. 1 3. 1
- 28. Самостоятельная работа Вариант 1 1. С наибольшей скоростью с водородом реагирует 1. CI2 2. N2 3.
- 29. Самостоятельная работа Вариант 1 3. Увеличение скорости разложения бертолетовой соли KCIO3 в большей степени зависит от
- 30. Самостоятельная работа Вариант 1 5. Растворение магния в соляной кислоте будет замедляться при 1. увеличении концентрации
- 31. Самостоятельная работа Вариант 1 7. Скорость реакции 2H 2S(г)+3O 2(г)=2H 2O(ж)+2SO 2(г) при увеличении давления в
- 32. Самостоятельная работа Вариант 2 1. С наибольшей скоростью с водой реагирует 1. Pb 2. Mg 3.
- 33. Самостоятельная работа Вариант 2 3. Скорость реакции S+O2=SO2 уменьшается при 1. нагревании 2. увеличении давления 3.
- 34. Самостоятельная работа Вариант 2 5. С наименьшей скоростью происходит реакция между цинком и 1. HCI(20%-ный p-p)
- 35. Самостоятельная работа Вариант 2 7. Скорость реакции 2H 2S(г)+3O 2(г)=2H 2O(ж)+2SO 2(г) при уменьшении давления в
- 36. Факторы, от которых зависит скорость реакции Природа реагирующих веществ Концентрация веществ в системе (давление в газовой
- 37. Как повысить скорость химической реакции: А2(г)+ 3В2(г) = 2АВ3 в 81 раз?
- 38. Как повысить скорость химической реакции: А2(г)+ 3В2(г) = 2АВ3 в 81 раз? А) повысить температуру на
- 39. Задачи урока: 1) повторение понятий «скорость химических реакций», «факторы, оказывающие влияние на скорость химических реакций», 2)
- 40. Скорость химических реакций
- 42. Скачать презентацию




































 Ферменттер.Ферменттердің құрылымы.Биохимиялық маңызы
Ферменттер.Ферменттердің құрылымы.Биохимиялық маңызы Кристаллы. Формирование кристаллов
Кристаллы. Формирование кристаллов Игровые технологии на уроках химии как средство реализации системно-деятельного подхода в обучении
Игровые технологии на уроках химии как средство реализации системно-деятельного подхода в обучении Кислоты
Кислоты Вода знакомая и не знакомая
Вода знакомая и не знакомая Алканы
Алканы Презентация на тему Ковалентная связь: полярная и неполярная
Презентация на тему Ковалентная связь: полярная и неполярная  Ртуть. Правила работы со ртутью
Ртуть. Правила работы со ртутью Золото
Золото Коррозия металлов
Коррозия металлов Расчетная работа. Тепловой эффект клинкерообразования
Расчетная работа. Тепловой эффект клинкерообразования Составление ионных уравнений
Составление ионных уравнений Углеводороды: соединения, состоящие из углерода и водорода
Углеводороды: соединения, состоящие из углерода и водорода Презентация на тему Органическая химия "Жиры"
Презентация на тему Органическая химия "Жиры"  Плотность вещества
Плотность вещества Получение металлов
Получение металлов Высокомолекулярные соеденения
Высокомолекулярные соеденения Производство органических препаратов ароматического ряда
Производство органических препаратов ароматического ряда Степень окисления
Степень окисления Молекулярная химия
Молекулярная химия Возможные роли АФК в старении
Возможные роли АФК в старении Разнообразие веществ. 3 класс
Разнообразие веществ. 3 класс Обобщение знаний по курсу органической химии
Обобщение знаний по курсу органической химии Влияние кислотности среды на свойство белка
Влияние кислотности среды на свойство белка Ионные реакции
Ионные реакции Кислотные оксиды
Кислотные оксиды Кислород
Кислород Гальванический элемент
Гальванический элемент