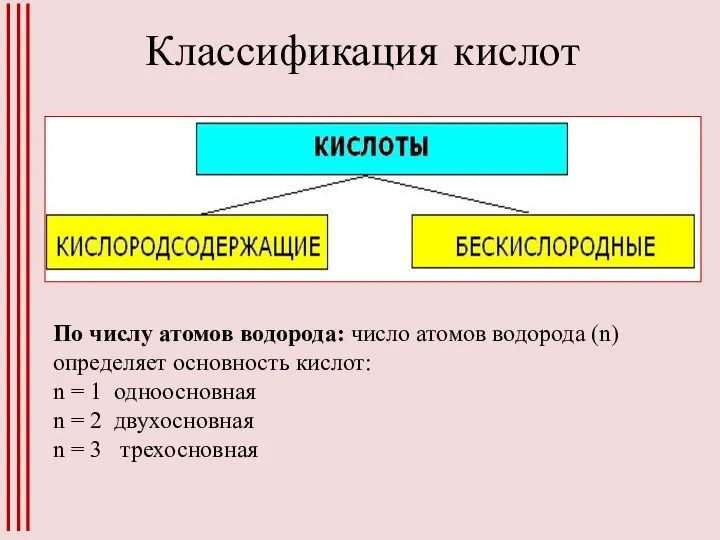
Слайд 2Классификация кислот
По числу атомов водорода: число атомов водорода (n) определяет основность кислот:
n = 1
одноосновная
n = 2 двухосновная
n = 3 трехосновная
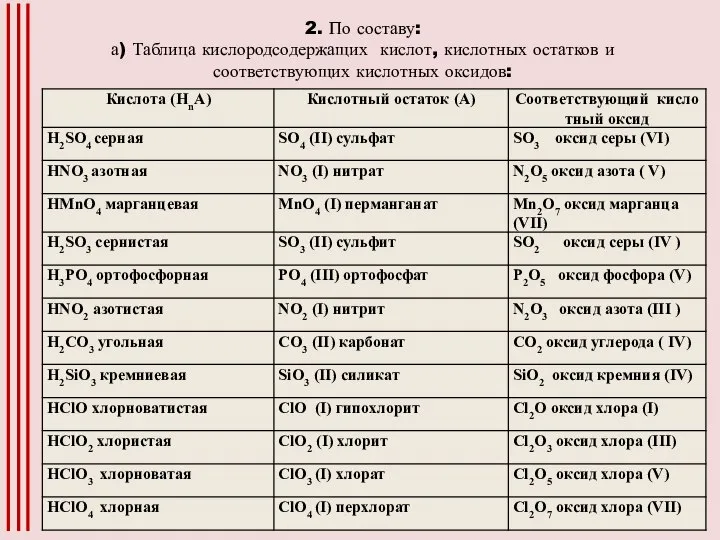
Слайд 32. По составу:
а) Таблица кислородсодержащих кислот, кислотных остатков и соответствующих кислотных оксидов:
Слайд 4б) Таблица бескислородных кислот
Физические свойства кислот
Многие кислоты, например серная, азотная, соляная –

это бесцветные жидкости. Известны также твёрдые кислоты: ортофосфорная, метафосфорная HPO3, борная H3BO3. Почти все кислоты растворимы в воде. Пример нерастворимой кислоты – кремниевая H2SiO3. Растворы кислот имеют кислый вкус. Так, например, многим плодам придают кислый вкус содержащиеся в них кислоты. Отсюда названия кислот: лимонная, яблочная и т.д.




 Коррозия металлов. Экзаменационные вопросы
Коррозия металлов. Экзаменационные вопросы Chemsheets AS 1009 (Electron arrangement)
Chemsheets AS 1009 (Electron arrangement) Обобщение по теме Теория химического строения органических веществ
Обобщение по теме Теория химического строения органических веществ Классификация процессов коррозии
Классификация процессов коррозии Обобщение и систематизация знаний по теме Углеводороды
Обобщение и систематизация знаний по теме Углеводороды Презентация на тему Галогены и здоровье человека
Презентация на тему Галогены и здоровье человека  Производство аммиака
Производство аммиака Хімія у вирішенні промислової проблеми
Хімія у вирішенні промислової проблеми Презентация на тему Металлы и неметаллы
Презентация на тему Металлы и неметаллы  Презентация на тему Мыло. Синтетические моющие средства
Презентация на тему Мыло. Синтетические моющие средства  Презентация на тему Палладий
Презентация на тему Палладий  Классификация НПВС (по химической структуре активности)
Классификация НПВС (по химической структуре активности) Растворы. Процесс растворения (1)
Растворы. Процесс растворения (1) Формирование универсальных учебных действий
Формирование универсальных учебных действий Строение атома
Строение атома ЛК 2_окислительно-восстановительные процессы
ЛК 2_окислительно-восстановительные процессы Презентация на тему Основные законы химии
Презентация на тему Основные законы химии  Предельные углеводороды Алканы
Предельные углеводороды Алканы Железо в продуктах питания
Железо в продуктах питания Презентация на тему: Чистые вещества и смеси
Презентация на тему: Чистые вещества и смеси Оксиды азота
Оксиды азота Органические вещества
Органические вещества Презентация на тему Альдегиды (10 класс)
Презентация на тему Альдегиды (10 класс)  Получение формальдегида методом дегидрирования метанола
Получение формальдегида методом дегидрирования метанола Окислительновосстановительные индикаторы. Задача 12 Команда: Мастера Беспорядка
Окислительновосстановительные индикаторы. Задача 12 Команда: Мастера Беспорядка Реакции этерификации
Реакции этерификации Проточные реакторы непрерывного действия. (Лекция 5)
Проточные реакторы непрерывного действия. (Лекция 5) Разминка
Разминка