Содержание
- 2. «Ядерная физика и технологии», «Физика материалов и процессов», «Ядерная физика и космофизика», «Ядерная медицина» «Физика элементарных
- 3. 1часть: Основы теории химии электронное строение атома и химическая связь химическая термодинамика, химическая кинетика химическое равновесие,
- 4. 1 семестр - зачет 2 семестр - экзамен Российская и международная система оценок Работа в семестре
- 5. Коровин Н.В. Общая химия. М.: Высшая школа. 2002, 2013 Ахметов, Н.С. Общая и неорганическая химия/Н.С. Ахметов.
- 6. Электронные курсы по Химии отдел дистанционного образования Управления ДПО Ананьева Е.А., Глаголева М.А., Звончевская М.Ф., Кучук
- 7. теоретическая часть; иллюстрации, видео, анимация; гиперссылки, аннотированные ссылки; контрольные и учебные тесты; глоссарий, персоналии. Что в
- 8. Где их найти?
- 9. Как выбрать курс? На главной странице СДО перейти по ссылке «Подать заявку»
- 10. Электронные курсы по Химии отдел дистанционного образования Управления ДПО Ананьева Е.А., Глаголева М.А., Звончевская М.Ф., Кучук
- 11. теоретическая часть; иллюстрации, видео, анимация; гиперссылки, аннотированные ссылки; контрольные и учебные тесты; глоссарий, персоналии. Что в
- 12. Где их найти?
- 13. Как выбрать курс? На главной странице СДО перейти по ссылке «Подать заявку»
- 14. ЛЕКЦИЯ 1 ХИМИЧЕСКИЕ СИСТЕМЫ Введение Химия, как наука Химические системы Характеристика химических систем: Вещество, структурная единица
- 15. Классификация фундаментальных наук на уровне макрообъектов
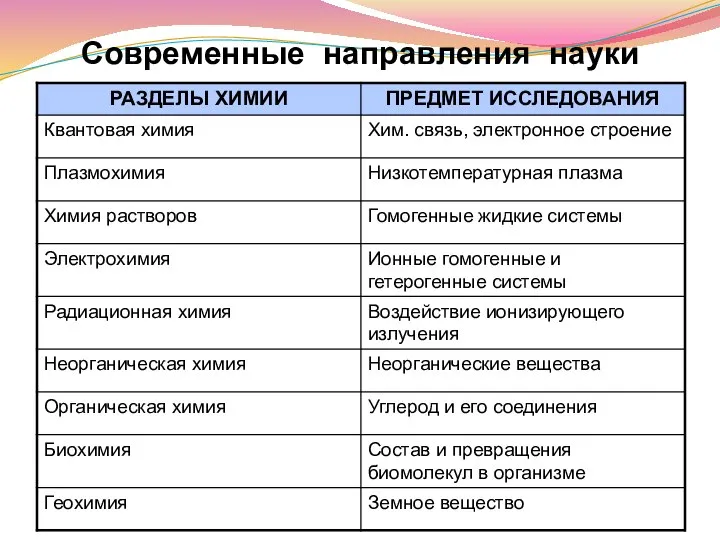
- 16. Современные направления науки
- 17. Химические системы - совокупность микро- и макроколичеств веществ, способных под воздействием внешних факторов к превращениям с
- 18. Факторы, условия Условия, при которых протекают реакции, принято указывать над стрелкой символизирующей химические превращения (р,Т, hν,
- 19. Факторы, условия кислотность среды
- 20. Характеристика кислотности среды Кислотность раствора определяется концентрацией ионов водорода. в нейтральной [H+] = [OH-] в кислой
- 21. Структурные единицы вещества: Атом – наименьшая частица химического элемента, сохраняющая все его химические свойства, электронейтральная система,
- 22. Простые вещества – вещества , молекулы которых состоят из атомов одного и того же элемента. газ
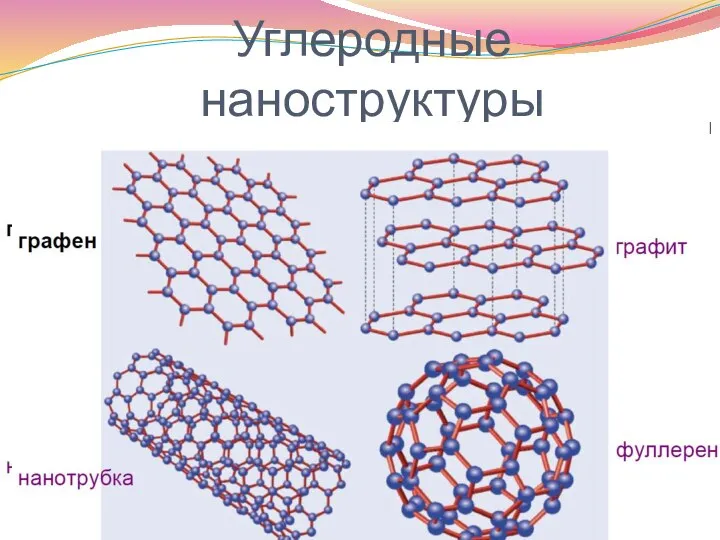
- 23. Углеродные наноструктуры
- 24. УГЛЕРОДНАЯ ЭЛЕКТРОНИКА ГРАФЕН
- 25. Основные признаки химических превращений выделение газа: образование осадка: выделение или поглощение тепла: изменение цвета, как результат
- 26. Метод классической химии Нобелевский лауреат Р. Фейнман: «Чтобы узнать, как расположены атомы в какой-нибудь невероятно сложной
- 27. Типы химических реакций Классификационные признаки: 1. Число и состав исходных веществ и продуктов реакции. 2. Тип
- 28. Типы химических реакций Реакция разложения: CaCO3 → CaO↓ + CO2↑ Реакция соединения: CO2↑ + H2O →
- 29. Ионно-молекулярные уравнения химических реакций Для того чтобы ионно-молекулярные уравнения правильно отражали механизм процесса, необходимо придерживаться следующей
- 30. Сильные электролиты Сильные кислоты: НNO3, HCl, HBr, HI, HClO4, H2SO4 и т.д. HnSOm где m-n ≥
- 31. Вещества, остающиеся ввиде молекул, при составлении ионных уравнений оксиды (пероксиды): BaO, P2O5, Al2O3, H2O, H2O2 и
- 32. Примеры ионных уравнений выделение газа выпадение осадка образоване малодис-социирующего вещества
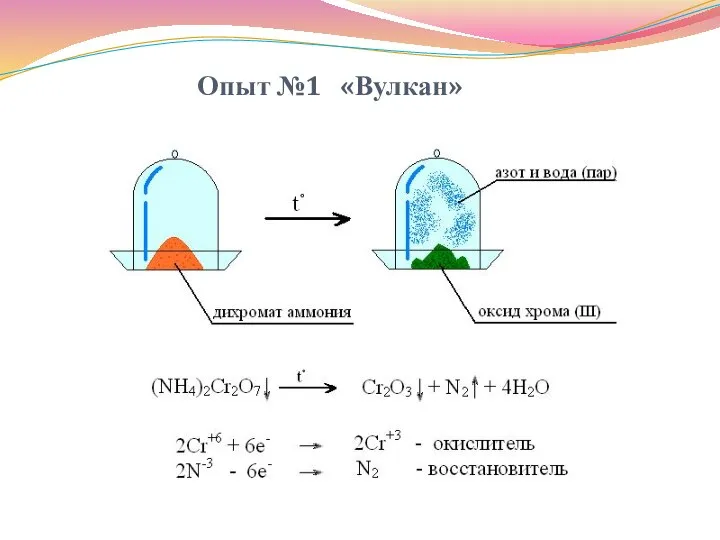
- 33. Опыт №1 «Вулкан»
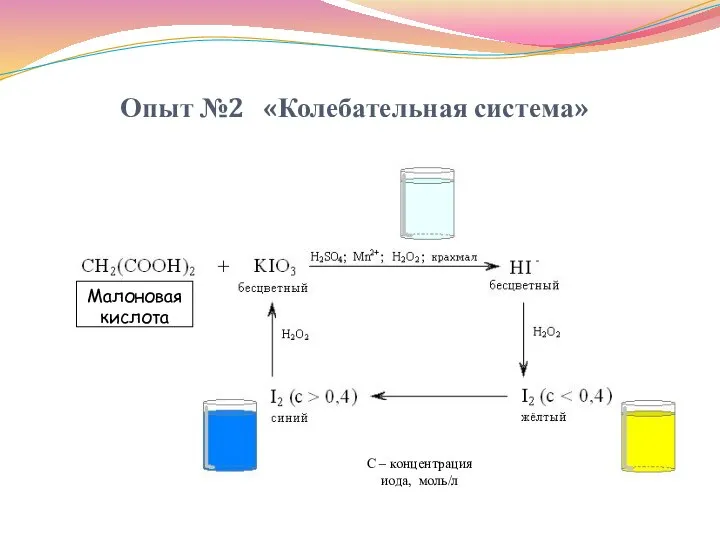
- 34. Опыт №2 «Колебательная система» Малоновая кислота С – концентрация иода, моль/л
- 35. Химическая двойственность Амфотерность гидроксида алюминия Al(OH)3 : Al(OH)3 + 3HCl → AlCl3 + 3HCl (pH основание
- 37. Скачать презентацию















![Характеристика кислотности среды Кислотность раствора определяется концентрацией ионов водорода. в нейтральной [H+]](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1086340/slide-19.jpg)












 Химическое равновесие
Химическое равновесие Химия и география. Блиц-опрос. 7 класс
Химия и география. Блиц-опрос. 7 класс Амилаза. Строение амилазы
Амилаза. Строение амилазы Моющие и чистящие средства
Моющие и чистящие средства Основные химические законы
Основные химические законы Соли: получение
Соли: получение Синтетическое моторное масло. Маркировка моторных масел
Синтетическое моторное масло. Маркировка моторных масел Khim_8
Khim_8 Химические реакции
Химические реакции Систематизация знаний по периодической системе химических элементов
Систематизация знаний по периодической системе химических элементов химия
химия Nevarne snovi
Nevarne snovi Основания. Классификация
Основания. Классификация Стелс-материалы
Стелс-материалы Тип кристаллической решетки у белого фосфора…. Тест
Тип кристаллической решетки у белого фосфора…. Тест Классификация и свойства кислот
Классификация и свойства кислот Сeквенирование нуклеиновых кислот
Сeквенирование нуклеиновых кислот Набор для выращивания монокристалла. Защита проекта
Набор для выращивания монокристалла. Защита проекта Алканы. Строение, номенклатура, изомерия, физические свойства
Алканы. Строение, номенклатура, изомерия, физические свойства Реакции разложения и соединения
Реакции разложения и соединения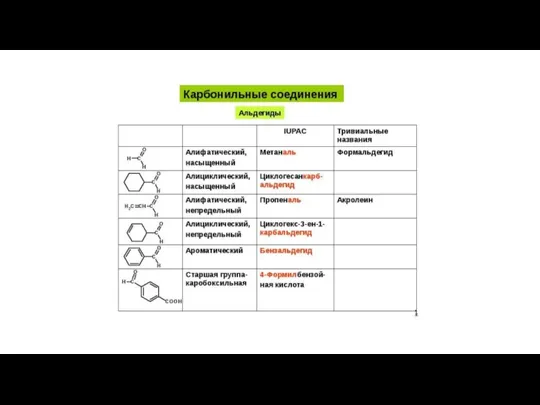 Карбонильные соединения (альдегиды)
Карбонильные соединения (альдегиды) карбоновые кислоты
карбоновые кислоты Вуглеводи. Групи
Вуглеводи. Групи Вычисление температур стеклования полимера при различных степенях отверждения смолы
Вычисление температур стеклования полимера при различных степенях отверждения смолы Сера
Сера Валенттілік. Атом-молекулалы ілім
Валенттілік. Атом-молекулалы ілім Классификация органических соединений
Классификация органических соединений Метанол. Краткая характеристика
Метанол. Краткая характеристика