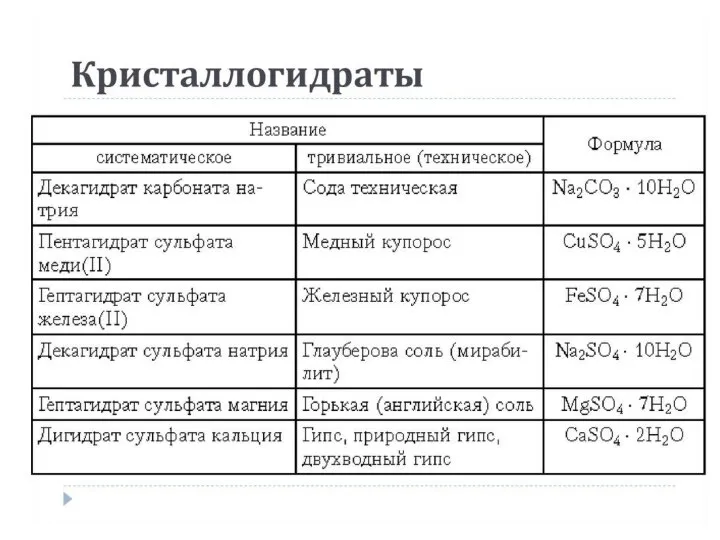
Слайд 7Кристаллогидраты – соли, содержащие связанную воду

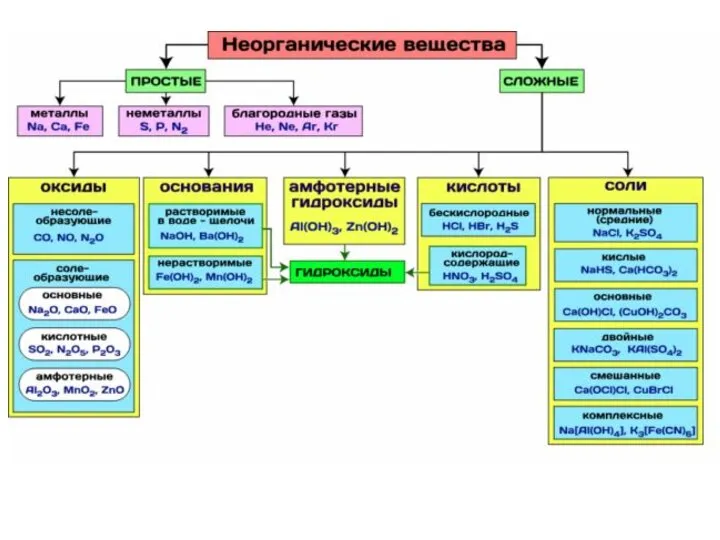
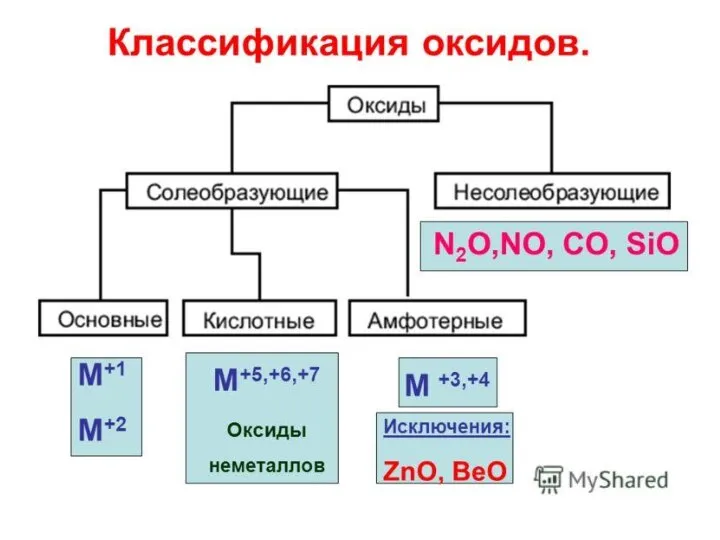
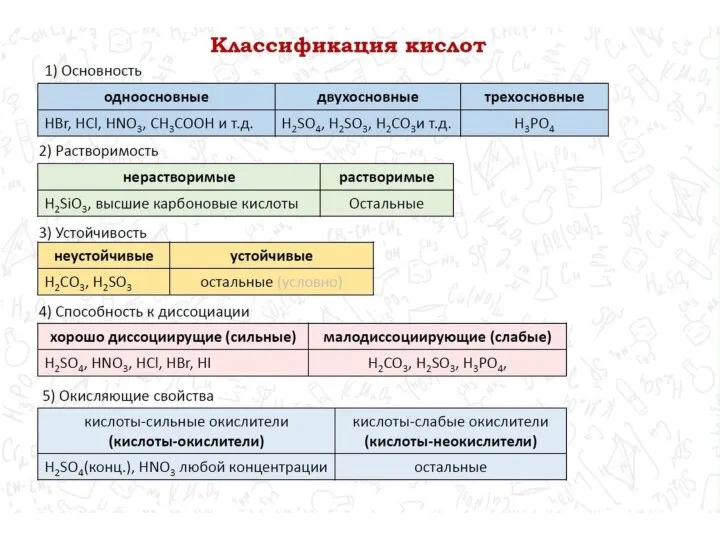
Слайд 9Задания ЕГЭ по классификации неорганических веществ (№5) 1 балл
Вывод – учим тривиальные

названия веществ!
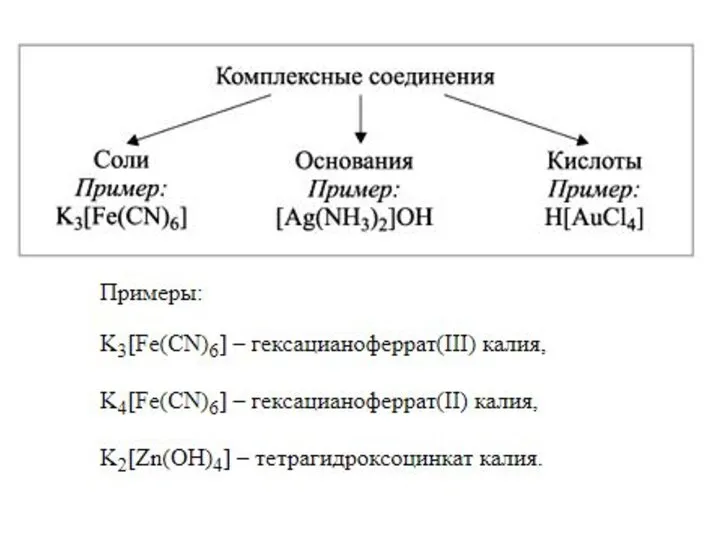
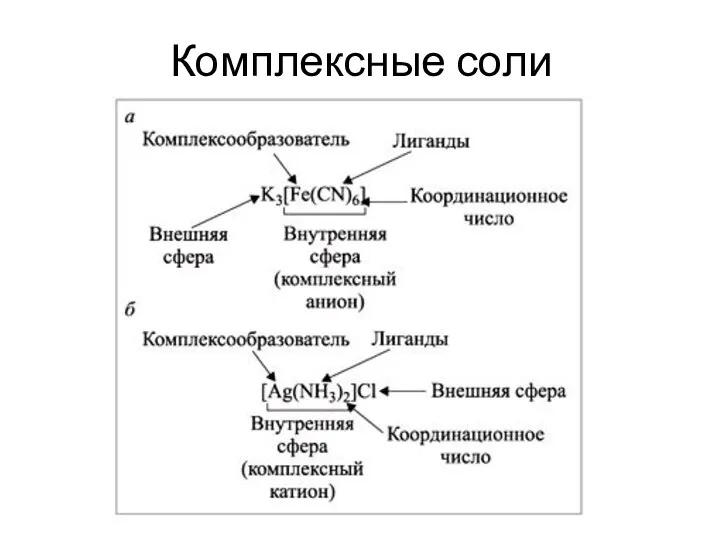
Слайд 15Химические свойства комплексных соединений
В растворе комплексные соединения ведут себя как сильные электролиты,

т.е. полностью диссоциируют на катионы и анионы:
[Pt(NH3)4]Cl2 = Pt(NH3)4]2+ + 2Cl–,
K2[PtCl4] = 2K+ + [PtCl4]2–.
Диссоциация по такому типу называется первичной.
Вторичная диссоциация связана с удалением лигандов из внутренней сферы комплексного иона:
[PtCl4]2– PtCl3– + Cl–.
Вторичная диссоциация происходит ступенчато: комплексные ионы ([PtCl4]2–) являются слабыми электролитами.
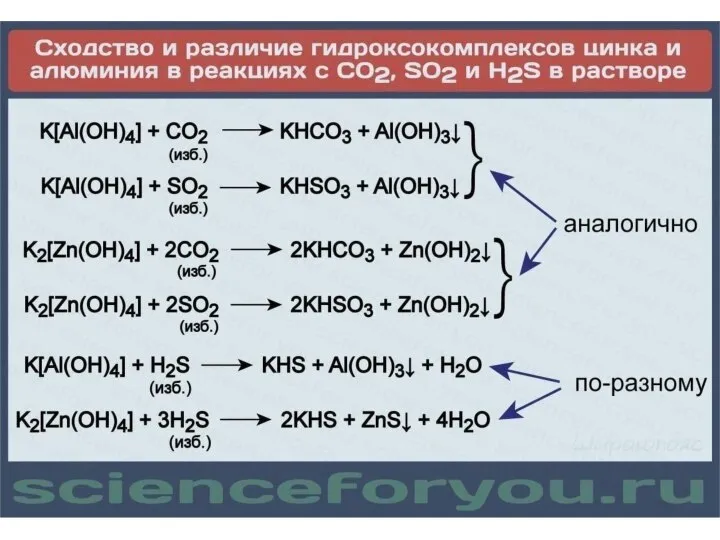
Слайд 162. При действии сильных кислот происходит разрушение гидроксокомплексов, например:
а) при недостатке кислоты
Na3[Al(OH)6] +

3HCl = 3NaCl + Al(OH)3 + 3H2O;
б) при избытке кислоты
Na3[Al(OH)6] + 6HCl = 3NaCl + AlCl3 + 6H2O.
3. Нагревание (термолиз) всех аммиакатов приводит к их разложению, например:
[Cu(NH3)4]SO4 CuSO4 + 4NH3.
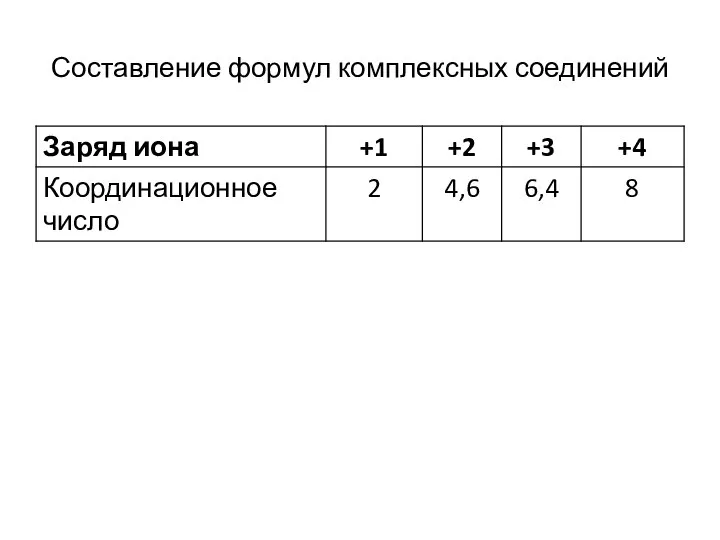
Слайд 17Составление формул комплексных соединений
Слайд 19Примеры заданий ЕГЭ № 32 (4 балла)
Медь растворили в разбавленной азотной кислоте.

К полученному раствору добавили избыток раствора аммиака, наблюдая сначала образование осадка, а затем — его полное растворение с образованием тёмно-синего раствора. Полученный раствор обработали серной кислотой до появления характерной голубой окраски солей меди. Запишите уравнения описанных реакций.
Слайд 20К раствору гидроксида натрия добавили порошок алюминия. Через раствор полученного вещества пропустили

избыток углекислого газа. Выпавший осадок отделили и прокалили. Полученный продукт сплавили с карбонатом натрия.










 Химические средства защиты растений
Химические средства защиты растений Степень окисления
Степень окисления Презентация на тему Стронций
Презентация на тему Стронций  углеводы (1)
углеводы (1) Протолитические буферные системы. Буферные системы организма, их взаимодействие
Протолитические буферные системы. Буферные системы организма, их взаимодействие Общая характеристика элементов подгруппы углерода. Углерод – его строение и свойства
Общая характеристика элементов подгруппы углерода. Углерод – его строение и свойства Коферменты. Промышленное получение и применение ферментов
Коферменты. Промышленное получение и применение ферментов Лиофильные и лиофобные дисперсные системы. Свойства лиофильных систем. Лекция 12
Лиофильные и лиофобные дисперсные системы. Свойства лиофильных систем. Лекция 12 Презентация на тему Альдегиды
Презентация на тему Альдегиды  Кислород
Кислород Классификация химических реакций
Классификация химических реакций Dereglarea metabolismului
Dereglarea metabolismului Окислительно-восстановительные реакции. Типы химических реакций
Окислительно-восстановительные реакции. Типы химических реакций Термокаталитические процессы переработки нефтяных фракций
Термокаталитические процессы переработки нефтяных фракций 175 – летию со дня рождения Дмитрия Ивановича Менделеева посвящается… АВТОР ПРЕЗЕНТАЦИИ: учитель химии МОУ СОШ №2 города Ртищево Саратовской области ПОПКОВА Е.Г.
175 – летию со дня рождения Дмитрия Ивановича Менделеева посвящается… АВТОР ПРЕЗЕНТАЦИИ: учитель химии МОУ СОШ №2 города Ртищево Саратовской области ПОПКОВА Е.Г. SHOT.шампуни. Состав. Компоненты
SHOT.шампуни. Состав. Компоненты Презентация на тему Количество вещества. Молярная масса
Презентация на тему Количество вещества. Молярная масса  Органическая химия. Теория строения органических соединений
Органическая химия. Теория строения органических соединений Характеристика кислорода и серы
Характеристика кислорода и серы Reactivi444
Reactivi444 Процессы в растворах: электролитическая диссоциация (ЭД)
Процессы в растворах: электролитическая диссоциация (ЭД) (Bu4N)2[Mo6I8(OOCCH3)6]. Синтез
(Bu4N)2[Mo6I8(OOCCH3)6]. Синтез Общая характеристика элементов главной подгруппы VI группы (подгруппы кислорода)
Общая характеристика элементов главной подгруппы VI группы (подгруппы кислорода) Классификация органических соединений. Предельные углеводороды (УВ)
Классификация органических соединений. Предельные углеводороды (УВ) Расчеты по химическим уравнениям
Расчеты по химическим уравнениям Закон сохранения массы веществ
Закон сохранения массы веществ Молярная масса вещества
Молярная масса вещества Свойства кислорода. Оксиды
Свойства кислорода. Оксиды