Слайд 2Химическая связь
– это вид взаимодействия, при котором происходит перераспределение электронов между атомами.

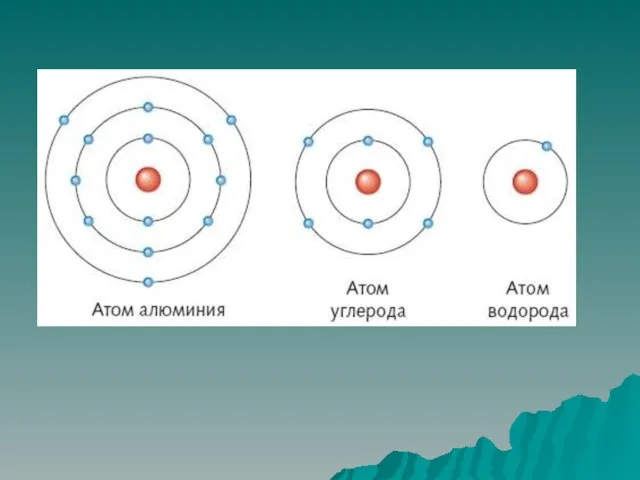
Слайд 5Если число электронов на внешнем уровне атома максимальное, то такой уровень называется

завершенным.
такие атомы не вступают в химической взаимодействие при обычных условиях. Это благородные элементы – 8 главная подгруппа.
Внешний уровень других атомов незавершенным. Они стремятся довести его до 8-электронного.
Электроны внешнего энергетического уровня являются валентными
При взаимодействии этих электронов образуется химическая связь.
В молекуле электроны становятся общими.
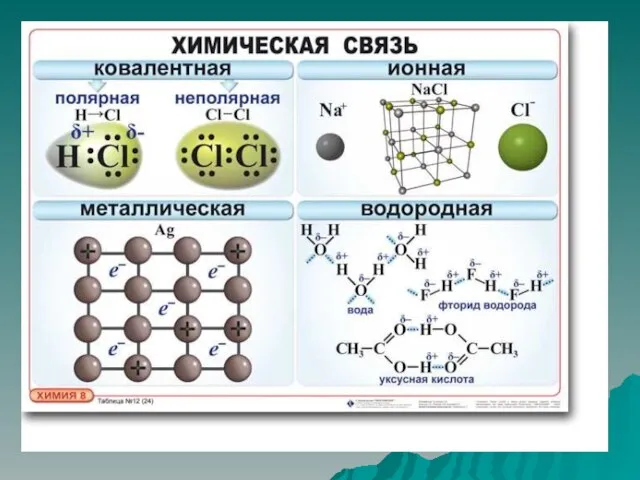
Слайд 6Ковалентная связь
Ковалентная связь – это тип химической связи между двумя атомами, возникающий

при обобществлении электронов, которые принадлежат этим атомам
Образуются общие электронные пары.
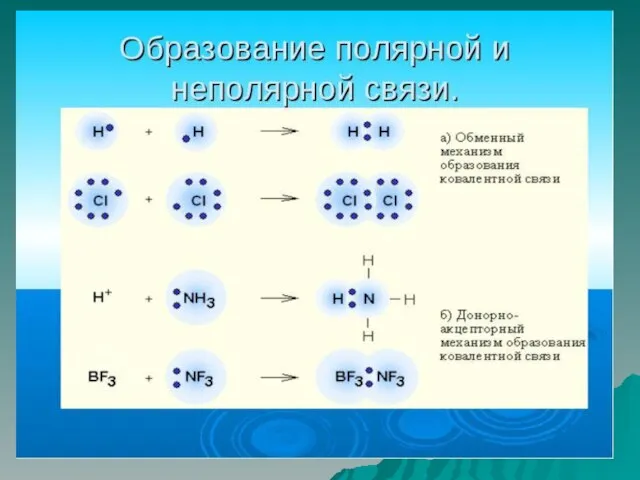
Слайд 8Метод валентных схем
Ковалентная вязь образуется между двумя атомами за счет перекрывания одноэлектронных

валентных облаков (обменный механизм) или перекрывания двухэлектронных валентных облаков и вакантных облаков (донорно-акцепторный механизм)
Слайд 11Характеристики ковалентной связи
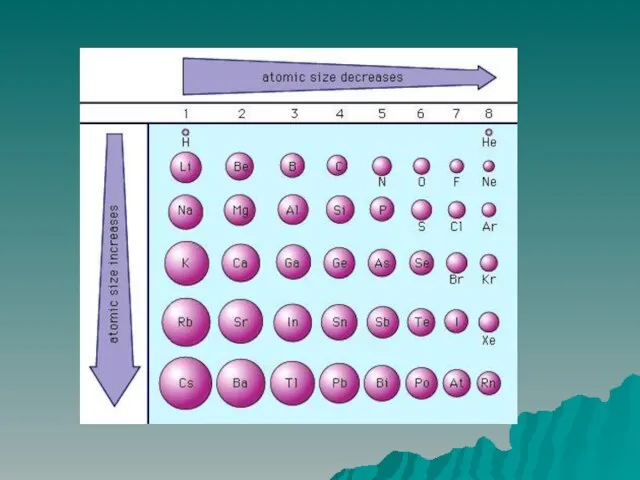
Энергия связи – эта та энергия, которую необходимо затратить для

разрыва данной связи. Измеряется в кДж/моль
Зависит от радиуса перекрывающихся облаков.
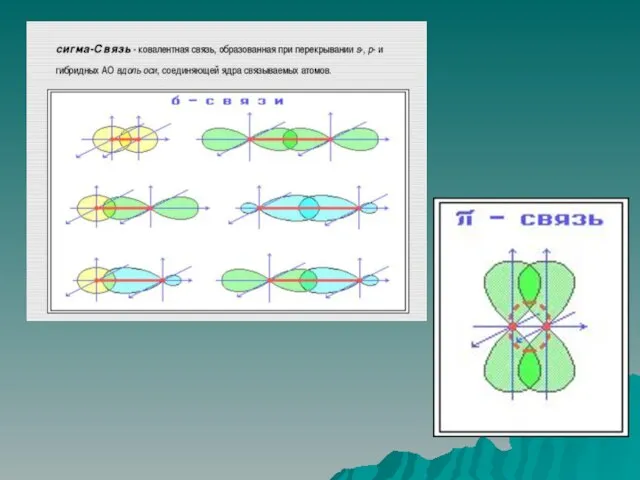
Слайд 14Способ перекрывания электронных облаков
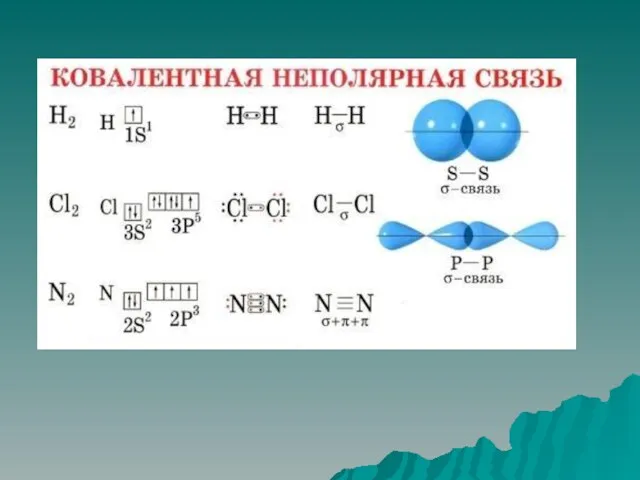
σ - связь образуется при перекрывании вдоль линии, соединяющей

центры атомов. Более прочная.
π – связь образуется при боковом перекрывании в двух областях пространства. Между р-орбиталями
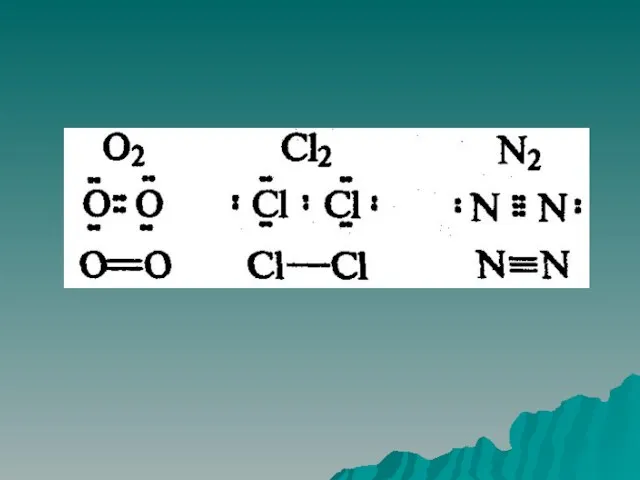
Слайд 16Кратность связи – число химических связей между двумя атомами
Ее можно показать сплошной

линией между атомами либо – точками –
Чем больше кратность связи, тем прочнее связь
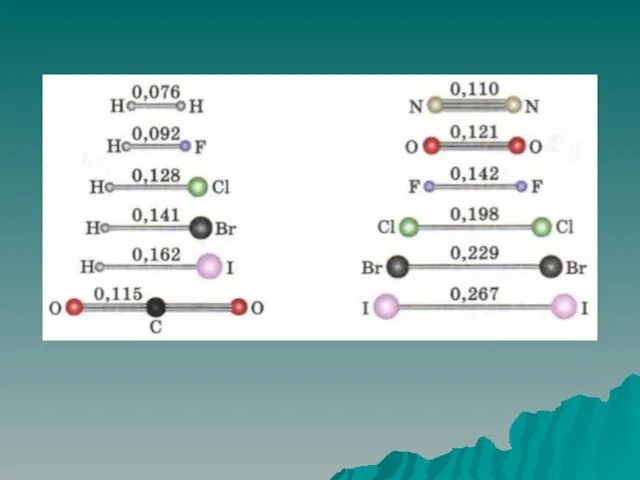
Слайд 18Длина связи – расстояние между ядрами атомов в молекуле.
зависит:
радиусов атома НF, HCl,

HBr, HJ
от кратности связи
Чем больше кратность связи и меньше радиус атомов, тем сильнее химическая связь, ее энергия.
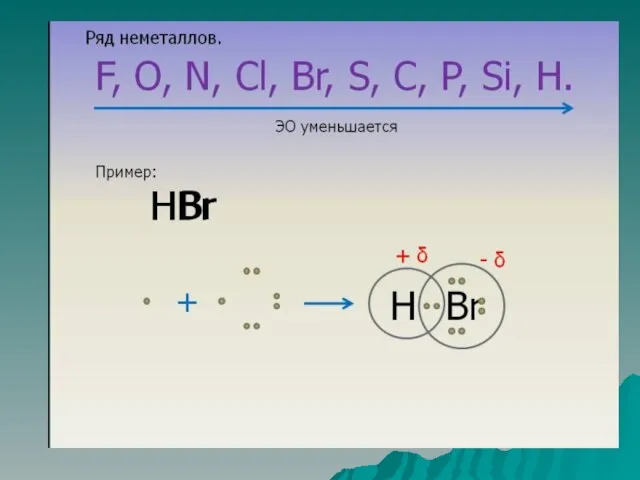
Слайд 20Полярность связи – смещение общей электронной плотность к более электроотрицательному атому.
В зависимости

от этого ковалентная связь делится на полярную и неполярную.
Слайд 23Неполярная ковалентная связь –электронная плотность между атомами распределяется равномерно. К ней относятся

двухатомные молекулы, состоящие из одного элемента: кислород, азот, хлор и т.д.
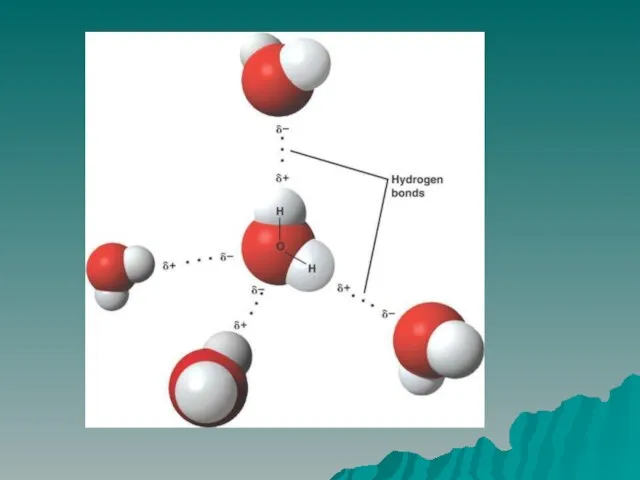
Полярная ковалентная связь – электронное облако смещено к более электроотрицательному атому. Газы: HCl, H2O, NH3 и т.д.
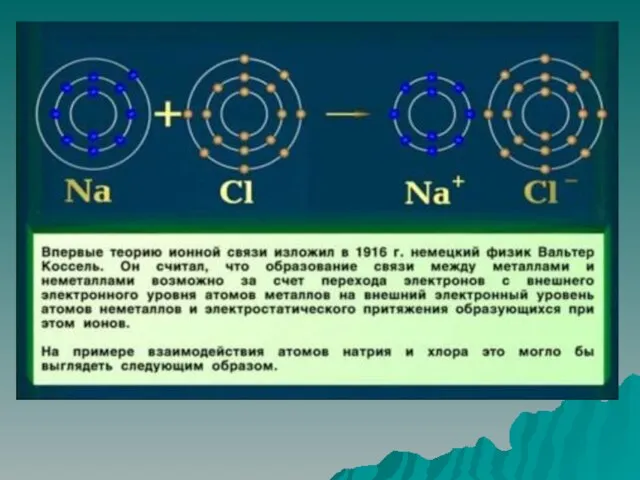
Слайд 25Степень окисления – это условный заряд, который приобретает элемент, исходя из того,

что связь чисто ионная
У элементов 1-3 группы в соединениях всегда положительная степень окисления.
У элементов 4-7 группы максимальная положительная степень окисления равна номеру группы, а промежуточные через единицу от максимальной.
Чем выше в группе находится элемент, тем характернее для него максимальная положительная степень окисления
У элементов 4-7 группы максимальная отрицательная степень окисления равна разности (8 - номеру группы), а промежуточные через единицу от максимальной.
S -2, 0, +2, +4, +6















 Полимеры. Виды полимеров
Полимеры. Виды полимеров Альдегиды
Альдегиды 10_KISLOTNO_OSNOVNOE_TITROVANIE
10_KISLOTNO_OSNOVNOE_TITROVANIE Виды изомерии. Углеводороды
Виды изомерии. Углеводороды Синтетические органические соединения
Синтетические органические соединения Природный источник нефть
Природный источник нефть Материаловедение. Технология конструкционных материалов. Диаграмма состояния Fe-Fe3C
Материаловедение. Технология конструкционных материалов. Диаграмма состояния Fe-Fe3C Реакция полимеризации
Реакция полимеризации Презентация на тему Кремний
Презентация на тему Кремний  Солевые кристаллы
Солевые кристаллы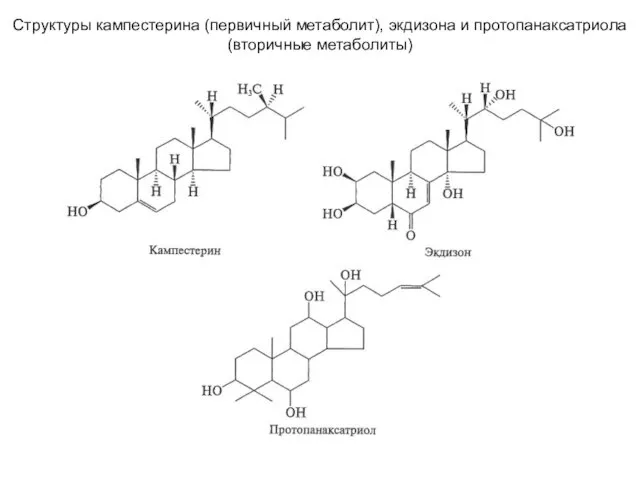 Структуры кампестерина (первичный метаболит), экдизона и протопанаксатриола (вторичные метаболиты)
Структуры кампестерина (первичный метаболит), экдизона и протопанаксатриола (вторичные метаболиты) Процессы переработки нефти
Процессы переработки нефти Ацетилен
Ацетилен Адсорбция твёрдыми адсорбентами
Адсорбция твёрдыми адсорбентами Коррозия металлов
Коррозия металлов Адсорбция на границе раствор-газ. ПАВ и ПНАВ
Адсорбция на границе раствор-газ. ПАВ и ПНАВ Проект в сфере экологического волонтерства преподавателя химии первой квалификационной категории
Проект в сфере экологического волонтерства преподавателя химии первой квалификационной категории Явление хемилюменисценции
Явление хемилюменисценции Типы химических реакций
Типы химических реакций Стирол - важнейшее производное бензола
Стирол - важнейшее производное бензола Презентация на тему Азотная кислота и её соли
Презентация на тему Азотная кислота и её соли  Самородные элементы. Сера. Лекция 7
Самородные элементы. Сера. Лекция 7 Изотопная геохимия. Лекция 4-5
Изотопная геохимия. Лекция 4-5 Хімія у вирішенні промислової проблеми
Хімія у вирішенні промислової проблеми Растворение. Экспериментальная работа с веществами
Растворение. Экспериментальная работа с веществами Кислородсодержащие органические соединения. Многоатомные спирты
Кислородсодержащие органические соединения. Многоатомные спирты Получение функциональных плёнок на основе TiO2
Получение функциональных плёнок на основе TiO2 Нуклеиновые кислоты
Нуклеиновые кислоты