Содержание
- 2. 3. В каких агрегатных состояниях при н. у. встречаются оксиды? Вопросы 2. Что такое оксиды? 4.
- 3. Назовите под №1 оксиды металлов под №2 оксиды неметаллов . Na2O, H2O, CaCl2, NO, BaO, NaOH,
- 4. Тема урока ОСНОВАНИЯ
- 5. Оксидам металла соответствуют основания: Составьте основания из оксидов: ZnO, Li2O, MgO. Попробуйте самостоятельно составить оксиды из
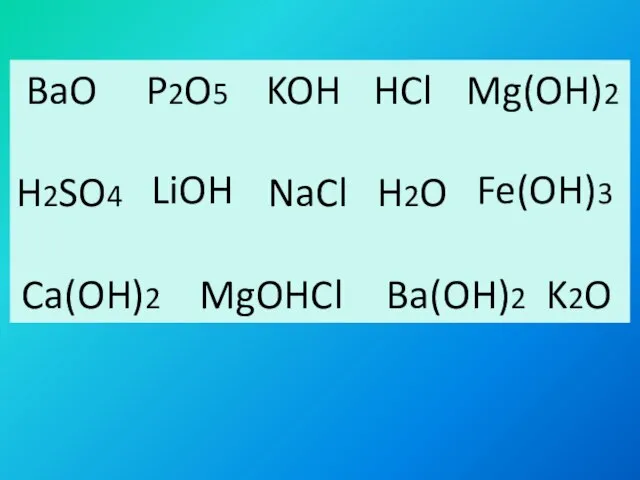
- 6. BaO P2O5 HCl H2SO4 NaCl H2O MgOHCl K2O KOH Mg(OH)2 LiOH Fe(OH)3 Ca(OH)2 Ba(OH)2
- 7. Номенклатура: Ca(OH)2 – гидроксид кальция Fe(OH)2 – гидроксид железа (II) Fe(OH)3 – гидроксид железа (III) =
- 8. Основания – это сложные вещества, состоящие из ионов металлов и связанных с ними одного или нескольких
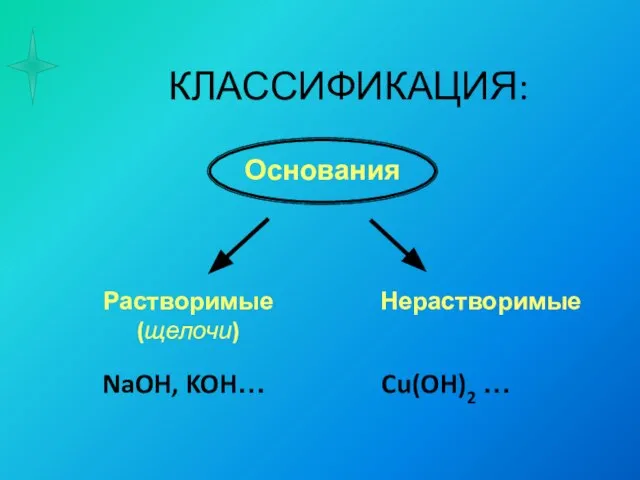
- 9. КЛАССИФИКАЦИЯ: NaOH, KOH… Cu(OH)2 …
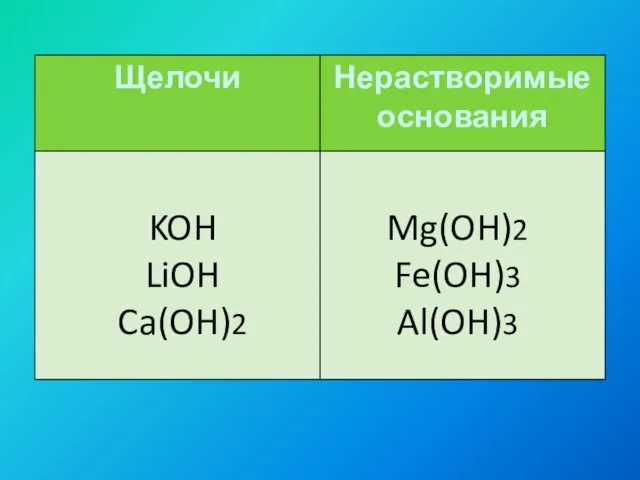
- 10. KOH LiOH Ca(OH)2 Mg(OH)2 Fe(OH)3 Al(OH)3
- 11. Физические свойства оснований Ba(OH)2 Co(OH)2 NaOH Ca(OH)2 LiOH Cu(OH)2
- 12. Получение оснований Активный металл + вода = = щелочь + водород 2Na + 2H2O = 2NaOH
- 13. Химические свойства оснований Взаимодействие с кислотами: NaOH + HCl = NaCl +H2O 2. Взаимодействие щелочей с
- 14. Закрепление 1. Что такое основание? 2. Какими по растворимости бывают основания? 3. Каким оксидам соответствуют основания?
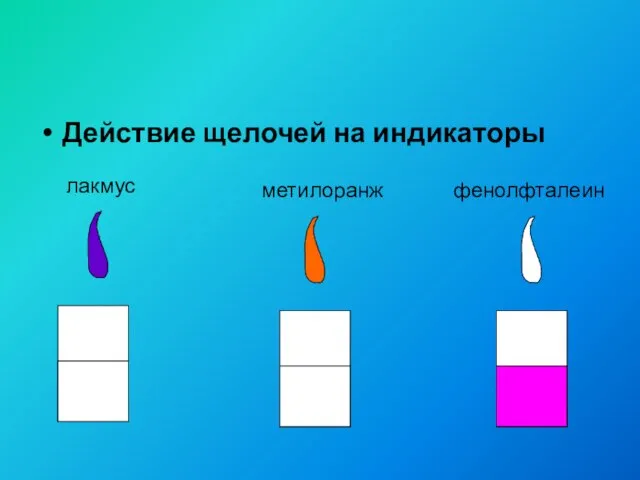
- 15. Действие щелочей на индикаторы лакмус метилоранж фенолфталеин
- 16. Выберите смайлик, который выражает ваше настроение (грустное, весёлое, без эмоций) 1 2 3
- 17. Домашнее задание §31 упр.1- 4 стр.99
- 19. Скачать презентацию












 h-m-chniy-zv-yazok-budova-rechovin
h-m-chniy-zv-yazok-budova-rechovin Органическая химия. Классификация. Номенклатура
Органическая химия. Классификация. Номенклатура Органика в ЕГЭ (В,С)
Органика в ЕГЭ (В,С) Контроль знаний на уроках химии
Контроль знаний на уроках химии Неорганические и органические кислоты
Неорганические и органические кислоты Водород. Доклад по химии
Водород. Доклад по химии Природные источники углеводородов
Природные источники углеводородов Презентация на тему Выбирай вопрос и отвечай
Презентация на тему Выбирай вопрос и отвечай  Углеводороды в природе
Углеводороды в природе Ксилит. Получение
Ксилит. Получение Нефть и способы её переработки
Нефть и способы её переработки Фосфорная кислота и ее свойства
Фосфорная кислота и ее свойства Физическая химия тугоплавких неметаллических и силикатных материалов (ТНСМ)
Физическая химия тугоплавких неметаллических и силикатных материалов (ТНСМ) Дека́н (н-декан) — органическое соединение класса алканов
Дека́н (н-декан) — органическое соединение класса алканов Производство серной кислоты контактным способом
Производство серной кислоты контактным способом Основания как электролиты
Основания как электролиты Гидрокрекинг нефтяного сырья
Гидрокрекинг нефтяного сырья Классификация_органических_соединений[1]
Классификация_органических_соединений[1] Алкадиены. Каучук
Алкадиены. Каучук Презентация на тему Применение этанола и влияние его на человека
Презентация на тему Применение этанола и влияние его на человека  Тривиальные названия веществ, наиболее часто встречаемых в ЕГЭ
Тривиальные названия веществ, наиболее часто встречаемых в ЕГЭ Сухой спирт
Сухой спирт Ocena zawartości mikotoksyn w wybranych produktach spożywczych
Ocena zawartości mikotoksyn w wybranych produktach spożywczych Амины
Амины Общие свойства металлов
Общие свойства металлов Сода. Что я знаю о ней!?
Сода. Что я знаю о ней!? Презентация - Крахмал - подготовительная группа
Презентация - Крахмал - подготовительная группа Презентация на тему Полимеры
Презентация на тему Полимеры