Содержание
- 2. Материаловедение и технология конструкционных материалов 16 лекций (32 час) 8 практических занятий (16 час) 4 лабораторные
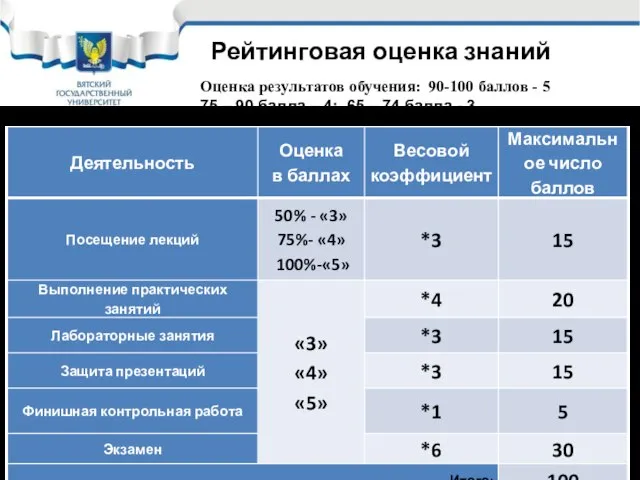
- 3. Рейтинговая оценка знаний Оценка результатов обучения: 90-100 баллов - 5 75 – 90 балла – 4;
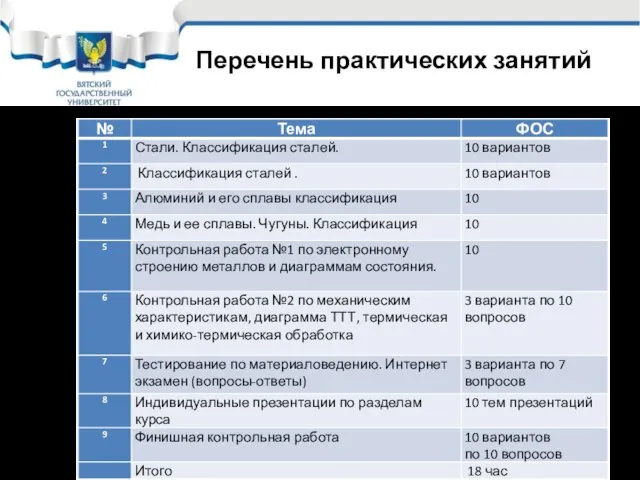
- 4. Перечень практических занятий
- 5. Литература Основная литература Солнцев Ю.П., Пряхин Е.И. Материаловедение. Учебник для вузов. – С.П.: Химиздат, 2004, 735
- 6. Модуль 1. Основы строения и свойства материалов. Слайд 1.01 Конструкционные материалы в истории человечества.
- 7. На сегодняшний день широко применяются следующие основные виды конструкционных материалов: Металлы и сплавы; Полимерные материалы (пластмассы,
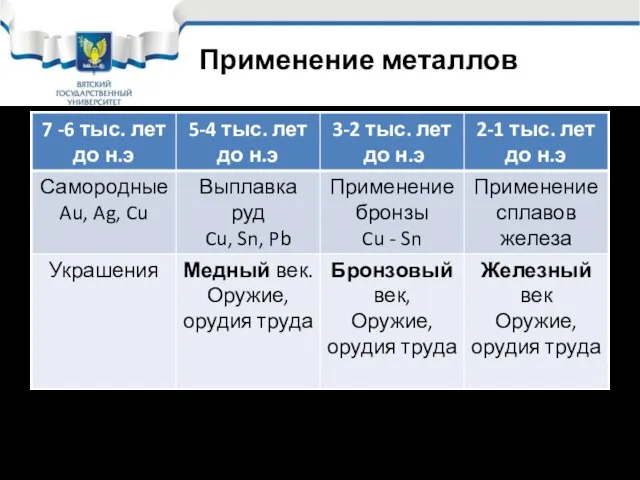
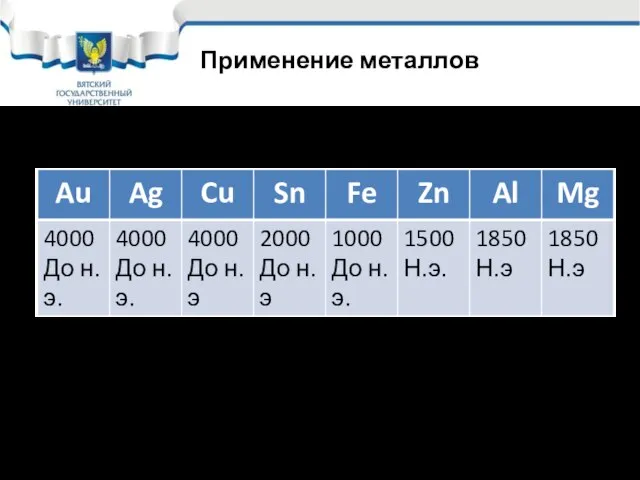
- 8. Применение металлов
- 9. Применение металлов Европа
- 10. Применение железа Вначале метеоритное железо Затем получение в ямах Получение в печах
- 11. Из всех известных видов конструкционных материалов металлы продолжают оставаться самыми распространёнными и по сей день. Черные
- 12. Металлы как вид конструкционных материалов имеют следующие общие свойства: Высокая прочность; Высокие тепло- и электропроводность; Высокая
- 13. Атомно-кристаллическое строение металлов Все металлы за исключением ртути при обычных условиях находятся в твердом состоянии, т.е.
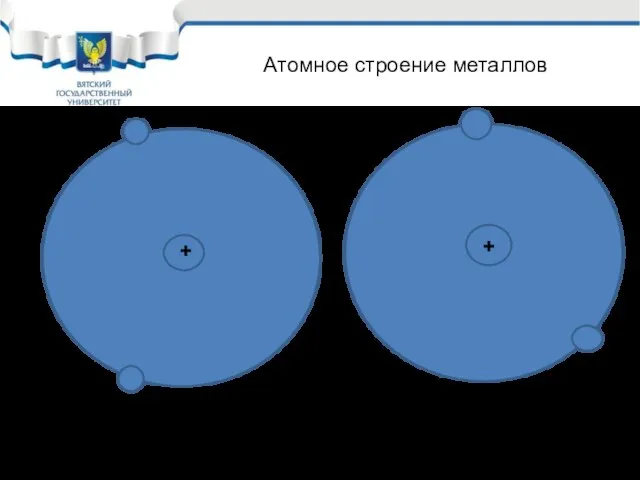
- 14. + + На большом расстоянии друг от друга атомы металла не взаимодействуют друг с другом Атомное
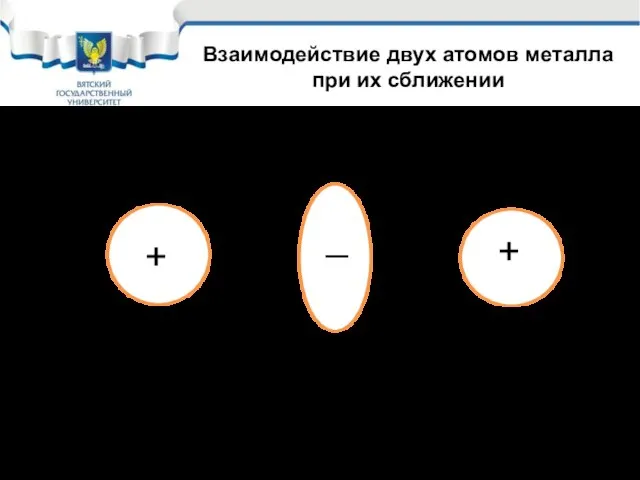
- 15. + Взаимодействие двух атомов металла при их сближении + _ При сближении атомов металлов начинается взаимодействие:
- 16. Однако, при слишком близком сближении атомов металла начинают резко нарастать сила отталкивания между положительно заряженными ядрами
- 17. r 1 2 3 r0 F 1 - изменение сил притяжения между атомами металла; 2 -
- 18. Решетка в твердом кристаллическом металле Таким образом в твердом металле все атомы располагаются на наиболее удобном
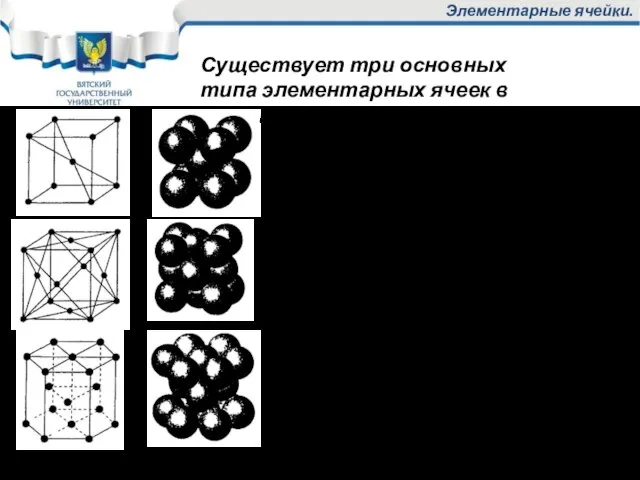
- 19. Элементарные ячейки. ОЦК – объёмноцентрированная кубическая nат=2 К=8 Кзап=68% ГЦК – гранецентрированная кубическая nат=4 К=12 Кзап=74%
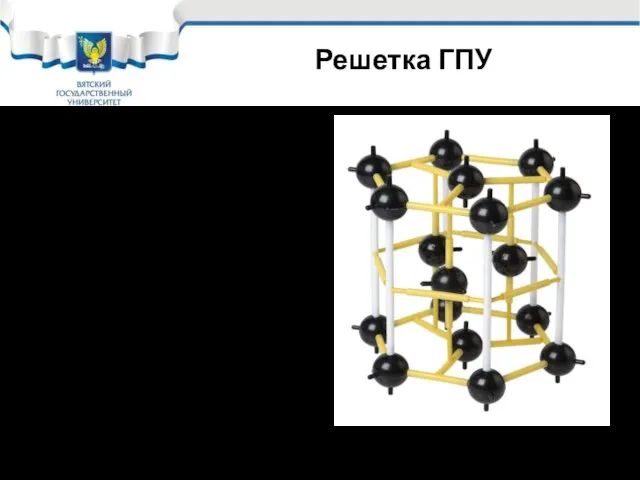
- 20. Решетка ГПУ Еще одно изображение Гексагональной плотно- упакованной решетки (ГПУ)
- 21. Характеристики элементарных ячеек Расстояние между центрами атомов (зависит от диаметра атомов); ОЦК, и ГЦК - один
- 22. Характеристики элементарных ячеек 5. Количество и размер пор. В любой решетке есть два вида пор: тетраэдрические
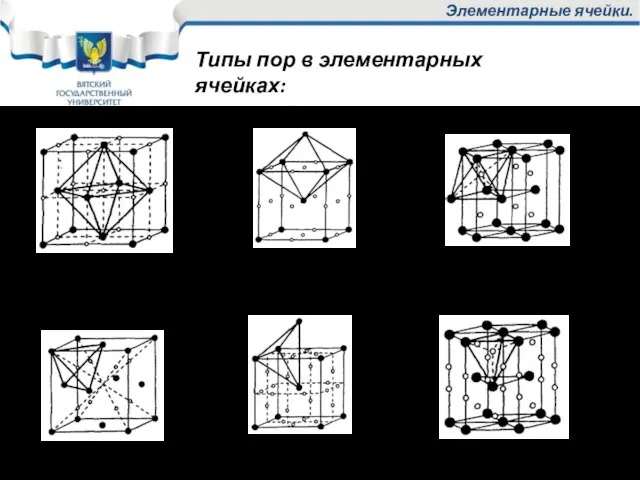
- 23. Элементарные ячейки. Типы пор в элементарных ячейках: Октаэдрические: Тетраэдрические: ГЦК ОЦК ГПУ ГЦК ОЦК ГПУ
- 24. Металлическая связь и свойства металлов Связь между атомами металла в кристаллографической решетке называется металлической связью. Металлическая
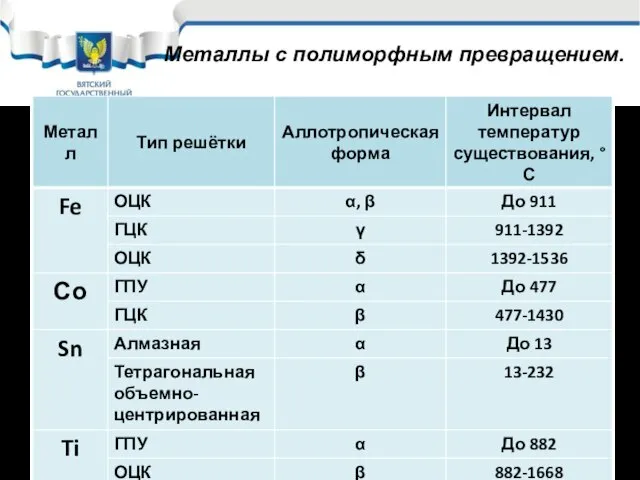
- 25. Некоторые металлы при разных температурах могут иметь различную кристаллическую решётку. Способность металла существовать в различных кристаллических
- 26. Металлы с полиморфным превращением.
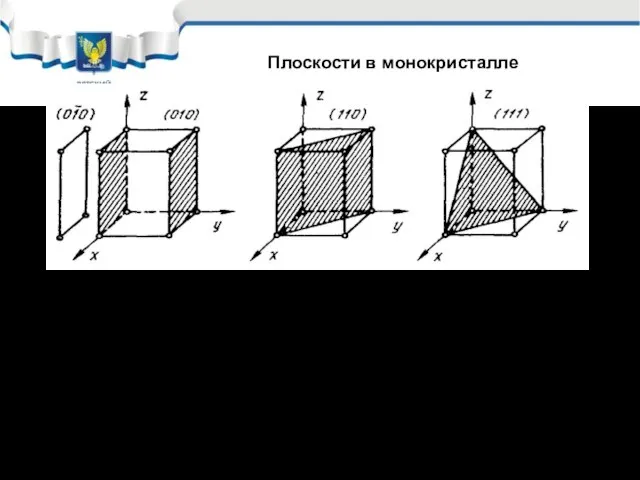
- 27. Плоскости в монокристалле Решетка идеального металла может быть разрезана по разным плоскостям. В этом случае сразу
- 28. Плоскости в идеальном металле Поэтому возникает задача указать по какой плоскости разрезан монокристалл, т.е. присвоить плоскости
- 29. В кристаллографии положение атомных плоскостей в кристалле определяется отрезками, отсекаемыми этими плоскостями при их пересечении с
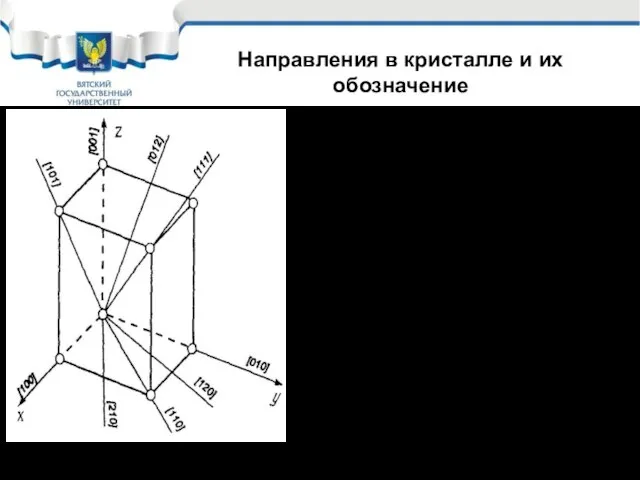
- 30. Если в кристалле металла рассмотреть разные направления, то увидим, что плотность расположения в них атомов неодинакова,
- 32. Скачать презентацию

















 Метаболизм чужеродных соединений
Метаболизм чужеродных соединений Генетическая связь между классами неорганических веществ
Генетическая связь между классами неорганических веществ Структура материалов
Структура материалов Обобщить и систематизировать знания учащихся о кислотах неорганических и органических, о их составе и свойствах
Обобщить и систематизировать знания учащихся о кислотах неорганических и органических, о их составе и свойствах Электролитическая диссоциация. 8 класс
Электролитическая диссоциация. 8 класс Углеводы. Несахароподобные полисахариды
Углеводы. Несахароподобные полисахариды Изомерия органических соединений. Лекция 2
Изомерия органических соединений. Лекция 2 Способы получения металлов
Способы получения металлов 热塑性复合材料的分类及特性
热塑性复合材料的分类及特性 Закон постоянства состава веществ. Химические формулы. (8 класс)
Закон постоянства состава веществ. Химические формулы. (8 класс) Основания. Состав оснований
Основания. Состав оснований Концепция химической связи
Концепция химической связи Алкены. Тестирование
Алкены. Тестирование Хлор. Химические свойства и применение. Лекция 5
Хлор. Химические свойства и применение. Лекция 5 Элемент первой группы, калий
Элемент первой группы, калий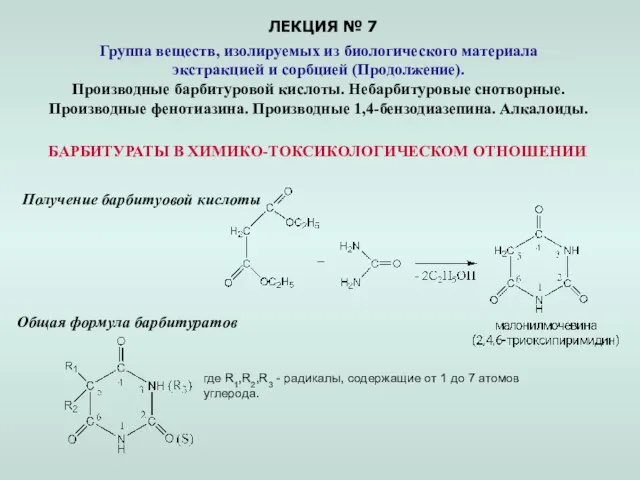 Презентация по Химии "Группа веществ, изолируемых из биологического материала экстракцией и сорбцией"
Презентация по Химии "Группа веществ, изолируемых из биологического материала экстракцией и сорбцией"  Предмет биоорганической химии. Лекция 1
Предмет биоорганической химии. Лекция 1 Растворы полимеров
Растворы полимеров Фенол
Фенол Мицелла. Строение мицеллы
Мицелла. Строение мицеллы Химия – это область чудес
Химия – это область чудес Бишофит - новый старый антигололедный реагент
Бишофит - новый старый антигололедный реагент Электролиз расплавов и растворов солей
Электролиз расплавов и растворов солей Соли. Свойства. Получение
Соли. Свойства. Получение Презентацию выполнила ученица 10 класса Поликарпова Диана 2010 год
Презентацию выполнила ученица 10 класса Поликарпова Диана 2010 год Фосфорорганические соединения
Фосфорорганические соединения Презентация на тему Неорганічні речовини живих організмів
Презентация на тему Неорганічні речовини живих організмів  ZnS и ZnSe как оптические материалы,люминофоры, лазерные матрицы
ZnS и ZnSe как оптические материалы,люминофоры, лазерные матрицы