Содержание
- 2. Цели и задачи урока: Дать определение данному типу реакций Показать алгоритм записи о-в реакции Дать понятия
- 3. Содержание Роль ОВР в современном мире Основные понятия Расчет степени окисления Творческое задание Домашнее задание Сочиняют
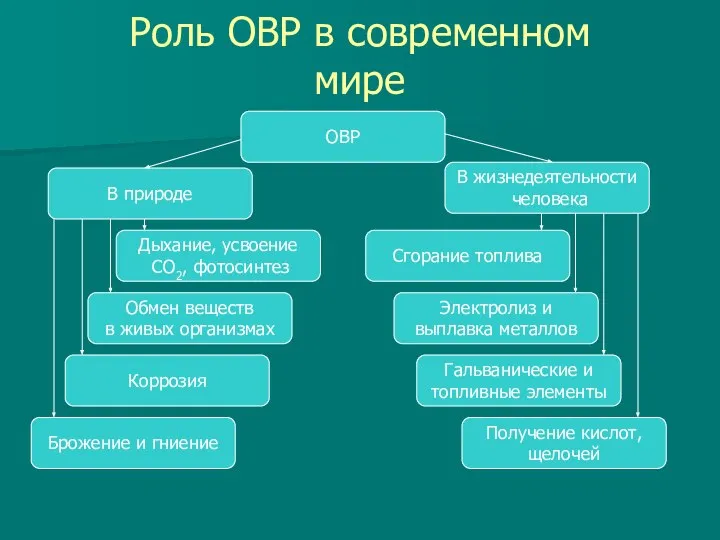
- 4. Роль ОВР в современном мире В природе ОВР В жизнедеятельности человека Дыхание, усвоение CO2, фотосинтез Сгорание
- 5. Основные понятия окислительно-восстановительная реакция степень окисления окислитель восстановитель процесс окисления-восстановления
- 6. Расчет степени окисления Следует запомнить: 1. Степени окисления атомов в простых веществах равны нулю: Na0; H20
- 7. Расчет степени окисления 1. Для веществ из двух элементов: -поставить постоянную степень окисления CO-2 -рассчитать степень
- 8. Расчет степени окисления 2.Для веществ из трех и более элементов: -поставить постоянные степени окисления H+1MnO4-2 -рассчитать
- 9. Творческое задание: ОВР в технике и жизни Задание для двух команд: Внимательно изучить представленную на слайде
- 10. Творческое задание 1 3 3 4 2 4 5 6 7 8 9 10 11 14
- 11. Домашнее задание 1. §57,59,61 – учебника 8 класса №10.40-10.42 , Хомченко И.Г. «Сборник задач и упражнений
- 12. Сочиняют дети…. Окислитель, как отъявленный злодей, Как пират, бандит, агрессор, Бармалей, Отнимает электроны - и OK!
- 13. Окислительно-восстановительные реакции Реакции, протекающие с изменением степени окисления, называются окислительно-восстановительными реакциями. 0 +2 0 +2 Cu
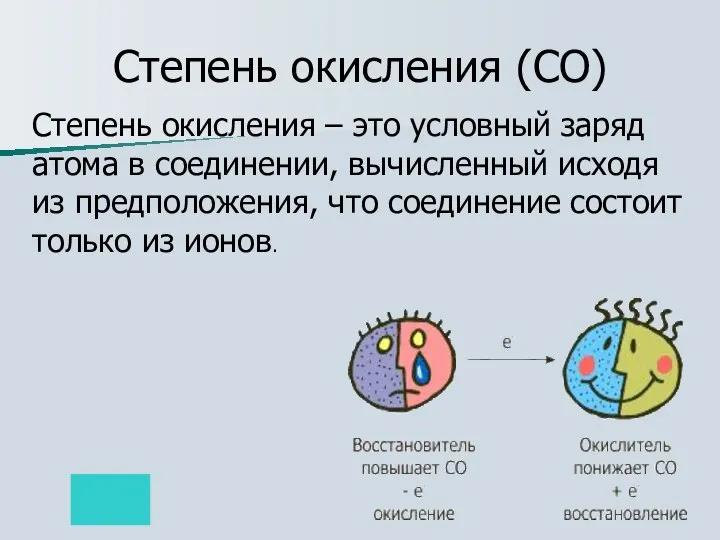
- 14. Степень окисления (СО) Степень окисления – это условный заряд атома в соединении, вычисленный исходя из предположения,
- 15. Окислитель -Частица (атом, ион), которая в ходе окислительно-восстановительного процесса принимает электроны называется окислителем -Простые вещества -
- 16. Типичные окислители К ним относятся многие сложные и простые вещества KClO3, F2, H2SO4 (конц.), Cl2, HNO3,
- 17. Восстановитель Частица (атом, ион), которая в ходе окислительно-восстановительного процесса отдает электроны, называется восстановителем Типичные восстановители
- 18. Типичные восстановители К ним также относятся простые и сложные вещества H2, KI, C (графит), HCl (конц.),
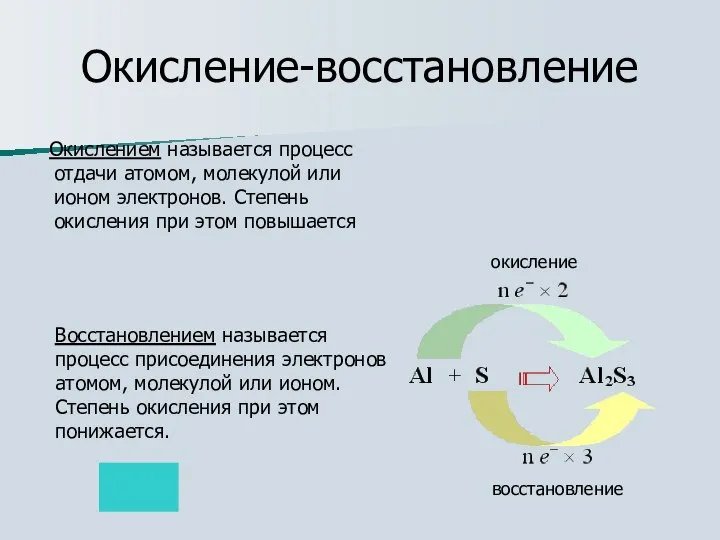
- 19. Окисление-восстановление окисление Окислением называется процесс отдачи атомом, молекулой или ионом электронов. Степень окисления при этом повышается
- 20. Окисление-процесс отдачи электронов 0 +2 Cu – 2 e- = Cu При окислении степень окисления элемента
- 22. Скачать презентацию
















 Презентация на тему Соединения серы
Презентация на тему Соединения серы  Основные законы и понятия химии. Основные классы неорганических соединений. Химический эквивалент. Закон эквивалентов
Основные законы и понятия химии. Основные классы неорганических соединений. Химический эквивалент. Закон эквивалентов Незаменимая уксусная кислота
Незаменимая уксусная кислота Перегонка. Вклад алхимиков в органическую химию
Перегонка. Вклад алхимиков в органическую химию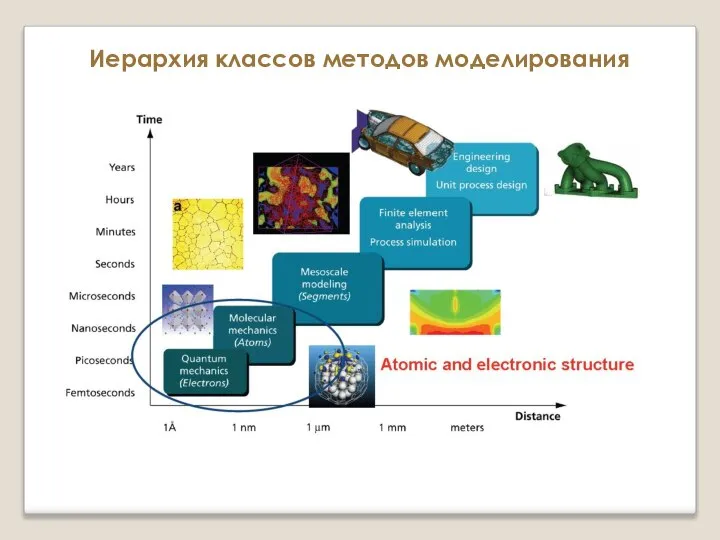 Иерархия классов методов моделирования. Атомистические и микроскопические методы
Иерархия классов методов моделирования. Атомистические и микроскопические методы Магний и кальций
Магний и кальций Сахароза, крахмал, целлюлоза
Сахароза, крахмал, целлюлоза Строение сложного фермента
Строение сложного фермента Хімія у вирішенні промислової проблеми
Хімія у вирішенні промислової проблеми Вещество и тело. Атом и молекула. Свойства веществ. Простые и сложные вещества. Химический элемент
Вещество и тело. Атом и молекула. Свойства веществ. Простые и сложные вещества. Химический элемент Основи молекулярно-кінетичної теорії
Основи молекулярно-кінетичної теорії Углеводороды. Общие знания
Углеводороды. Общие знания Gelation in aqueous solution of L-cysteine and silver nitrate
Gelation in aqueous solution of L-cysteine and silver nitrate Заполни электронные уровни элементов
Заполни электронные уровни элементов Явление аллотропии
Явление аллотропии Исследование структуры продуктов аммонолиза мезопористых магниетермических порошков тантала
Исследование структуры продуктов аммонолиза мезопористых магниетермических порошков тантала Центробежное осаждение
Центробежное осаждение Характеристика кислорода и серы
Характеристика кислорода и серы Актуальные задачи химии
Актуальные задачи химии Металлы - наши друзья или враги
Металлы - наши друзья или враги Получение, свойства и применение алкенов
Получение, свойства и применение алкенов Классификация силикатов
Классификация силикатов Способы получения металлов
Способы получения металлов Фуллерены
Фуллерены 6. Характеристика элементов на основе положения в периодической системе
6. Характеристика элементов на основе положения в периодической системе Природные источники углеводородов
Природные источники углеводородов علاوي الندوة
علاوي الندوة Цезій
Цезій