Содержание
- 2. Кислородсодержащие органические соединения Спирты -одноатомные -многоатомные Альдегиды и кетоны Кислородсодержащие органические соединения Карбоновые кислоты Эфиры -простые
- 3. Задачи 1. Выяснить функциональную группу, общую формулу карбоновых кислот. 2. Сформулировать определение. 3. Изучить классификацию карбоновых
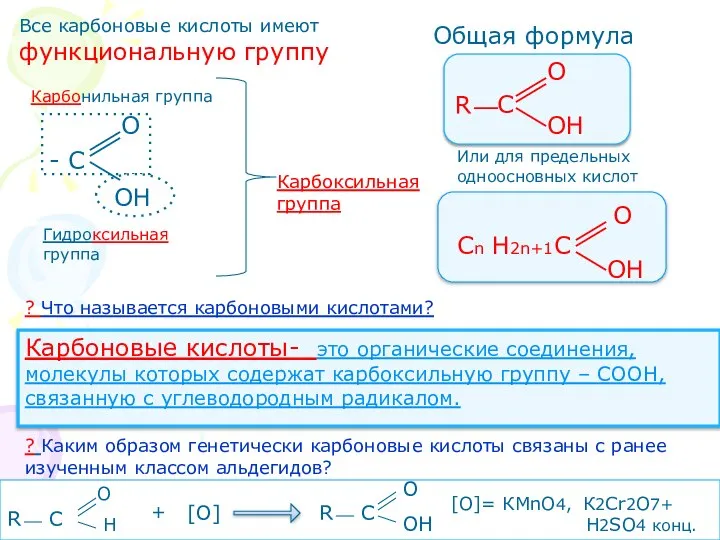
- 4. Все карбоновые кислоты имеют функциональную группу - С ОН О Карбонильная группа Гидроксильная группа Карбоксильная группа
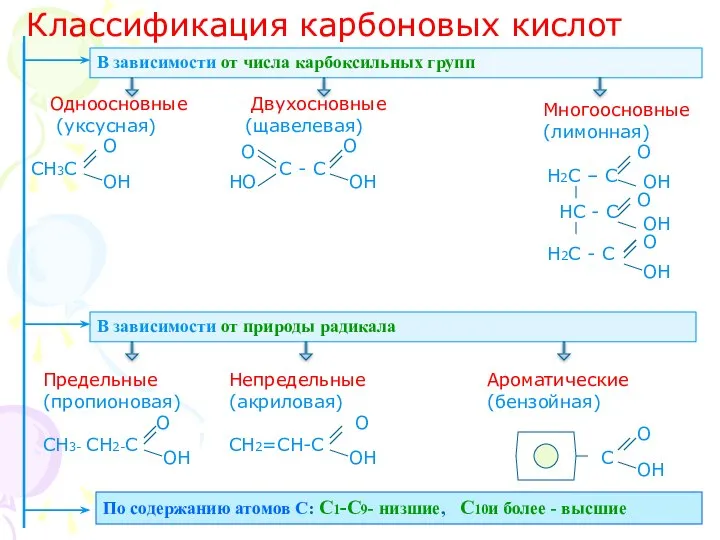
- 5. Классификация карбоновых кислот В зависимости от числа карбоксильных групп Одноосновные Двухосновные (уксусная) (щавелевая) СН3С С -
- 6. Проклассифицируйте предложенные кислоты 1) СH3 – СН2 – СН2 – СН2 - COOH 2) HOOC -
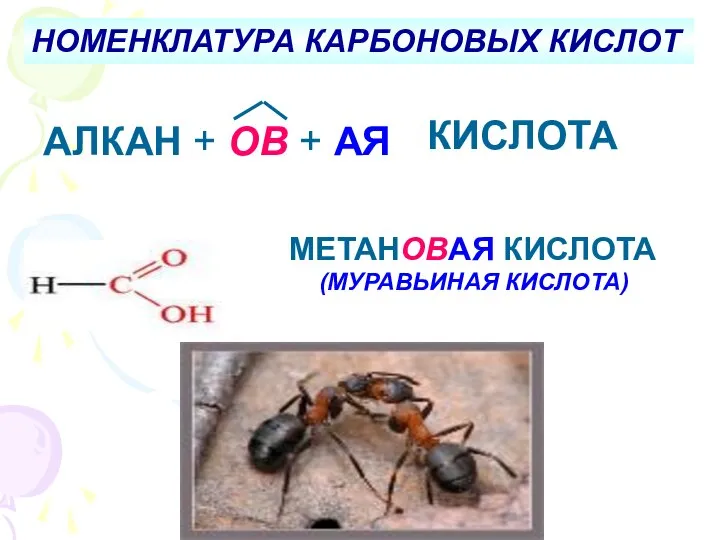
- 7. НОМЕНКЛАТУРА КАРБОНОВЫХ КИСЛОТ АЛКАН + ОВ + АЯ КИСЛОТА МЕТАНОВАЯ КИСЛОТА (МУРАВЬИНАЯ КИСЛОТА)
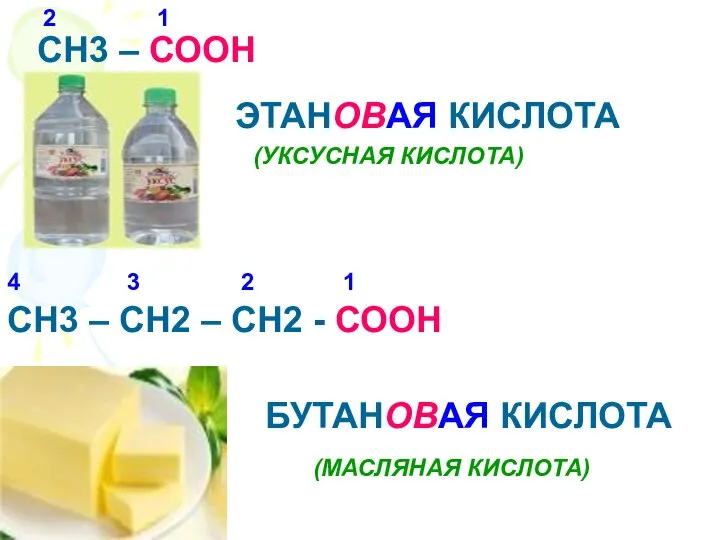
- 8. СН3 – СООН 1 2 ЭТАНОВАЯ КИСЛОТА (УКСУСНАЯ КИСЛОТА) СН3 – СН2 – СН2 - СООН
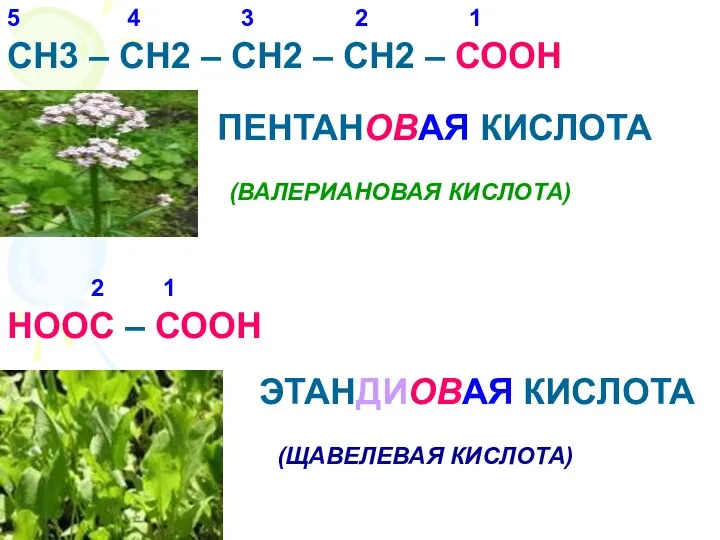
- 9. СН3 – СН2 – СН2 – СН2 – СООН ПЕНТАНОВАЯ КИСЛОТА (ВАЛЕРИАНОВАЯ КИСЛОТА) 1 2 3
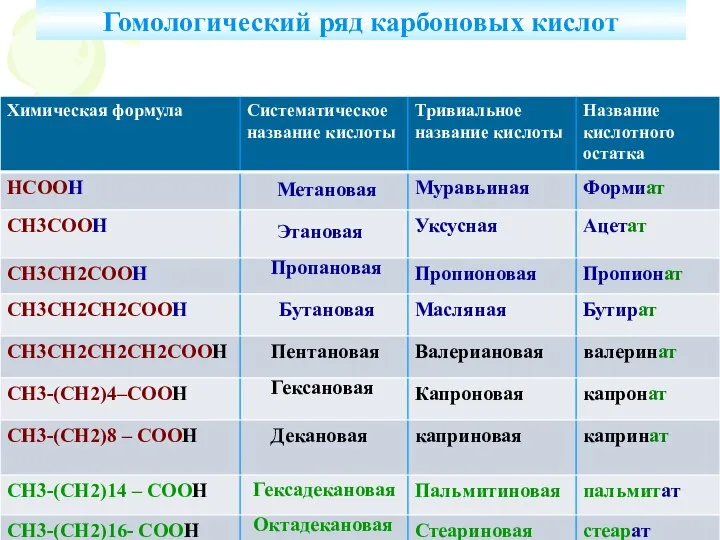
- 10. Гомологический ряд карбоновых кислот Метановая Этановая Пропановая Бутановая Пентановая Гексановая Декановая Гексадекановая Октадекановая
- 11. Алгоритм названия карбоновых кислот: 1. Находим главную цепь атомов углерода и нумеруем её, начиная с карбоксильной
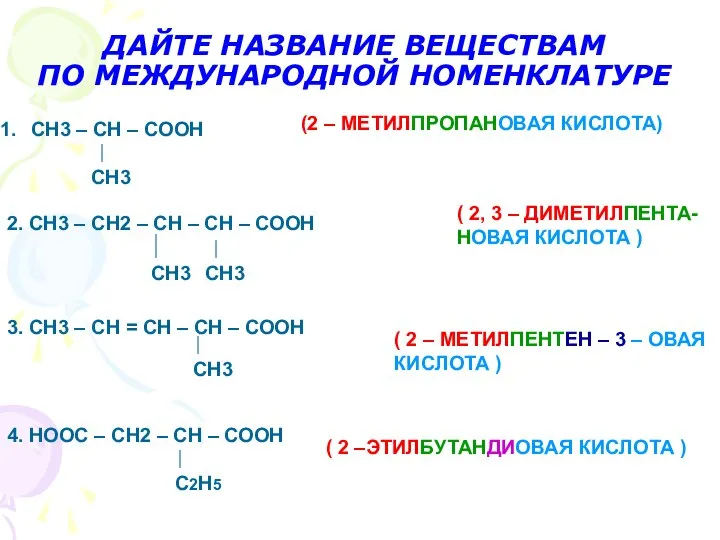
- 12. ДАЙТЕ НАЗВАНИЕ ВЕЩЕСТВАМ ПО МЕЖДУНАРОДНОЙ НОМЕНКЛАТУРЕ (2 – МЕТИЛПРОПАНОВАЯ КИСЛОТА) СН3 – СН – СООН 2.
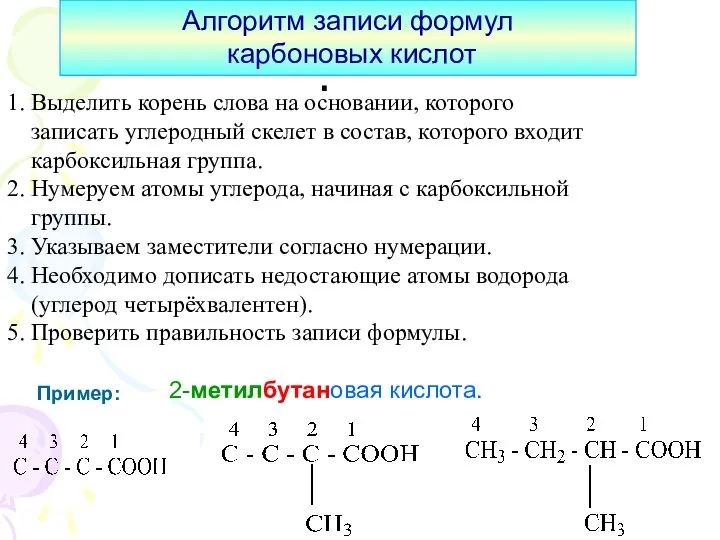
- 13. : 1. Выделить корень слова на основании, которого записать углеродный скелет в состав, которого входит карбоксильная
- 14. ФИЗИЧЕСКИЕ СВОЙСТВА С1 – С3 Жидкости с характерным резким запахом, хорошо растворимые в воде С4 –
- 15. Агрегатное состояние жидкое Цвет бесцветная прозрачная жидкость Запах резкий уксусный Растворимость в воде хорошая Температура кипения
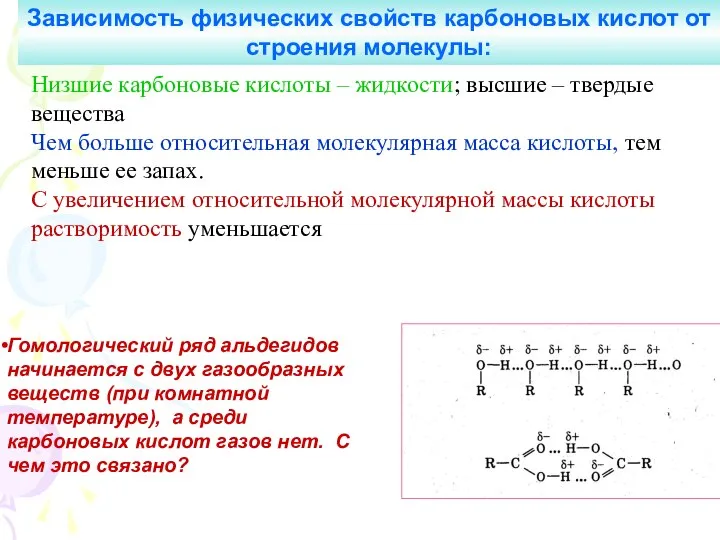
- 16. Низшие карбоновые кислоты – жидкости; высшие – твердые вещества Чем больше относительная молекулярная масса кислоты, тем
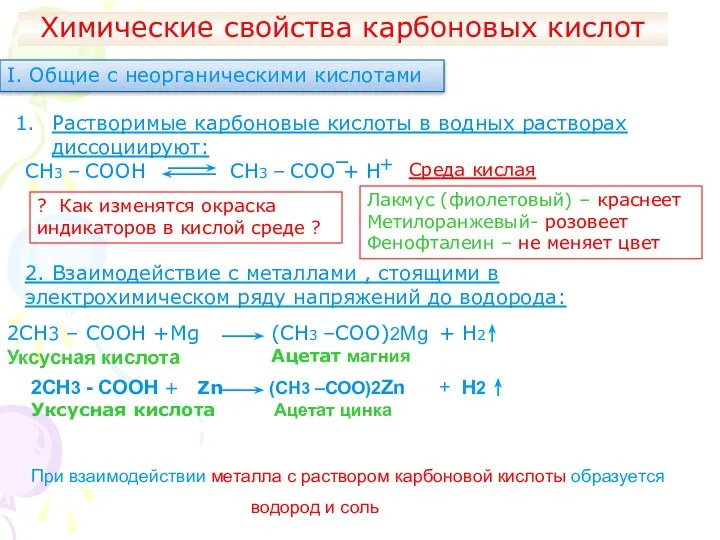
- 17. Химические свойства карбоновых кислот І. Общие с неорганическими кислотами Растворимые карбоновые кислоты в водных растворах диссоциируют:
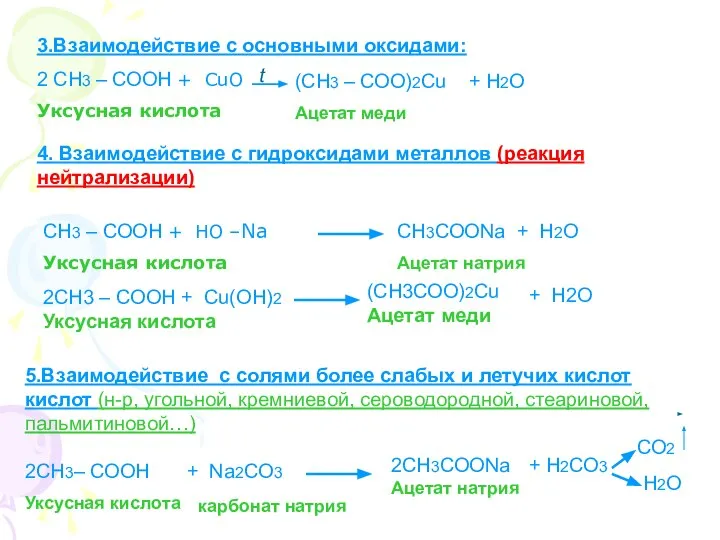
- 18. 3.Взаимодействие с основными оксидами: 2 СН3 – СООН + СuО Уксусная кислота t (СН3 – СОО)2Сu
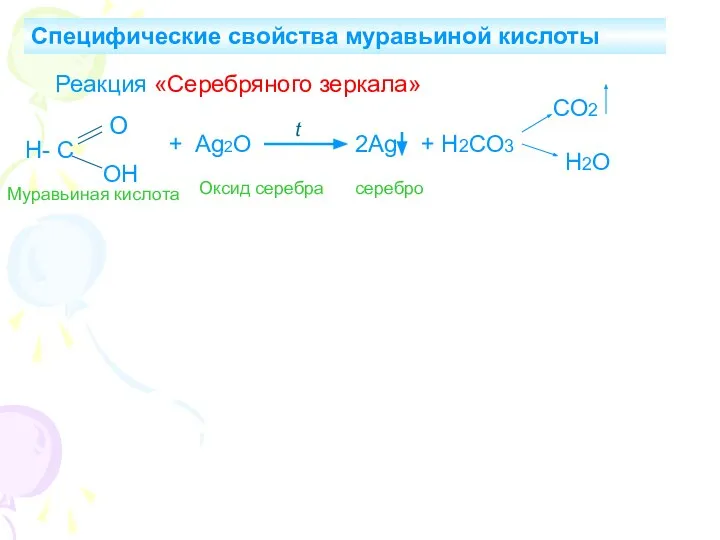
- 19. Специфические свойства муравьиной кислоты Реакция «Серебряного зеркала» Н- С О ОН + Ag2O t 2Ag +
- 20. Нахождение в природе и применение карбоновых кислот Муравьиная кислота(Метановая кислота) -Химическая формула СН2О2, или НСООН. -
- 21. Применение муравьиной кислоты Муравьиная кислота обладает ярко выраженными бактерицидными свойствами. Поэтому ее водные растворы используют как:
- 22. Вопрос: Почему нельзя смачивать водой место муравьиного укуса или ожога крапивой? Это приводит только к усилению
- 23. Уксусная кислота (этановая кислота) Это – первая кислота, полученная и использованная человеком. «Родилась» более 4 тыс.лет
- 24. Применение уксусной кислоты - Водные растворы уксусной кислоты широко используются в пищевой промышленности (пищевая добавка E-
- 25. Применение уксусной кислоты Известно применение спиртового уксуса в косметологии. А именно для придания мягкости и блеска
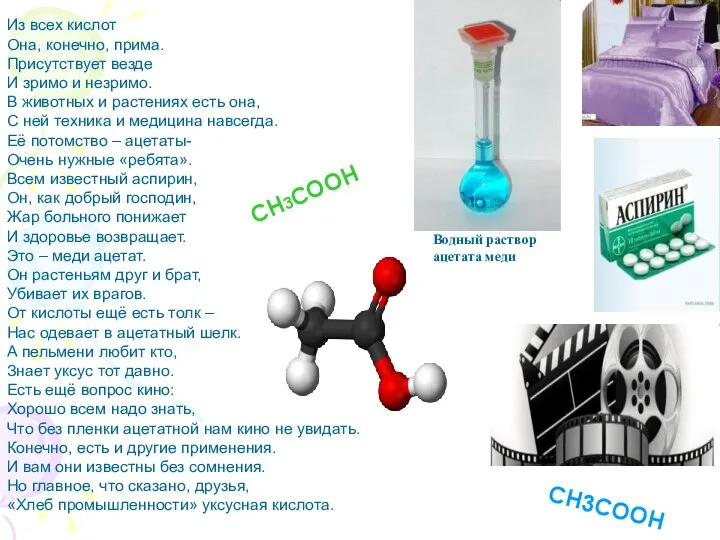
- 26. Из всех кислот Она, конечно, прима. Присутствует везде И зримо и незримо. В животных и растениях
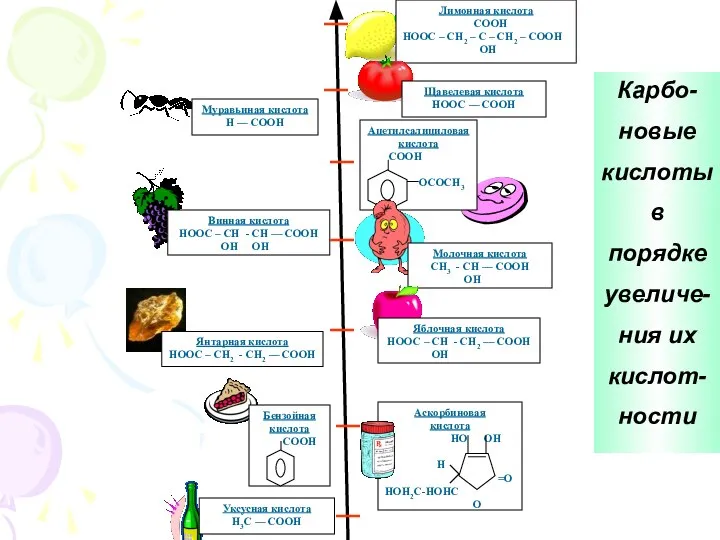
- 27. Карбо- новые кислоты в порядке увеличе- ния их кислот- ности
- 28. Выводы 1.Карбоновые кислоты- это органические соединения, молекулы которых содержат карбоксильную группу – СООН, связанную с углеводородным
- 29. Домашнее задание §12 , упражнения № 5 , 6 стр 91 упр.№9 Царица Клеопатра по совету
- 31. Скачать презентацию













 Отрасли химии
Отрасли химии Жизнь и деятельность А.М. Бутлерова
Жизнь и деятельность А.М. Бутлерова Анализ спорных ситуаций при оценивании заданий с развернутым ответом. Химия
Анализ спорных ситуаций при оценивании заданий с развернутым ответом. Химия Про краски
Про краски Кислоты: состав, классификация, номенклатура, получение
Кислоты: состав, классификация, номенклатура, получение Кроссворд по теме Металлы
Кроссворд по теме Металлы Аналитическая химия (ЛЕКЦИЯ 1)
Аналитическая химия (ЛЕКЦИЯ 1) кристал решетка
кристал решетка Алкены
Алкены Химические вещества парабены
Химические вещества парабены Положение металлов в Периодической системе химических элементов Д.И.Менделеева
Положение металлов в Периодической системе химических элементов Д.И.Менделеева Аэрозоли и аэродисперсии
Аэрозоли и аэродисперсии Характеристика химического элемента по кислотно-основным свойствам образуемых им соединений
Характеристика химического элемента по кислотно-основным свойствам образуемых им соединений Алкины
Алкины Презентация на тему Строение атома и атомного ядра
Презентация на тему Строение атома и атомного ядра  ЛК 2_окислительно-восстановительные процессы
ЛК 2_окислительно-восстановительные процессы Вывод формул веществ по известным массовым долям элементов
Вывод формул веществ по известным массовым долям элементов Характеристика кислорода и серы
Характеристика кислорода и серы Жаңа синтетикалық есірткілер
Жаңа синтетикалық есірткілер Обмен и функции нуклеотидов
Обмен и функции нуклеотидов Презентация на тему Альдегиды и Кетоны
Презентация на тему Альдегиды и Кетоны  Карбонильные Соединения. Альдегиды и кетоны
Карбонильные Соединения. Альдегиды и кетоны Типы химических реакций. Решение примеров
Типы химических реакций. Решение примеров Основания. Физические и химические свойства оснований
Основания. Физические и химические свойства оснований Алканы, предельные, насыщенные углеводороды (парафины)
Алканы, предельные, насыщенные углеводороды (парафины) Общие способы получения металлов
Общие способы получения металлов Состав популярных напитков, рН-группа
Состав популярных напитков, рН-группа Минералы
Минералы