Содержание
- 2. Уровни сложности задания: Б – базовый - 68% П – повышенный - 18% В – высокий
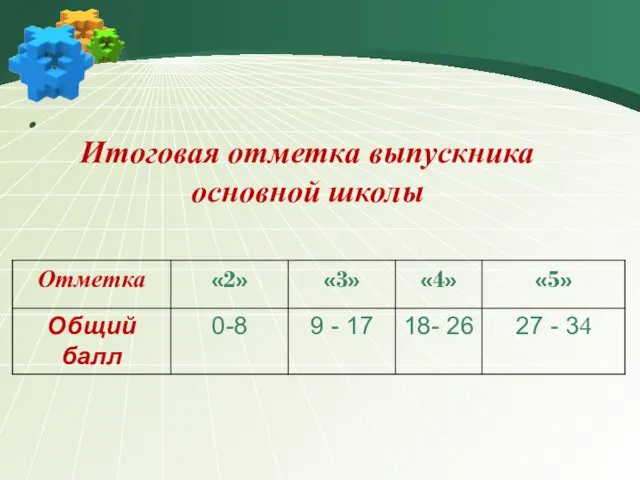
- 3. . Итоговая отметка выпускника основной школы
- 4. СТРУКТУРА ГИА
- 5. СОДЕРЖАТЕЛЬНЫЕ БЛОКИ (ТЕМЫ, РАЗДЕЛЫ)
- 6. Время проведения экзамена 120 минут (2 часа). Разрешенные материалы периодическая система химических элементов Д.И. Менделеева таблица
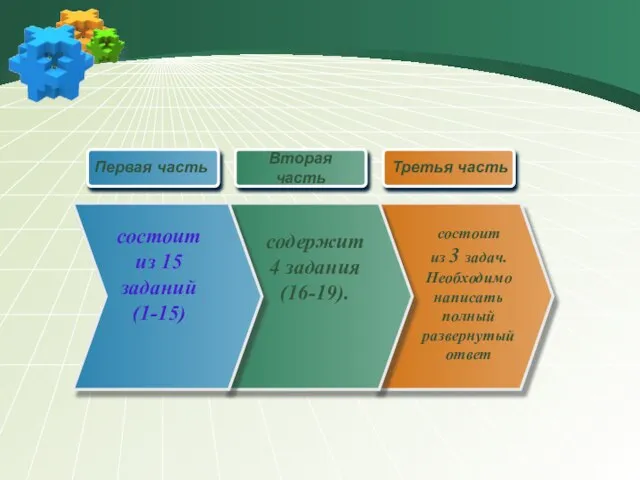
- 7. состоит из 15 заданий (1-15) Первая часть содержит 4 задания (16-19). состоит из 3 задач. Необходимо
- 8. Основные классы неорганических соединений 1 6 7 8 9 10 11 12 13 14 15 2
- 9. 1 Общее число электронов в атоме бериллия равно 1) 6 2) 4 3) 3 4) 5
- 10. 2 B pяду N – P – As - Sb 1) увеличивается число энергетических уровней в
- 11. 3 В соединении натрия с серой химическая связь 1) ковалентная неполярная 2) ковалентная полярная 3) ионная
- 12. 4 Наибольшая степень окисления азота в соединении 1) HNO3 2) Na3N 3) N2O 4) N2H4 В
- 13. 5 К основным оксидам относится 1) NO 2) К2О 3) Fe2O3 4) СО Вещества, формулы которых
- 14. 6 Масса всех веществ, участвующих в химической реакции 1) увеличивается 2) уменьшается 3) не изменяется 4)
- 15. 7 Наименьшее число ионов образуется в разбавленном растворе при полной диссоциации 1 моль FeCl3 2) Na2S
- 16. 8 Газ выделяется при взаимодействии 1) MgCl2 и Ba(NO3)2 2) Na2CO3 и CaCl2 3) NH4Cl и
- 17. 9 И литий, и железо при комнатной температуре реагируют с 1) гидроксидом натрия 2) водой 3)
- 18. 10 Оксид цинка реагирует с каждым веществом пары 1) Na2O и H2O 2) SiO2 и Ag
- 19. 11 Железо взаимодействуете каждым из двух веществ: 1) оксид углерода (IV), водород 2) соляная кислота, кислород
- 20. 12 Среди веществ: NaCl, Na2S, Na2SO4 – в реакцию с раствором Cu(NO3)2 вступает(-ют) 1) только Na2S
- 21. 13 Верны ли суждения о химическом загрязнении окружающей среды и его последствиях? А. Повышенное содержание в
- 22. 14 Степень окисления химических элементов. Окислитель и восстановитель. Окислительно-восстановительные реакции 1. К окислительно-восстановительным реакциям относятся 1)
- 23. 15 Массовая доля азота в нитрате алюминия равна 1) 19,7% 2) 27,2% 3) 36,8% 4) 54,9%
- 25. Периодический закон Д.И. Менделеева Закономерности изменения свойств элементов и их соединений в связи с положением в
- 26. 16 В каких рядах химические элементы расположены в порядке уменьшения кислотных свойств их высших оксидов? 1)
- 27. Первоначальные сведения об органических веществах 17 Углеводороды предельные и непредельные: метан, этан, этилен, ацетилен Кислородсодержащие вещества:
- 28. Первоначальные сведения об органических веществах Для этанола верны следующие утверждения: 1) в состав молекулы входит один
- 29. 18 Определение характера среды раствора кислот и щелочей с помощью индикаторов. Качественные реакции на ионы в
- 30. 14 В приборе, изображённом на рисунке, получают 1) хлор 2) аммиак 3) кислород 4) хлороводород Получение
- 31. Группы газов газы – простые вещества N2, O2, H2, Cl2 2) газы – оксиды CO, CO2,
- 32. Физические свойства газов Водород - Н2– самый легкий, бесцветный, не имеет запаха. Кислород - О2 -
- 33. Получение какого газа показано на рисунке? А) аммиак Б) кислород В) углекислый газ Г) водород
- 34. Идентификация газов О2 Поддерживает горение – тлеющая лучинка в нем вспыхивает Н2 Горючий газ. Набранный в
- 35. Определение какого газа показано на рисунке? А) аммиак Б) кислород В) углекислый газ Г) сероводород
- 36. Установите соответствие между двумя веществами и реактивом, с помощью которого эти вещества можно различить. 18
- 37. 19 Химические свойства простых веществ. Химические свойства сложных веществ.
- 38. Установите соответствие между названием вещества и реагентами, с которыми это вещество может взаимодействовать. НАЗВАНИЕ ВЕЩЕСТВА РЕАГЕНТЫ
- 39. 20 Степень окисления химических элементов. Окислитель и восстановитель. Окислительно-восстановительные реакции
- 40. Установите соответствие между схемой химической реакции и веществом - восстановителем в ней. СХЕМА РЕАКЦИИ ВОССТАНОВИТЕЛЬ А)
- 41. 21
- 42. 22 170 г раствора нитрата серебра смешали с избытком раствора хлорида натрия. Выпал осадок массой 8,61
- 43. С3 22 Химические свойства простых веществ. Химические свойства сложных веществ. Взаимосвязь различных классов неорганических веществ. Реакции
- 44. С3 Для определения качественного состава неизвестной соли учащимся выдали белое кристаллическое вещество, хорошо растворимое в воде
- 45. На занятиях химического кружка учащиеся исследовали кристаллическое вещество белого цвета. В результате добавления к нему гидроксида
- 46. 22
- 48. Скачать презентацию









































 Метаболизм азота
Метаболизм азота Важнейшие классы неорганических соединений. Соли
Важнейшие классы неорганических соединений. Соли Термохимия. Задания
Термохимия. Задания Кислоты. Классификация. Номенклатура
Кислоты. Классификация. Номенклатура 9-12 Гидролиз солей -
9-12 Гидролиз солей - Получение метанола из синтез-газа
Получение метанола из синтез-газа Предмет органической химии
Предмет органической химии Альдегиды и кетоны
Альдегиды и кетоны Железоуглеродистые сплавы. Диаграмма равновесного состояния железо-цементит. Фазы и структурные составляющие
Железоуглеродистые сплавы. Диаграмма равновесного состояния железо-цементит. Фазы и структурные составляющие Составление уравнений окислительно-восстановительных реакций
Составление уравнений окислительно-восстановительных реакций Альдегиды и кетоны
Альдегиды и кетоны Сахароза (С12Н22О11)
Сахароза (С12Н22О11) Классификация реакций в органической химии
Классификация реакций в органической химии Комплексные соединения
Комплексные соединения Презентация на тему Основания и их классификация
Презентация на тему Основания и их классификация 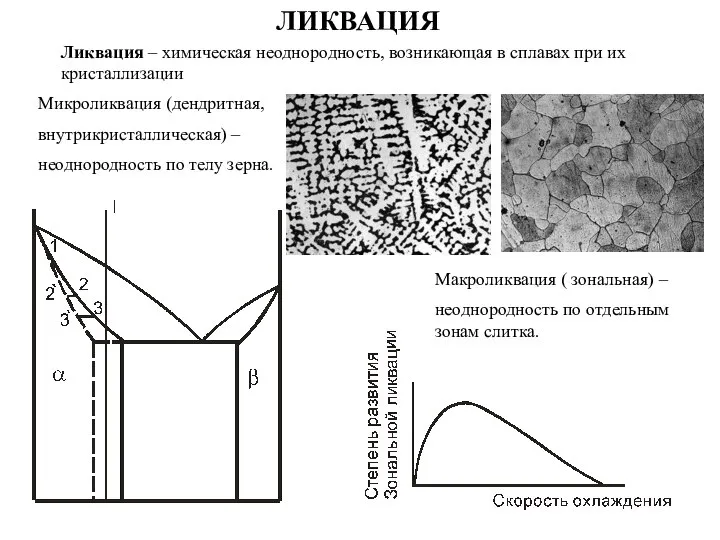 Ликвация. Микроликвация
Ликвация. Микроликвация Синтез-газ
Синтез-газ Реакции замещения
Реакции замещения Синтез 7,7 - дихлоробицикло [4.1.0] гептана
Синтез 7,7 - дихлоробицикло [4.1.0] гептана Углерод и его аллотропные модификации. Органическая химия - химия углерода
Углерод и его аллотропные модификации. Органическая химия - химия углерода Использование элементов модульной технологии на уроках химии
Использование элементов модульной технологии на уроках химии Физические свойства водорода
Физические свойства водорода Презентация на тему Витамины. Урок химии 10 класс
Презентация на тему Витамины. Урок химии 10 класс  Алюминий
Алюминий Окислительно-восстановительные реакции
Окислительно-восстановительные реакции Презентация по Химии "Ковалентная химическая связь"
Презентация по Химии "Ковалентная химическая связь"  Презентация на тему Изотопы
Презентация на тему Изотопы  Введение в химию. Вещества. Факультатив по химии для учащихся 7 класса
Введение в химию. Вещества. Факультатив по химии для учащихся 7 класса