Содержание
- 2. Алкадиены – ациклические углеводороды, содержащие в молекуле, помимо одинарных связей, две двойные связи между атомами углерода.
- 3. Общая формула CnH2n-2 Алкадиены – ациклические углеводороды, содержащие в молекуле, помимо одинарных связей, две двойные связи
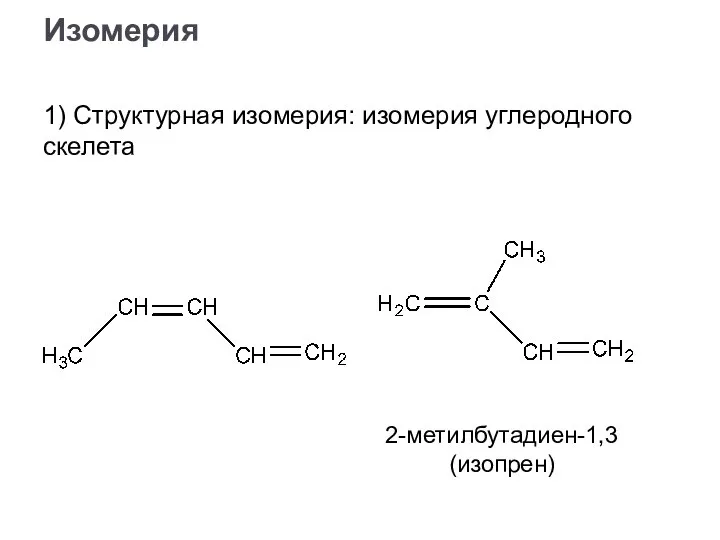
- 4. 1) Структурная изомерия: изомерия углеродного скелета Изомерия 2-метилбутадиен-1,3 (изопрен)
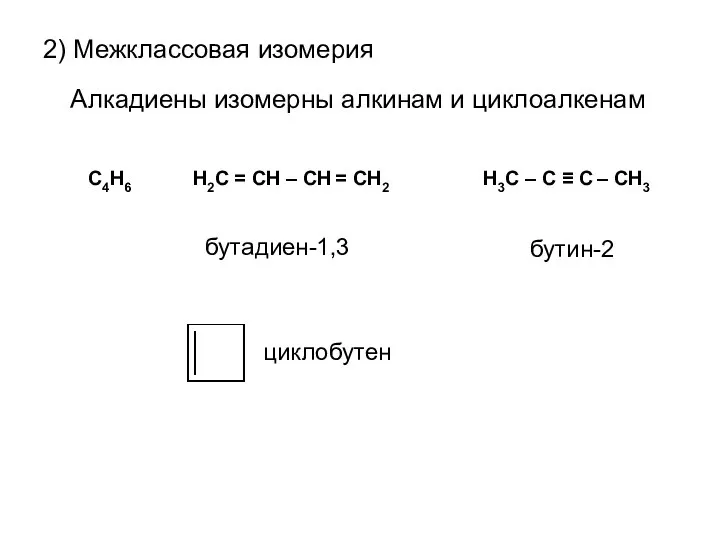
- 5. Алкадиены изомерны алкинам и циклоалкенам 2) Межклассовая изомерия C4H6 H3C – C ≡ C – CH3
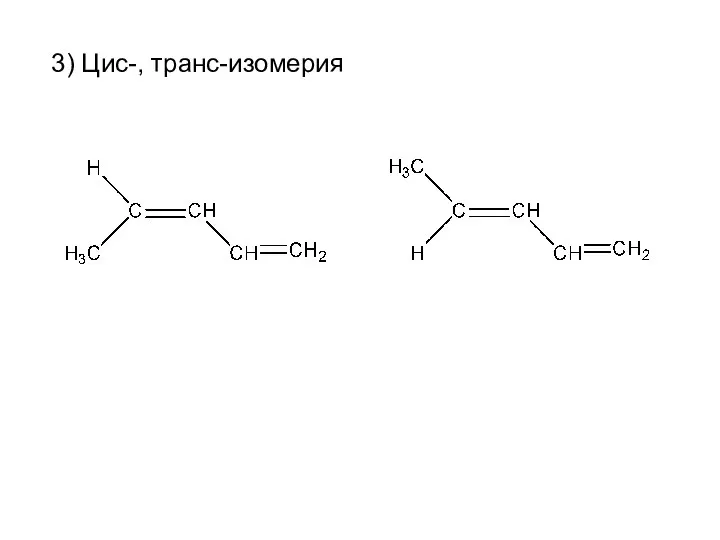
- 6. 3) Цис-, транс-изомерия
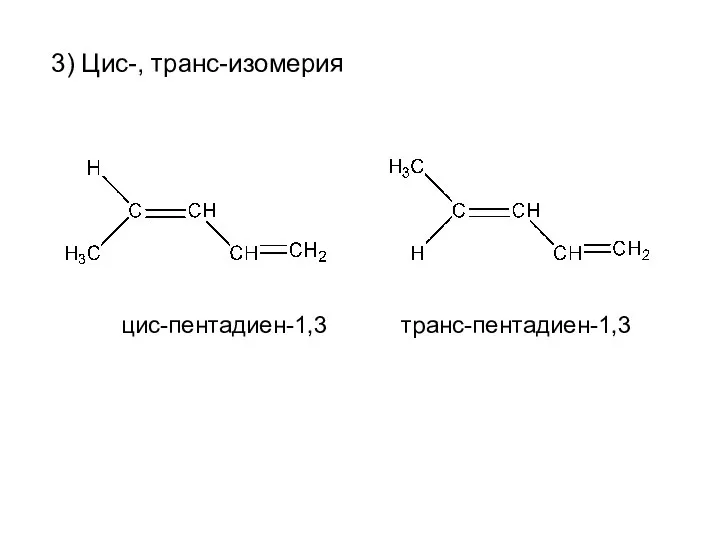
- 7. 3) Цис-, транс-изомерия цис-пентадиен-1,3 транс-пентадиен-1,3
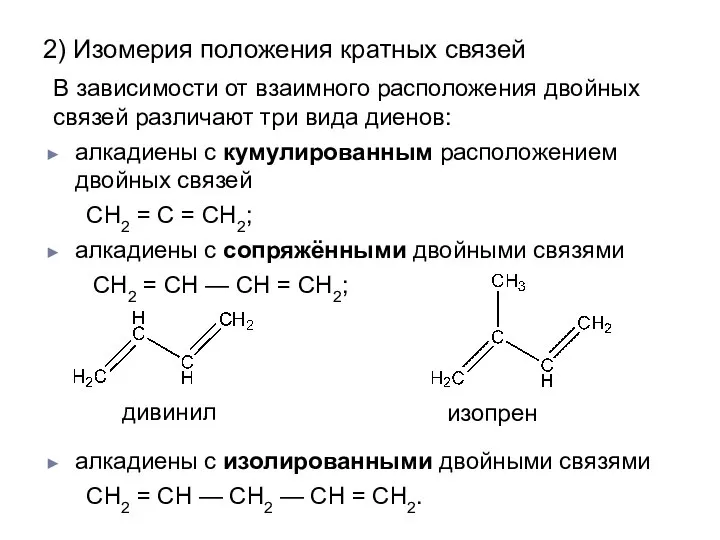
- 8. 2) Изомерия положения кратных связей В зависимости от взаимного расположения двойных связей различают три вида диенов:
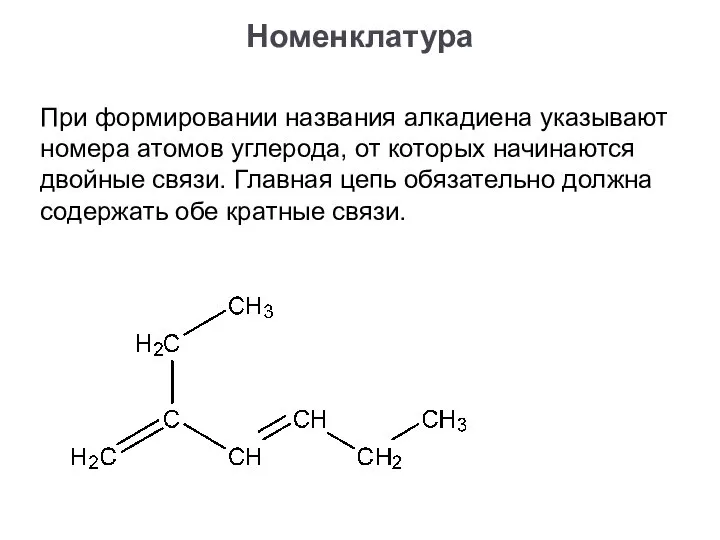
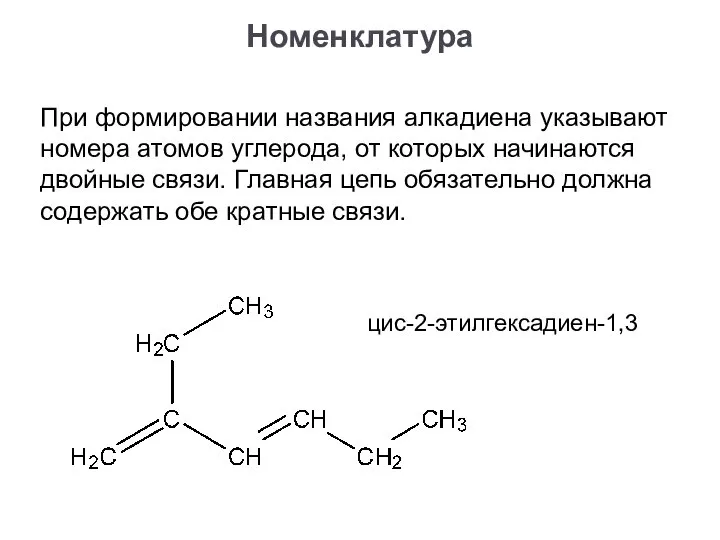
- 9. При формировании названия алкадиена указывают номера атомов углерода, от которых начинаются двойные связи. Главная цепь обязательно
- 10. При формировании названия алкадиена указывают номера атомов углерода, от которых начинаются двойные связи. Главная цепь обязательно
- 11. При нормальных условиях пропадиен-1,2, бутадиен-1,3 (дивинил) — газы 2-метилбутадиен-1,3 (изопрен) — летучая жидкость. Алкадиены с изолированными
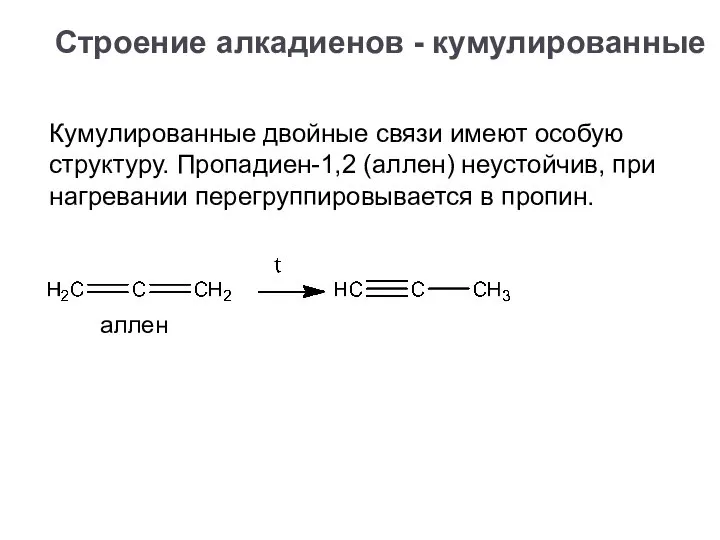
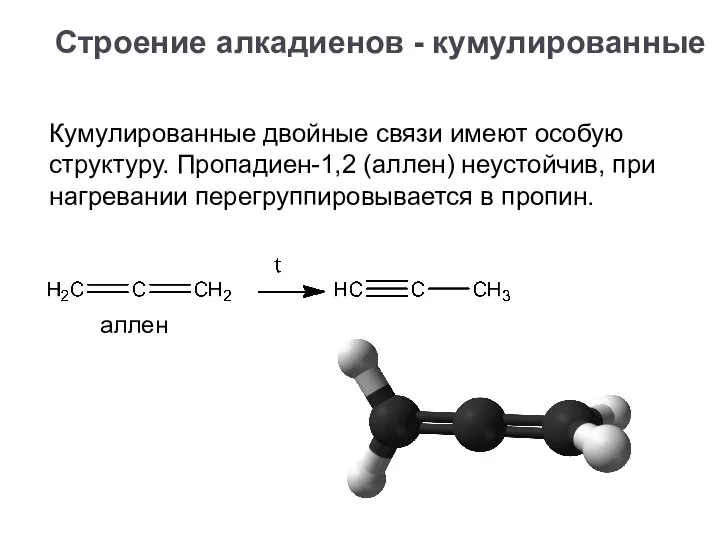
- 12. аллен Кумулированные двойные связи имеют особую структуру. Пропадиен-1,2 (аллен) неустойчив, при нагревании перегруппировывается в пропин. Строение
- 13. Кумулированные двойные связи имеют особую структуру. Пропадиен-1,2 (аллен) неустойчив, при нагревании перегруппировывается в пропин. аллен Строение
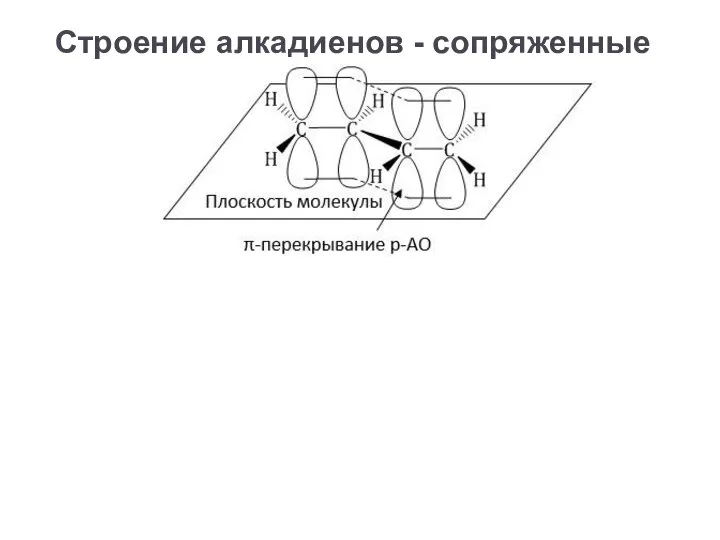
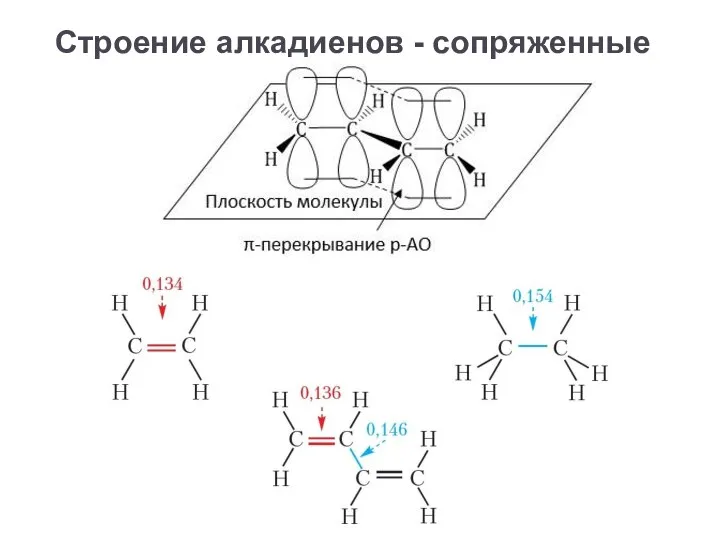
- 14. Строение алкадиенов - сопряженные
- 15. Строение алкадиенов - сопряженные
- 16. кумулированные алкадиены = интересно, но сложно - не проходим СН2 = С = СН2; сопряжённые алкадиены
- 17. Для алкадиенов характерны реакции электрофильного и радикального присоединения, окисления и полимеризации. AdE, AdR Химические свойства
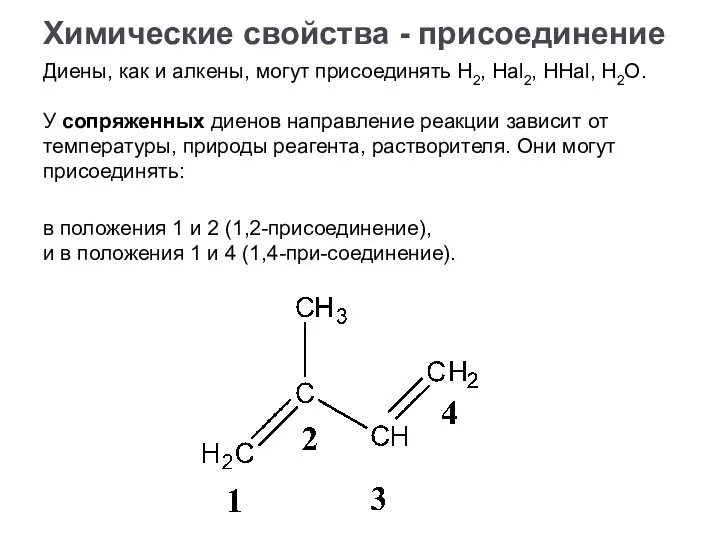
- 18. Диены, как и алкены, могут присоединять H2, Hal2, HHal, H2O. У сопряженных диенов направление реакции зависит
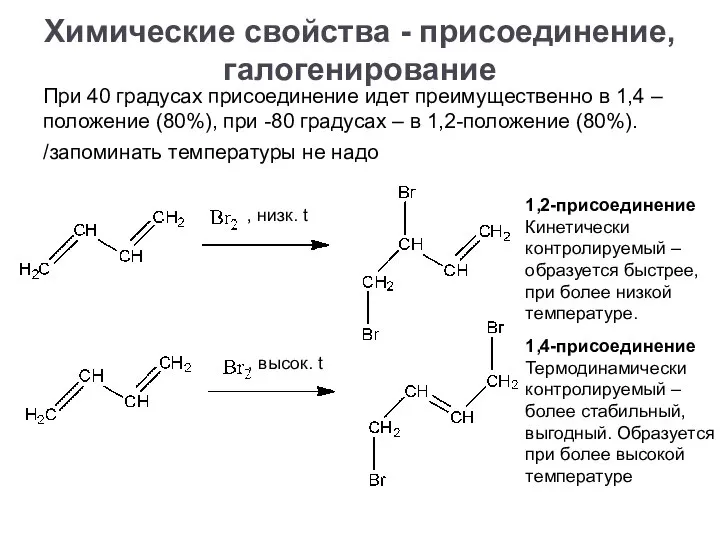
- 19. При 40 градусах присоединение идет преимущественно в 1,4 – положение (80%), при -80 градусах – в
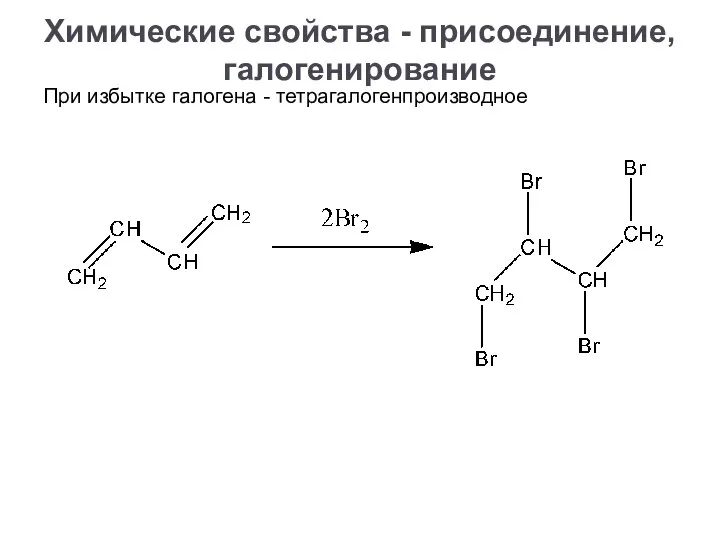
- 20. При избытке галогена - тетрагалогенпроизводное Химические свойства - присоединение, галогенирование
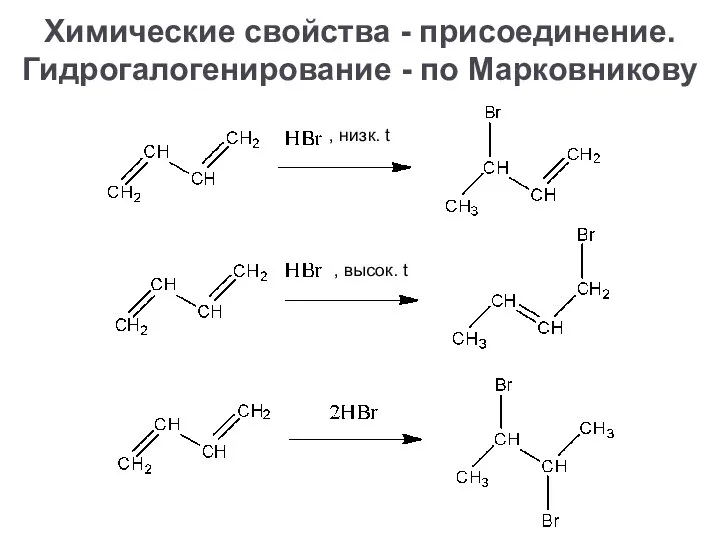
- 21. Химические свойства - присоединение. Гидрогалогенирование - по Марковникову , высок. t , низк. t
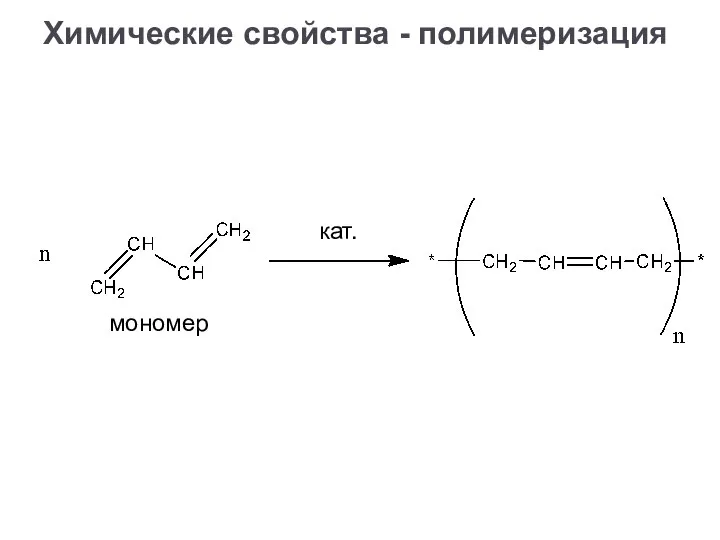
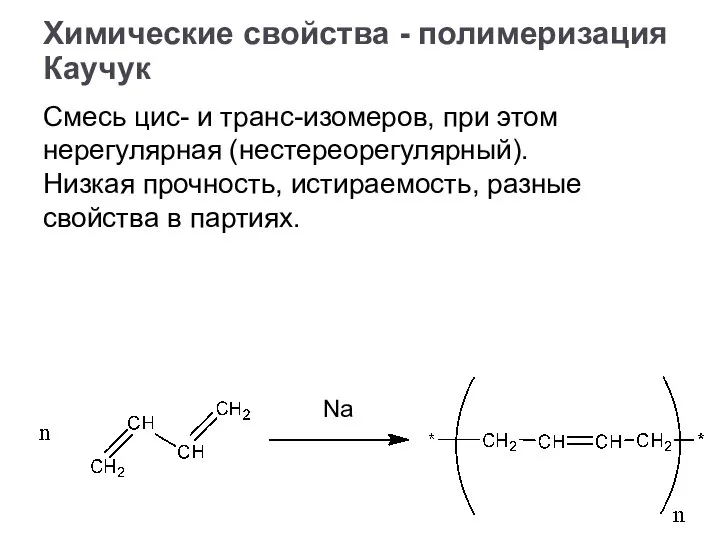
- 22. Химические свойства - полимеризация мономер кат.
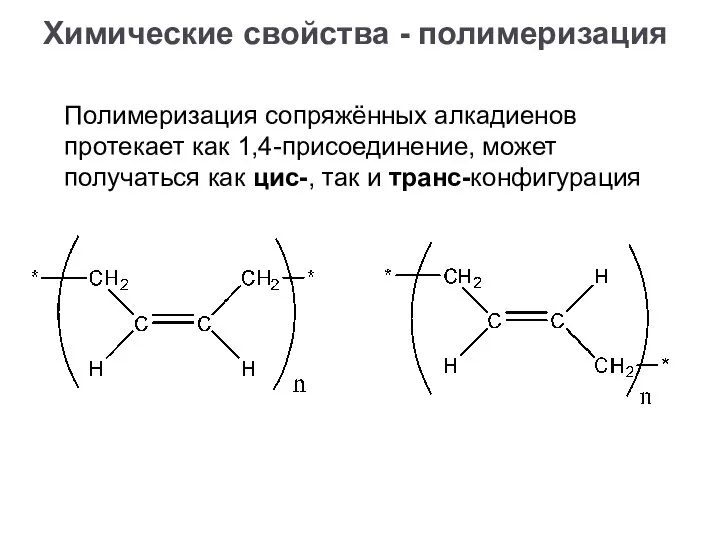
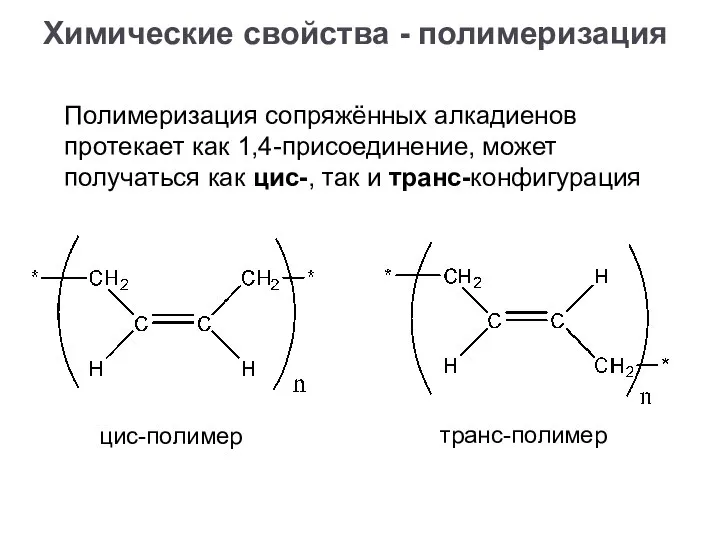
- 23. Полимеризация сопряжённых алкадиенов протекает как 1,4-присоединение, может получаться как цис-, так и транс-конфигурация Химические свойства -
- 24. Полимеризация сопряжённых алкадиенов протекает как 1,4-присоединение, может получаться как цис-, так и транс-конфигурация Химические свойства -
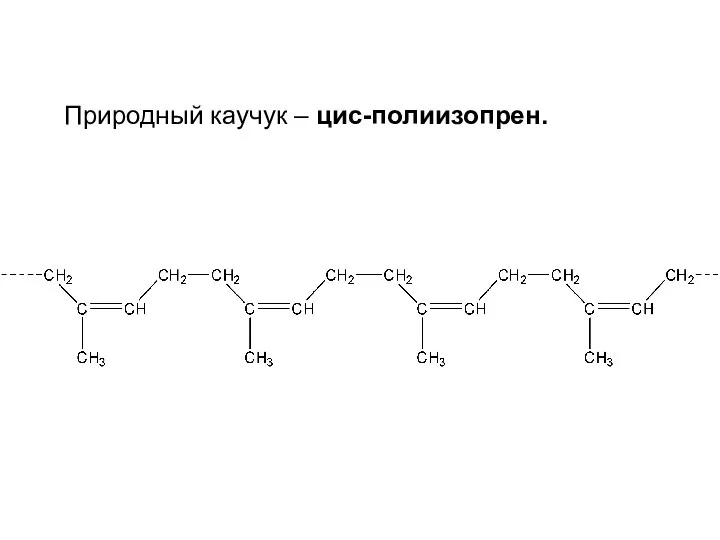
- 25. Природный каучук – цис-полиизопрен.
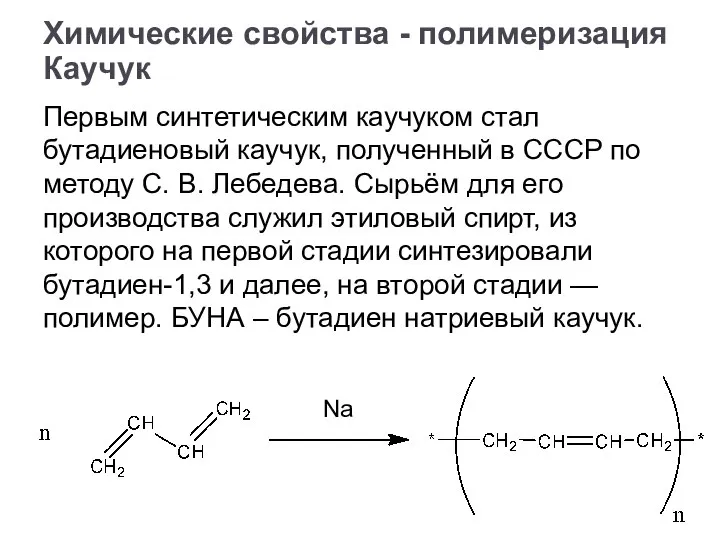
- 26. Каучук Первым синтетическим каучуком стал бутадиеновый каучук, полученный в СССР по методу С. В. Лебедева. Сырьём
- 27. Каучук Смесь цис- и транс-изомеров, при этом нерегулярная (нестереорегулярный). Низкая прочность, истираемость, разные свойства в партиях.
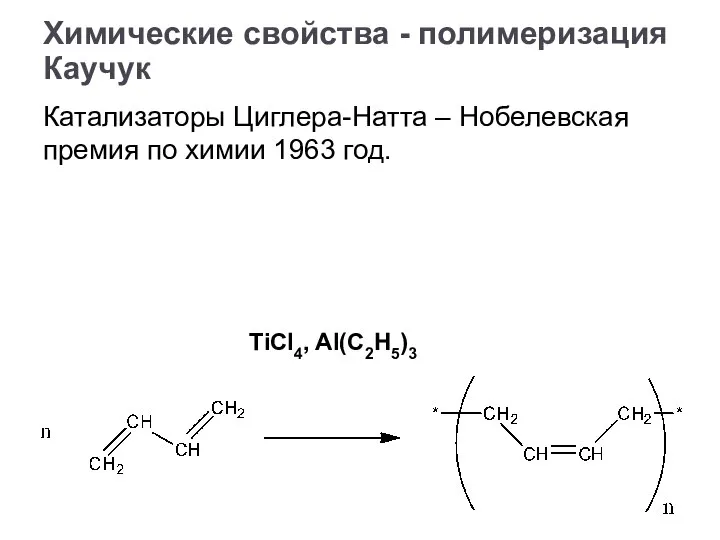
- 28. Каучук Катализаторы Циглера-Натта – Нобелевская премия по химии 1963 год. Химические свойства - полимеризация TiCl4, Al(C2H5)3
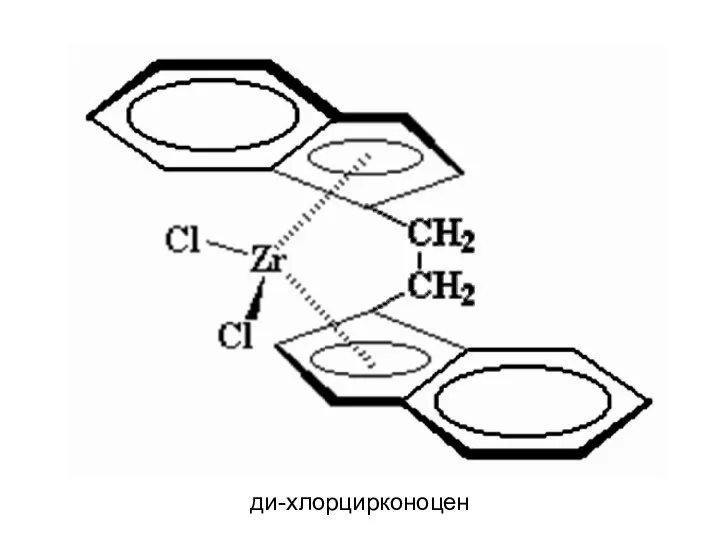
- 29. ди-хлорцирконоцен
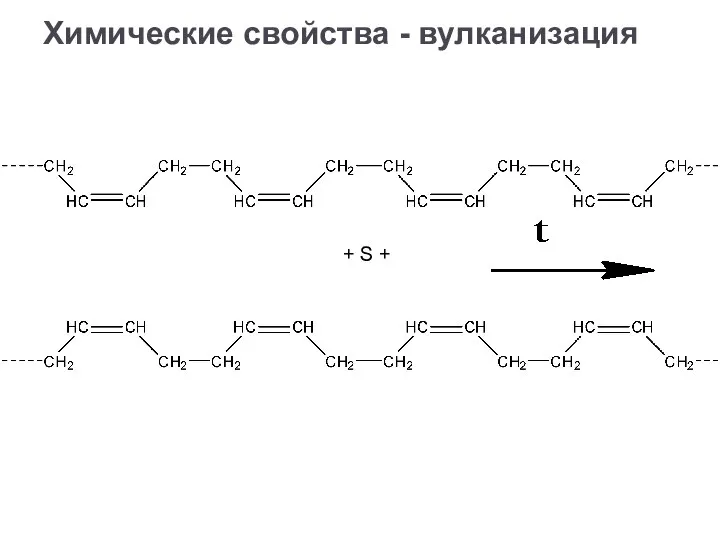
- 30. Химические свойства - вулканизация + S +
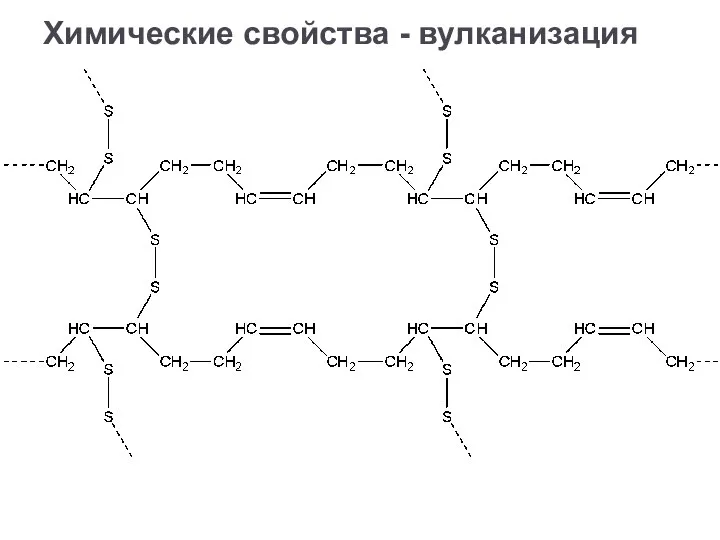
- 31. Химические свойства - вулканизация
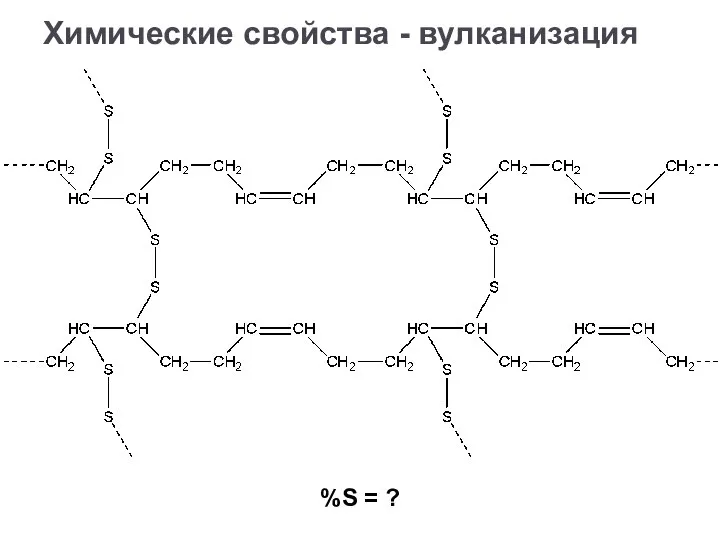
- 32. Химические свойства - вулканизация %S = ?
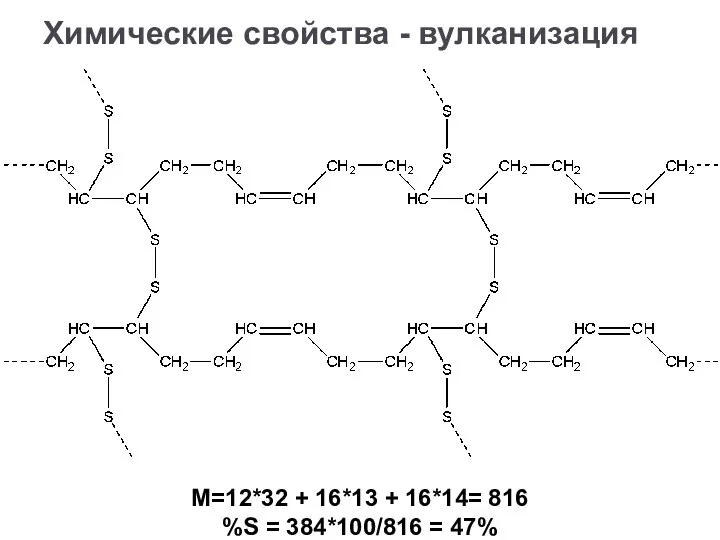
- 33. Химические свойства - вулканизация M=12*32 + 16*13 + 16*14= 816 %S = 384*100/816 = 47%
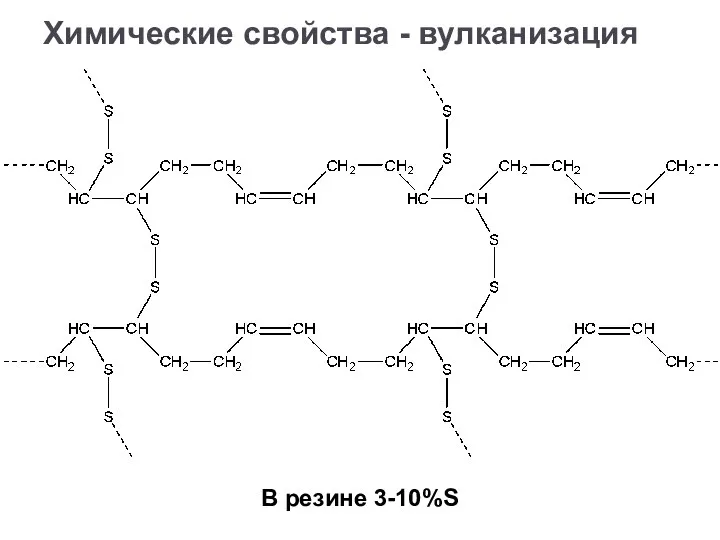
- 34. Химические свойства - вулканизация В резине 3-10%S
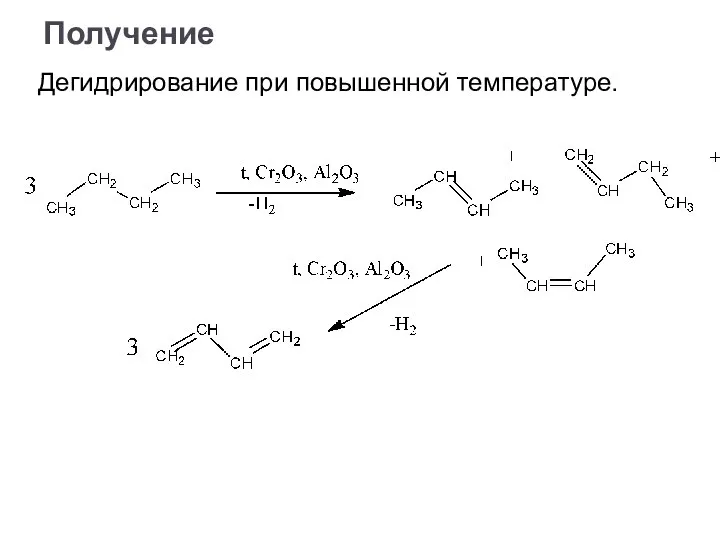
- 35. Дегидрирование при повышенной температуре. Получение
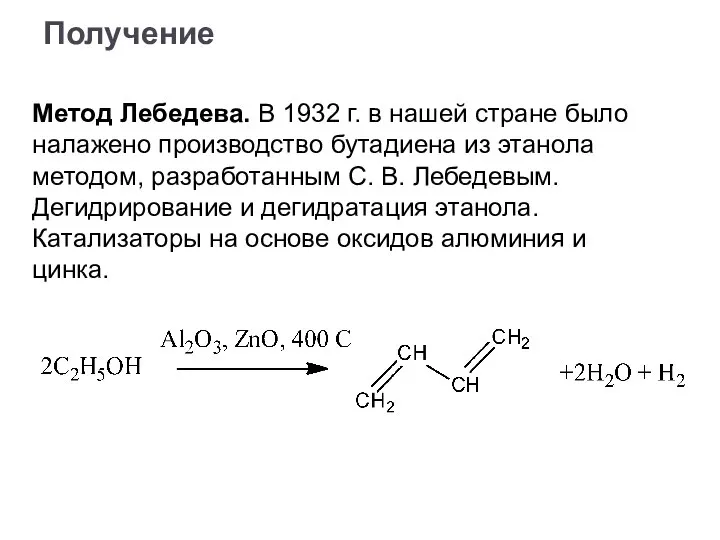
- 36. Метод Лебедева. В 1932 г. в нашей стране было налажено производство бутадиена из этанола методом, разработанным
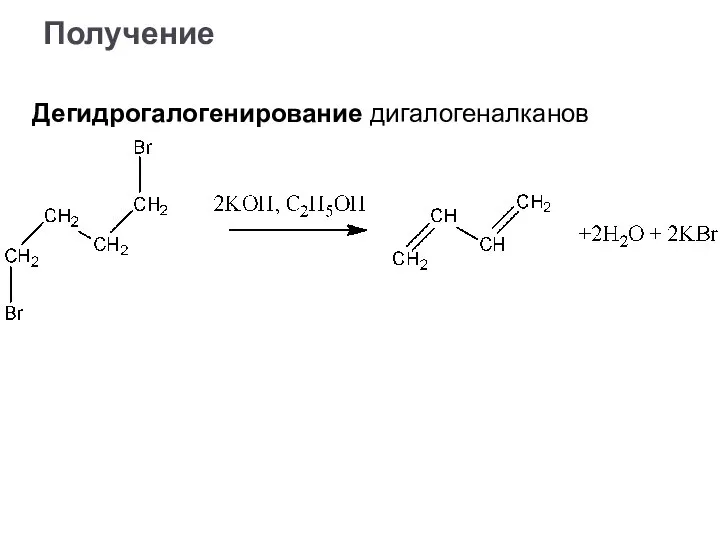
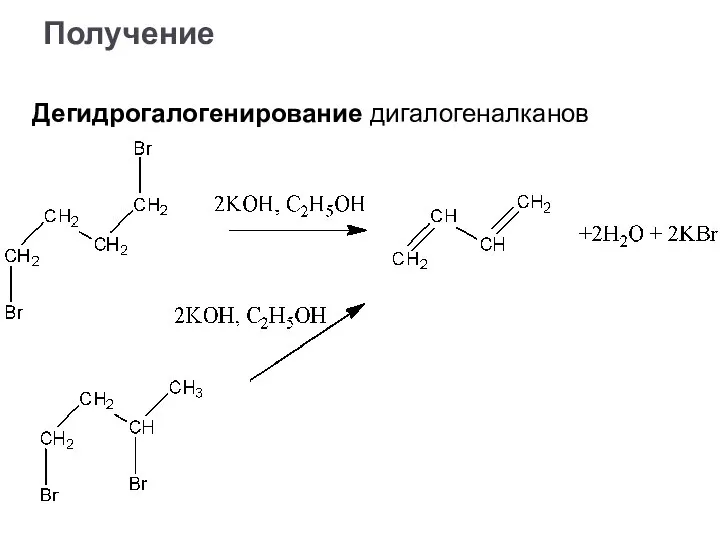
- 37. Получение Дегидрогалогенирование дигалогеналканов
- 38. Получение Дегидрогалогенирование дигалогеналканов
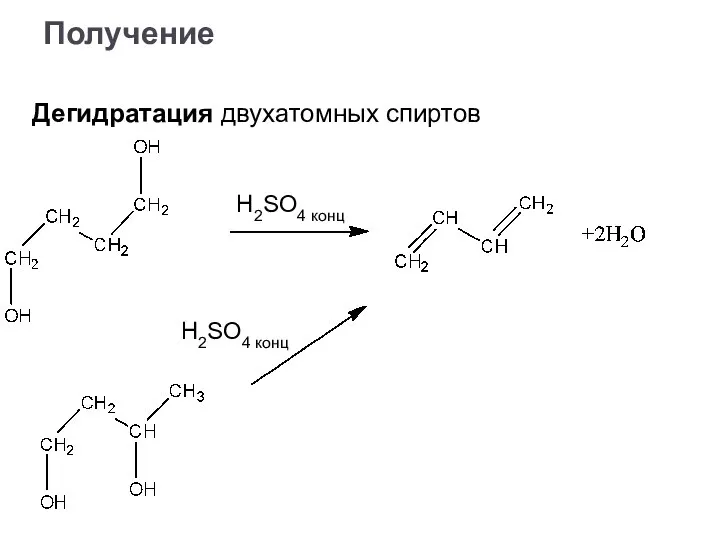
- 39. Получение Дегидратация двухатомных спиртов H2SO4 конц H2SO4 конц
- 41. Натуральный и синтетический каучуки. Резина. Эбонит Каучуки - продукты полимеризации диеновых углеводородов и их производных. Природный
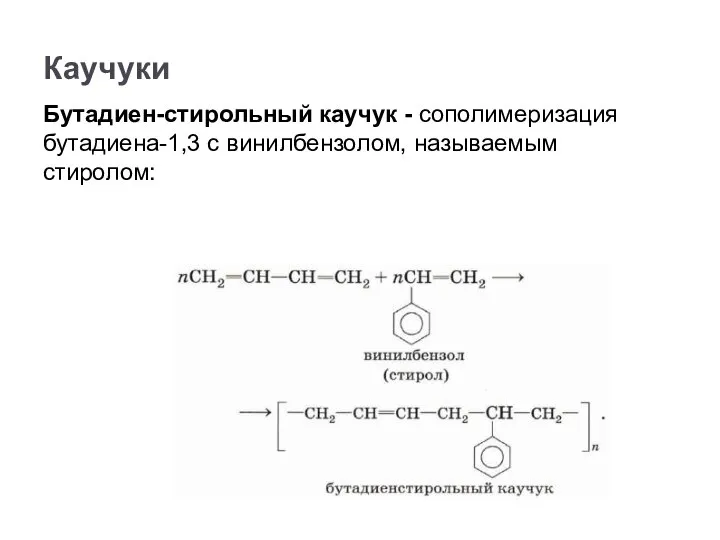
- 42. Бутадиен-стирольный каучук - сополимеризация бутадиена-1,3 с винилбензолом, называемым стиролом: Каучуки
- 44. Скачать презентацию







 Основы МКТ
Основы МКТ Практическая работа 1. ХТП. Классификация химических реакций
Практическая работа 1. ХТП. Классификация химических реакций Аммиа́к (нитрид водорода)
Аммиа́к (нитрид водорода) Карбоксилденген этоксилаттар
Карбоксилденген этоксилаттар Углеводы
Углеводы Оценка пригодности природной воды в качестве питьевой по формуле М.Г. Курлова
Оценка пригодности природной воды в качестве питьевой по формуле М.Г. Курлова Вещество. Свойства веществ
Вещество. Свойства веществ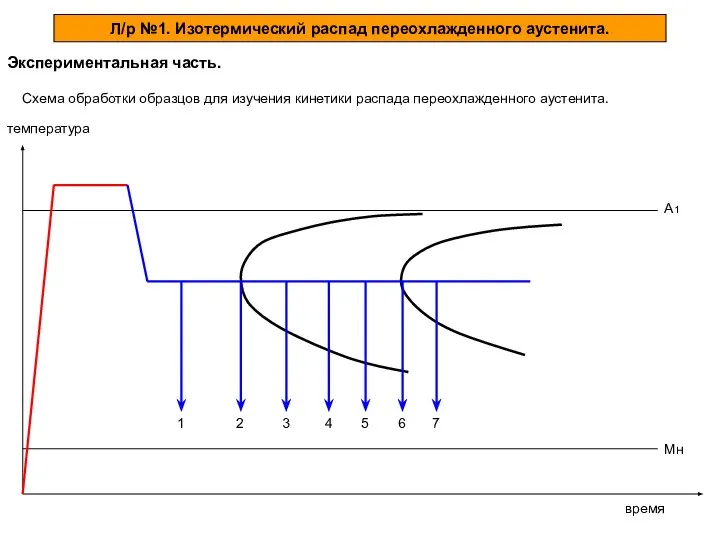 Изотермический распад переохлажденного аустенита. Экспериментальная часть
Изотермический распад переохлажденного аустенита. Экспериментальная часть Синтетическое моторное масло. Маркировка моторных масел
Синтетическое моторное масло. Маркировка моторных масел Понятие о химической реакции. Реакции, идущие без изменения состава веществ
Понятие о химической реакции. Реакции, идущие без изменения состава веществ Классификация химических реакций
Классификация химических реакций Соли. Определение, состав, классификация, физические свойства, применение
Соли. Определение, состав, классификация, физические свойства, применение Органическая химия как наука. Основные положения теории строения химических соединений. Структурная изомерия
Органическая химия как наука. Основные положения теории строения химических соединений. Структурная изомерия Многообразие органических веществ
Многообразие органических веществ Окислительно - восстановительные свойства серной кислоты
Окислительно - восстановительные свойства серной кислоты Карбонат натрия
Карбонат натрия Взаимодействие молекул (7 класс)
Взаимодействие молекул (7 класс) Виды химической связи
Виды химической связи Основные понятия в химии
Основные понятия в химии Каучук и резиновые материалы
Каучук и резиновые материалы Оливины. Структура оливинов
Оливины. Структура оливинов Метод окислительно - восстановительного титрования
Метод окислительно - восстановительного титрования Триады, октавы, спираль, таблица
Триады, октавы, спираль, таблица Алкадиены: номенклатуры, изомерия. Тест
Алкадиены: номенклатуры, изомерия. Тест Магний и кальций
Магний и кальций ZnS и ZnSe как оптические материалы,люминофоры, лазерные матрицы
ZnS и ZnSe как оптические материалы,люминофоры, лазерные матрицы Презентация на тему Гидролиз солей
Презентация на тему Гидролиз солей  Самородные металлы
Самородные металлы