Слайд 21.Положение в ПС
Цинк (Zn) располагается в 4 периоде, в II группе, побочной

подгруппе, имеет порядковый номер 30.
Цинк – d-элемент, металл.
Степени окисления минимальная: 0; максимальная: +2
Высший оксид: ZnO – оксид цинка.
Проявляет амфотерные свойства:
ZnO + 2NaOH + H2O ⟶ Na2[Zn(OH)4]
ZnO + 2HCl ⟶ ZnCl2 + H2O
Высший гидроксид: Zn(OH)2 – гидроксид цинка.
Проявляет амфотерные свойства:
Zn(OH)2 + 2NaOH ⟶ Na2[Zn(OH)4]
Zn(OH)2 + 2HCl ⟶ ZnCl2 + 2H2O
Слайд 32.Нахождение в природе
Цинк достаточно распространённый элемент, он содержится в земной коре, практически
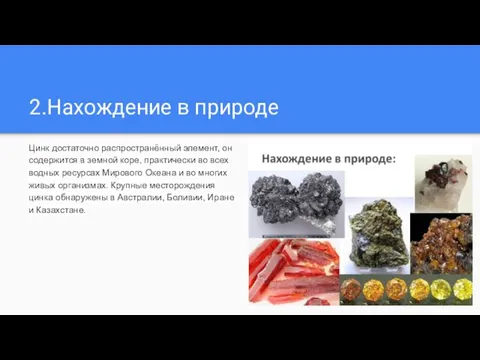
во всех водных ресурсах Мирового Океана и во многих живых организмах. Крупные месторождения цинка обнаружены в Австралии, Боливии, Иране и Казахстане.
Слайд 43.Получение
Пирометаллургический процесс
Оксид цинка сплавляют с коксом при температуре 1250–1350°С в огнеупорных ретортах:
ZnO

+ C = Zn + CO;
пары цинка конденсируются.
Гидрометаллургический процесс
Оксид цинка растворяют в серной кислоте:
ZnO + H2SO4 = ZnSO4 + H2O;
полученный раствор сульфата цинка подвергают электролизу, на катоде выделяется цинк:
2ZnSO4 + 2H2O(электролиз)=2Zn + O2 + 2H2SO4.
Для получения цинка высокой чистоты используют дистилляцию в инертной атмосфере или в вакууме.
Слайд 54.Физические свойства
Температура плавления — 419,58°С.
Температура кипения — 906,2° С.
Изменение температурного режима

активно влияет на изменение физических свойств металлического цинка:
комнатная температура ( 20 °С ) — цинк не пластичен, хрупок,
в диапазоне от 100°С до 150 физические свойства улучшаются, цинк становится пластичен, что активно используют при прокатки цинковых листов и проволоки,
с повышением температуры от 200 до 250°С физические характеристики цинка изменяются в худшею сторону (становится хрупким и ломким).
Слайд 65.1Химические свойства(простые вещества)
1. Цинк – сильный восстановитель. Цинк – довольно активный металл,
но на воздухе он устойчив, так как покрывается тонким слоем оксида, предохраняющим его от дальнейшего окисления. При нагревании цинк реагирует со многими неметаллами.
Цинк реагирует с галогенами с образованием галогенидов:
Zn + I2 → ZnI2
Реакция цинка с иодом при добавлении воды:
Слайд 7Цинк реагирует с серой с образованием сульфидов:
Zn + S → ZnS
Слайд 8Цинк взаимодействует с кислородом с образованием оксида:
2Zn + O2 → 2ZnO
Слайд 95.2Химические свойства(сложные вещества)
Цинк реагирует с соляной кислотой:
Zn + 2HCl → ZnCl2

+ H2↑
Слайд 10 Цинк – амфотерный металл, он взаимодействует с щелочами. При взаимодействии цинка

с раствором щелочи образуется тетрагидроксоцинкат и водород:
Zn + 2KOH + 2H2O = K2[Zn(OH)4] + H2
Слайд 11Цинк реагирует с парами воды при температуре красного каления с образованием оксида

цинка и водорода:
Zn0 + H2+O → Zn+2O + H20
Слайд 126.Применение
Наносится на поверхность стальных поверхностей для предотвращения процессов коррозии (оцинковка и металлизация);
Используется

для извлечения или восстановления золота, серебра и других металлов;
Применяется в изготовлении некоторых видов аккумуляторов и батареек;
В медицинской практике входит в состав различных антисептических и противовоспалительных средств;
Входит в состав латуни, масляных красок, люминофоров, оптических стекол, флюса для пайки металлов и другие.
Слайд 137.Биологическая роль
является компонентом многих ферментов в организме (известно более 300)
влияет на рост

клеток, особенно во время их репродукции и дифференциации
участвует в обмене нуклеиновых кислот, транскрипции
участвует в обмене белков
участвует в обмене витамина А
поддерживает концентрацию витамина Е в крови, в т.ч. облегчая его всасывание
участвует в связывании некоторых гормонов с соответствующими рецепторами
поддерживает репродуктивную функцию
участвует в кроветворении
участвует в процессах регенерации кожи, секреции сальных желез
участвует в росте ногтей, волос
повышает иммунитет
снижает эффект токсических веществ
участвует в работе вкусовых и обонятельных рецепторов












 Протравка стекла с помощью ионного обмена
Протравка стекла с помощью ионного обмена Презентация на тему Жидкое состояние вещества
Презентация на тему Жидкое состояние вещества  Нуклеин қышқылдары
Нуклеин қышқылдары Химический элемент Li
Химический элемент Li Своя игра. Химия и охрана почв
Своя игра. Химия и охрана почв Сравнительная характеристика галогенов
Сравнительная характеристика галогенов Химические свойства бензола. Получение, применение. Учитель биологии-химии МОУ «СОШ р.п. Озинки» Хорова Людмила Владимировна
Химические свойства бензола. Получение, применение. Учитель биологии-химии МОУ «СОШ р.п. Озинки» Хорова Людмила Владимировна Массовая доля вещества в смеси. Таблица
Массовая доля вещества в смеси. Таблица Натуральный каучук
Натуральный каучук Классификация нефтей и товарных нефтепродуктов. Основные свойства нефтепродуктов
Классификация нефтей и товарных нефтепродуктов. Основные свойства нефтепродуктов 596550
596550 Презентация на тему Подготовка к ЕГЭ. Полезно знать
Презентация на тему Подготовка к ЕГЭ. Полезно знать  Соль - без вины виновата
Соль - без вины виновата Ресурс Лови оксиды для систематизации знаний, умений, навыков по теме Оксиды
Ресурс Лови оксиды для систематизации знаний, умений, навыков по теме Оксиды Метод ТРИЗ (теория решения изобретательских задач) при обучении химии
Метод ТРИЗ (теория решения изобретательских задач) при обучении химии Силикатная промышленность
Силикатная промышленность Электрохимия. Решение задач. ИДЗ 4
Электрохимия. Решение задач. ИДЗ 4 Виды химической связи
Виды химической связи Тесты для самопроверки
Тесты для самопроверки Комментарии к выполненным заданиям по темам Алканы и Алкены. 9 класс
Комментарии к выполненным заданиям по темам Алканы и Алкены. 9 класс минералы_4_блеск
минералы_4_блеск Аминокислоты. Общая формула
Аминокислоты. Общая формула Альдегиды
Альдегиды Превращения веществ
Превращения веществ Классификация неорганический веществ
Классификация неорганический веществ Интерактивная интеллектуальная игра Юный химик
Интерактивная интеллектуальная игра Юный химик Узоры на молоке. Опыт
Узоры на молоке. Опыт Физические свойства алкенов
Физические свойства алкенов