Содержание
- 2. Зачем все это надо? Слабое место учеников нашей школы – абстрактное мышление. Это вызывает трудности в
- 3. Что такое моделирование? Модель – это упрощенное представление реального устройства, явления и/или протекающих в нем процессов.
- 4. Моделирование процессов электролитической диссоциации
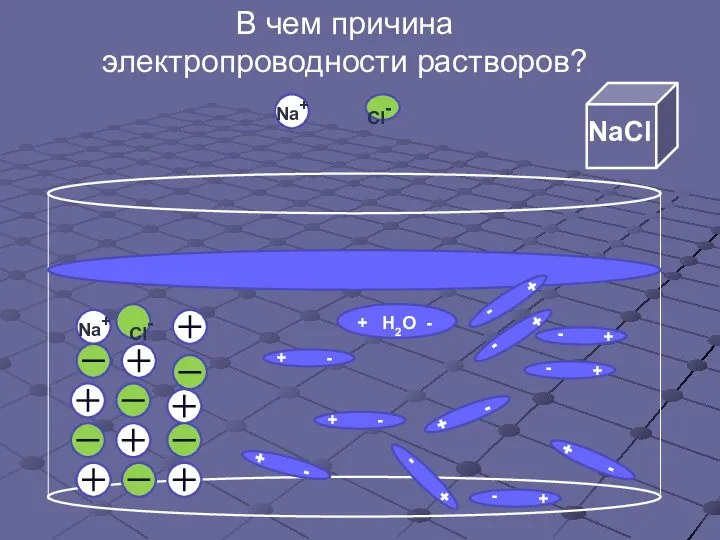
- 5. В чем причина электропроводности растворов? Cl-
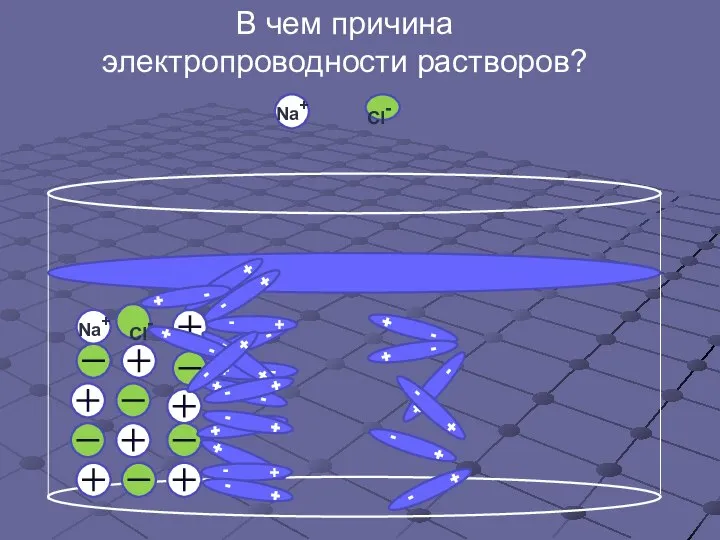
- 6. В чем причина электропроводности растворов? Cl-
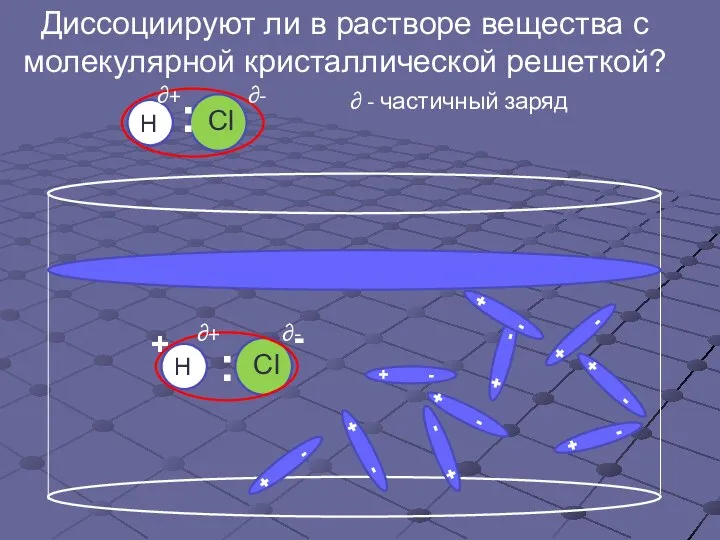
- 7. Диссоциируют ли в растворе вещества с молекулярной кристаллической решеткой? : : ∂+ ∂- ∂ - частичный
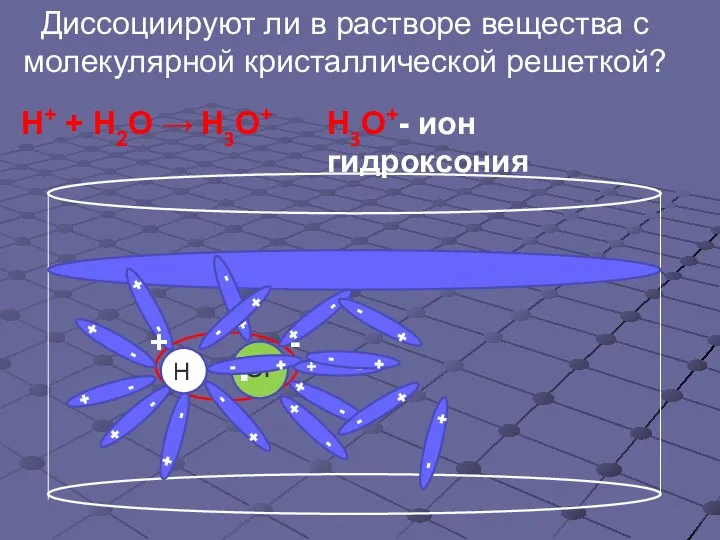
- 8. Диссоциируют ли в растворе вещества с молекулярной кристаллической решеткой? Н+ + Н2О → Н3О+ Н3О+- ион
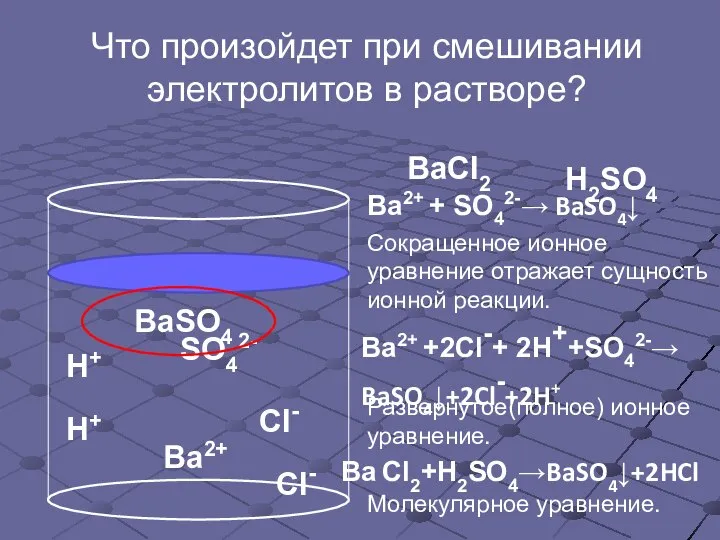
- 9. Что произойдет при смешивании электролитов в растворе? BaCl2 Ba2+ Cl- H2SO4 H+ H+ SO42- Cl- Ba2+
- 10. Моделирование влияния различных факторов на скорость химической реакции
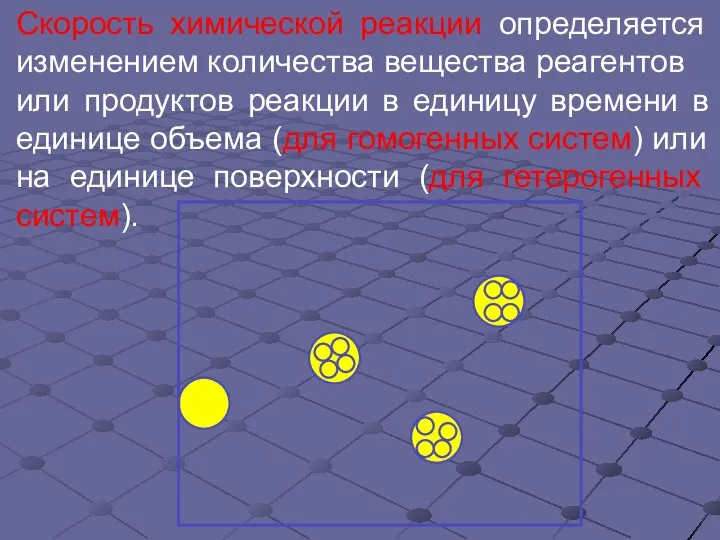
- 11. Скорость химической реакции определяется изменением количества вещества реагентов или продуктов реакции в единицу времени в единице
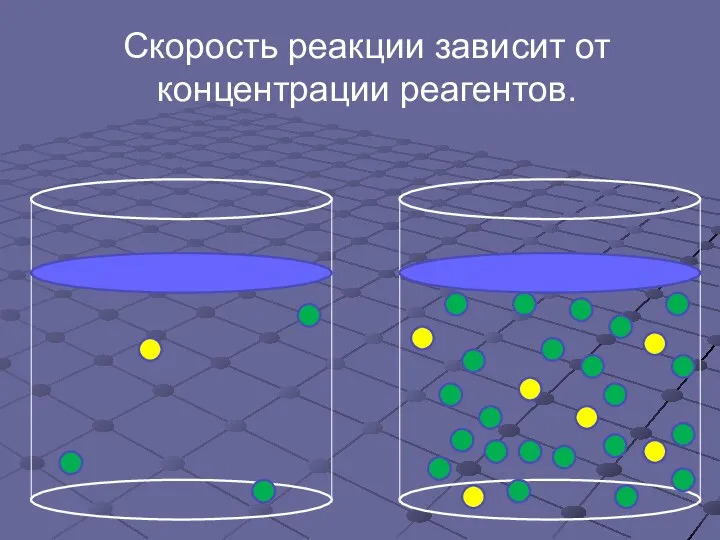
- 12. Скорость реакции зависит от концентрации реагентов.
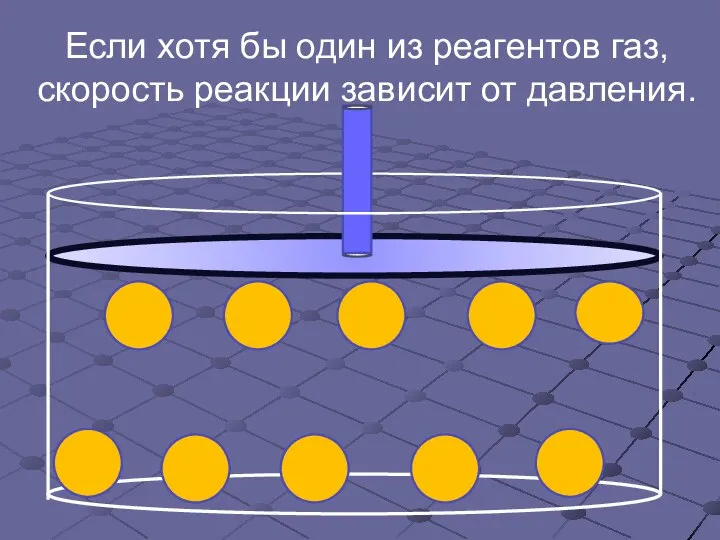
- 13. Если хотя бы один из реагентов газ, скорость реакции зависит от давления.
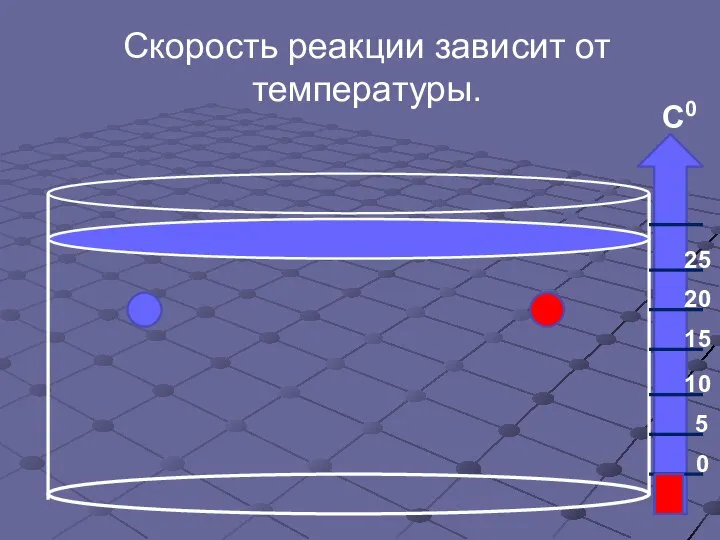
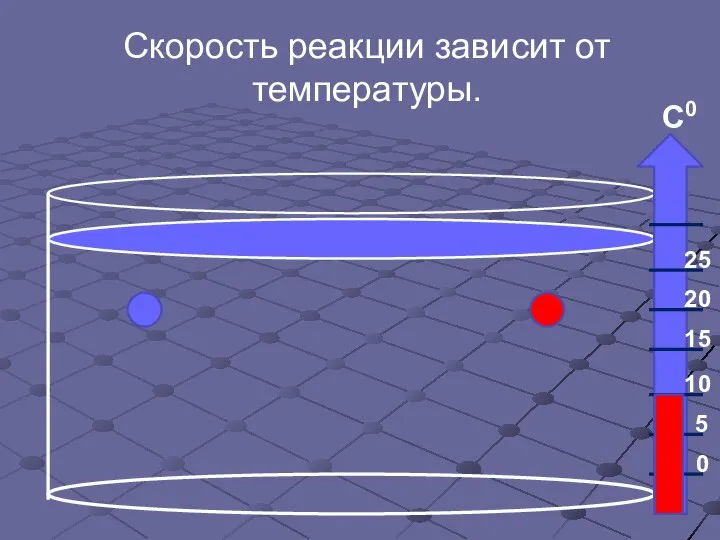
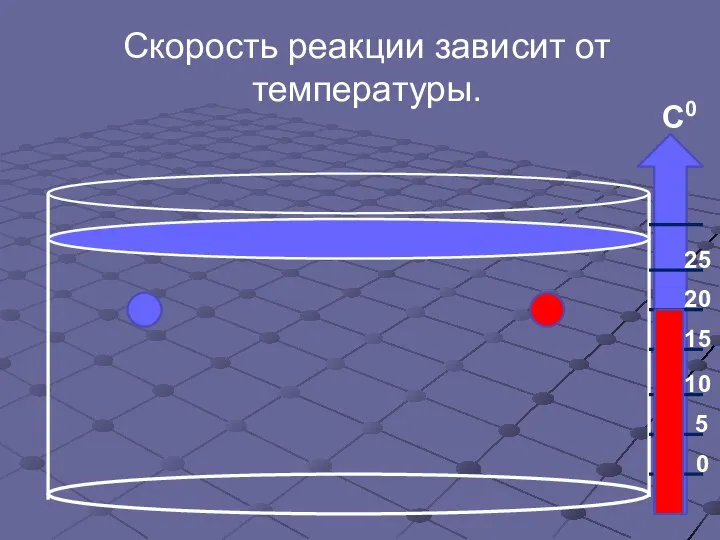
- 14. Скорость реакции зависит от температуры.
- 15. Скорость реакции зависит от температуры.
- 16. Скорость реакции зависит от температуры.
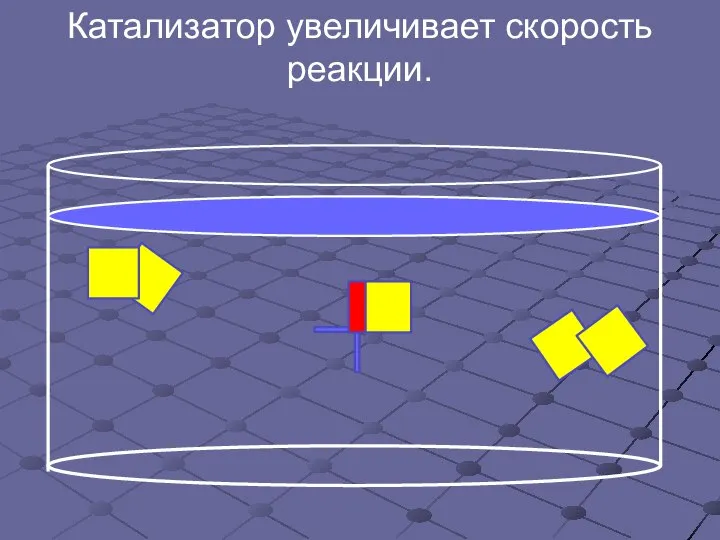
- 17. Катализатор увеличивает скорость реакции.
- 18. Модели понятий и формул
- 19. Атомы разных элементов имеют разную массу. Различие в массе вызвано разным количеством протонов и нейтронов в
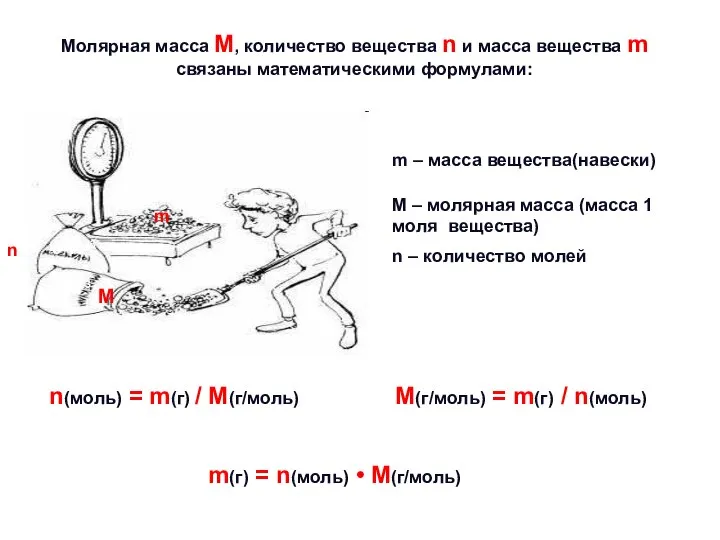
- 20. Молярная масса М, количество вещества n и масса вещества m связаны математическими формулами: n(моль) = m(г)
- 22. Скачать презентацию






 Презентация на тему Соединения серы
Презентация на тему Соединения серы  Основные законы и понятия химии. Основные классы неорганических соединений. Химический эквивалент. Закон эквивалентов
Основные законы и понятия химии. Основные классы неорганических соединений. Химический эквивалент. Закон эквивалентов Незаменимая уксусная кислота
Незаменимая уксусная кислота Перегонка. Вклад алхимиков в органическую химию
Перегонка. Вклад алхимиков в органическую химию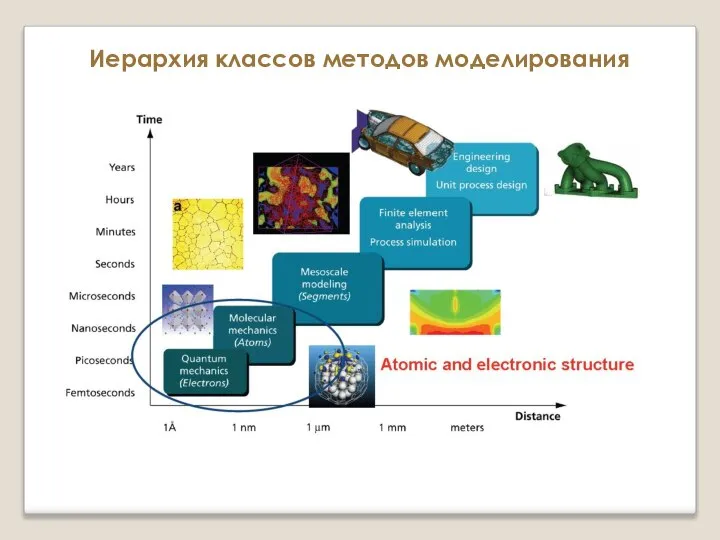 Иерархия классов методов моделирования. Атомистические и микроскопические методы
Иерархия классов методов моделирования. Атомистические и микроскопические методы Магний и кальций
Магний и кальций Сахароза, крахмал, целлюлоза
Сахароза, крахмал, целлюлоза Строение сложного фермента
Строение сложного фермента Хімія у вирішенні промислової проблеми
Хімія у вирішенні промислової проблеми Вещество и тело. Атом и молекула. Свойства веществ. Простые и сложные вещества. Химический элемент
Вещество и тело. Атом и молекула. Свойства веществ. Простые и сложные вещества. Химический элемент Основи молекулярно-кінетичної теорії
Основи молекулярно-кінетичної теорії Углеводороды. Общие знания
Углеводороды. Общие знания Gelation in aqueous solution of L-cysteine and silver nitrate
Gelation in aqueous solution of L-cysteine and silver nitrate Заполни электронные уровни элементов
Заполни электронные уровни элементов Явление аллотропии
Явление аллотропии Исследование структуры продуктов аммонолиза мезопористых магниетермических порошков тантала
Исследование структуры продуктов аммонолиза мезопористых магниетермических порошков тантала Центробежное осаждение
Центробежное осаждение Характеристика кислорода и серы
Характеристика кислорода и серы Актуальные задачи химии
Актуальные задачи химии Металлы - наши друзья или враги
Металлы - наши друзья или враги Получение, свойства и применение алкенов
Получение, свойства и применение алкенов Классификация силикатов
Классификация силикатов Способы получения металлов
Способы получения металлов Фуллерены
Фуллерены 6. Характеристика элементов на основе положения в периодической системе
6. Характеристика элементов на основе положения в периодической системе Природные источники углеводородов
Природные источники углеводородов علاوي الندوة
علاوي الندوة Цезій
Цезій