Слайд 2А1. Число электронов в атоме азота:
1) 7
2) 14
3) 9
4) 12

Слайд 3А2. По своим химическим свойствам галогены, как простые вещества:
1) окислители
2) восстановители
3)

химически инертны
4) не участвуют в процессах окисления-восстановления
Слайд 4А3. В природе в основном галогены находятся:
1) в свободном виде
2) в атмосфере
3)

в соединениях с неметаллами
4) в соединениях с металлами
Слайд 5А4. В какой химической реакции сера является окислителем:
1) SO2 + O2 =

SO3
2) 2H2S + 3О2 = 2SO2 + 2H2O
3) Cu + H2SO4 = CuSO4 + SO2 + H2O
4) H2SO4 = SO3 + H2O
Слайд 6А5. Формула оксида азота высшей степени окисления:
N2O3
N2O
N2O5
NO2

Слайд 7А6. Ион какого металла дает качественную реакцию на хлориды:
барий
калий
серебро
свинец

Слайд 8А7. Степень окисления азота в соединениях NO2 и NH4+ соответственно:
+4 и -3
+3

и -2
+2 и -4
+4 и -2
Слайд 9А8. Реактив, дающий определение в растворе солей аммония:
соляная кислота
сульфат бария
гидроксид натрия
лакмус

Слайд 10А9. В схеме превращений
NO → X → HNO3 , веществом Х

Слайд 11А10. Содержание кислорода и азота в воздухе равно соответственно:
50% и 50%
28% и

71%
21% и 78%
21% и 79%
Слайд 12В1. Закончите схему реакции и расставьте коэффициенты:
1) N2 + H2→
2) NO

+ O2 →
3) NH3 + HCl →
4) NH4Cl + NaOH →
Слайд 13В2. Напишите уравнения реакции в молекулярном, ионном и сокращенном ионном виде:
нитрат серебра

+ соляная кислота
гидроксид калия и сульфат аммония
Слайд 14С1. По вариантам:
На 120 г известняка, содержащего 80% карбоната кальция, подействовали соляной

кислотой. Какой газ выделился и в каком объёме?
К 10% раствору хлорида меди массой 54 г добавили избыток сульфида натрия. Определите массу выпавшего осадка.













 Типы химической связи
Типы химической связи Прикладная геохимия
Прикладная геохимия Чистые вещества и смеси
Чистые вещества и смеси Классификация сложных неорганических веществ. Оксиды
Классификация сложных неорганических веществ. Оксиды Минералы. Сокровища земли. Ко дню геолога
Минералы. Сокровища земли. Ко дню геолога Тест 1 задание
Тест 1 задание Химическое равновесие
Химическое равновесие Презентация на тему Виды химической связи и типы кристаллических решеток
Презентация на тему Виды химической связи и типы кристаллических решеток  Учебное задание Расчет теплоты сгорания
Учебное задание Расчет теплоты сгорания Презентация на тему Полезная химия во фруктах и овощах
Презентация на тему Полезная химия во фруктах и овощах  Донорно-акцепторный механизм образование связи
Донорно-акцепторный механизм образование связи Консультация по химии
Консультация по химии Нефть и продукты ее переработки. Лабораторная работа
Нефть и продукты ее переработки. Лабораторная работа Методы защиты металлов от электрохимической коррозии. Классификация методов защиты
Методы защиты металлов от электрохимической коррозии. Классификация методов защиты Кислотно-основные равновесия
Кислотно-основные равновесия Природный газ
Природный газ Сера
Сера Структура електронної оболонки атома. Енергетичні рівні та підрівні
Структура електронної оболонки атома. Енергетичні рівні та підрівні Генетическая связь между классами неорганических веществ
Генетическая связь между классами неорганических веществ Атомы. Нахождение в природе
Атомы. Нахождение в природе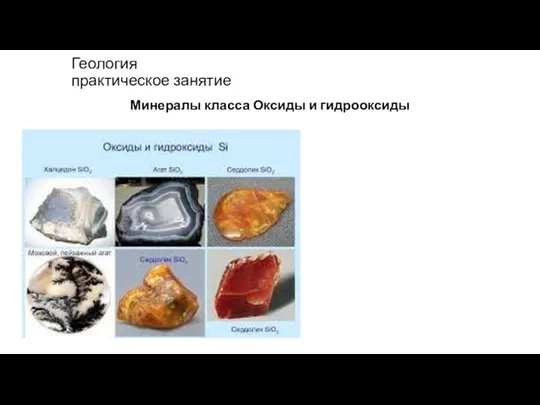 Оксиды и гидрооксиды
Оксиды и гидрооксиды 9-12 Гидролиз солей -
9-12 Гидролиз солей - Презентация на тему Неметаллы
Презентация на тему Неметаллы  Стекло
Стекло Карбоцепные полимеры
Карбоцепные полимеры Полиэтилен. Получение полиэтилена
Полиэтилен. Получение полиэтилена Группа веществ, требующих особых методов изолирования. Характеристика соединений. Токсикологическое значение
Группа веществ, требующих особых методов изолирования. Характеристика соединений. Токсикологическое значение Применение личностно-ориентированного подхода в обучении химии
Применение личностно-ориентированного подхода в обучении химии