Содержание
- 2. Правило октета Обычно химическая связь образуется за счет неспаренных электронов внешнего электронного слоя. Только инертные газы
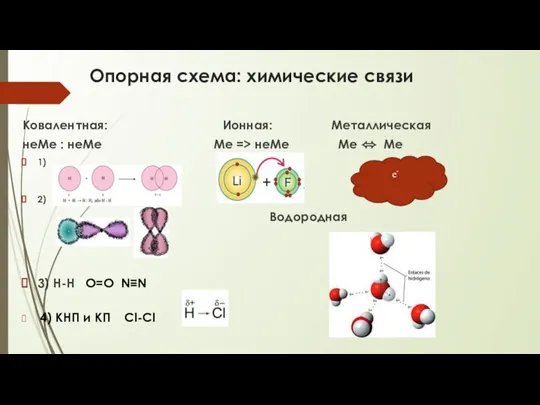
- 3. Опорная схема: химические связи Ковалентная: Ионная: Металлическая неМе : неМе Ме => неМе Ме ⬄ Ме
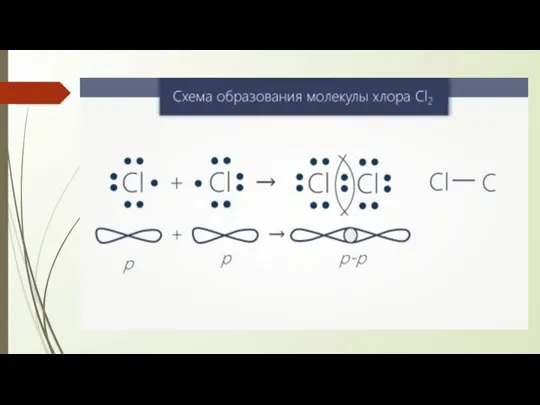
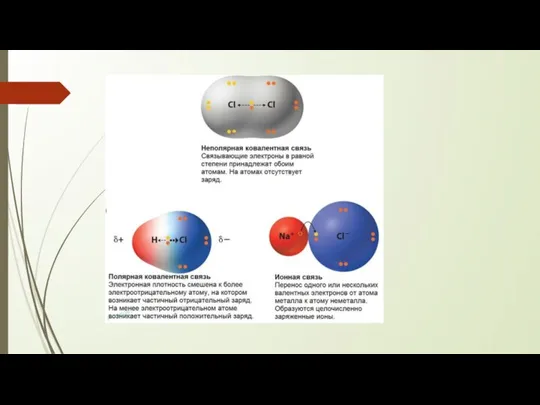
- 4. Ковалентная связь Ковалентная связь образуется между атомами неметаллов. За счет перекрывания электронных облаков между ядрами двух
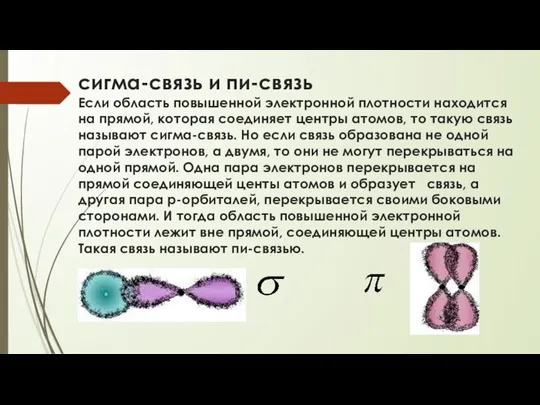
- 6. сигма-связь и пи-связь Если область повышенной электронной плотности находится на прямой, которая соединяет центры атомов, то
- 7. одинарные и кратные связи Связь, образованная одной парой электронов, называется одинарной. Это всегда связь Н-Н или
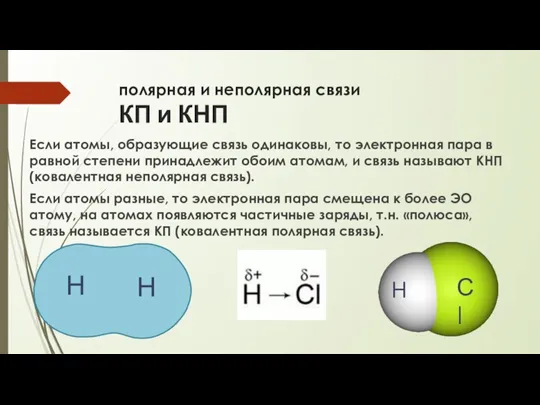
- 8. полярная и неполярная связи КП и КНП Если атомы, образующие связь одинаковы, то электронная пара в
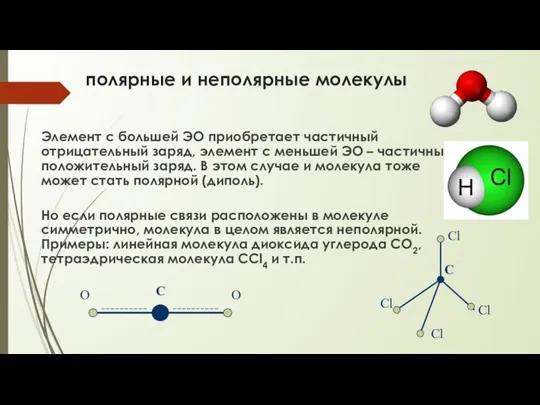
- 9. полярные и неполярные молекулы Элемент с большей ЭО приобретает частичный отрицательный заряд, элемент с меньшей ЭО
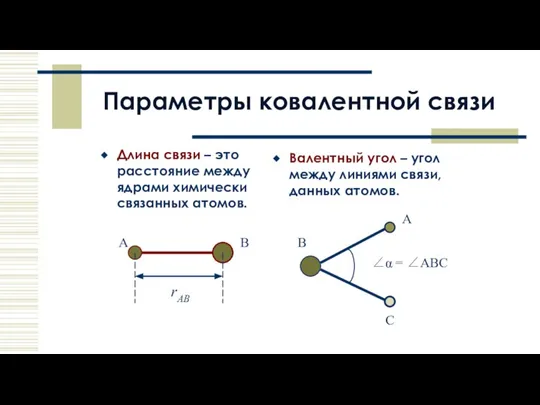
- 10. Параметры ковалентной связи Длина связи – это расстояние между ядрами химически связанных атомов. Валентный угол –
- 11. Энергия ковалентной связи E(AB) – это энергия, необходимая для того, чтобы разорвать связь между атомами A
- 12. Какая ковалентная связь более прочная? 1. или ? 2. одинарная или двойная? 3. полярная или неполярная?
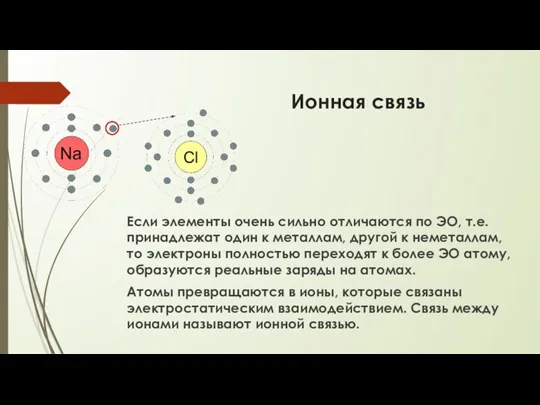
- 13. Ионная связь Если элементы очень сильно отличаются по ЭО, т.е. принадлежат один к металлам, другой к
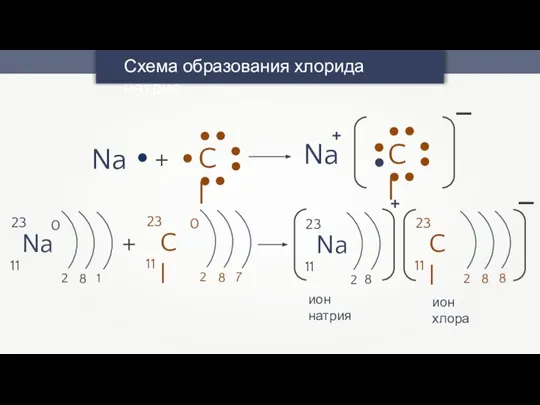
- 14. Схема образования хлорида натрия Na + Cl Na + Cl - 0 11 23 + 0
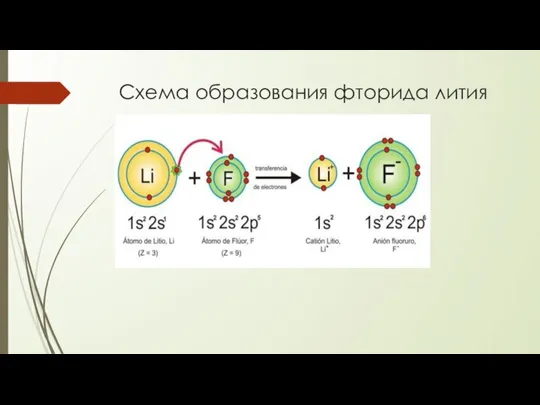
- 15. Схема образования фторида лития
- 16. Свойства ионной связи. Ионная связь – это «суперполярная» связь. Ионная связь менее прочная чем ковалентная. Ионная
- 18. металлическая связь Особенности атомов металлов: — на внешнем энергетическом уровне у них, как правило, находится от
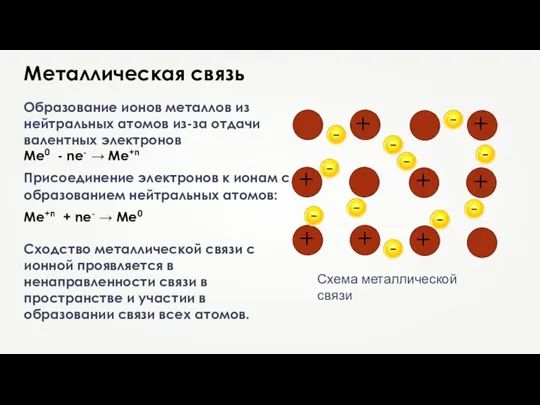
- 19. + + + + + + + + Схема металлической связи Металлическая связь Образование ионов металлов
- 20. +
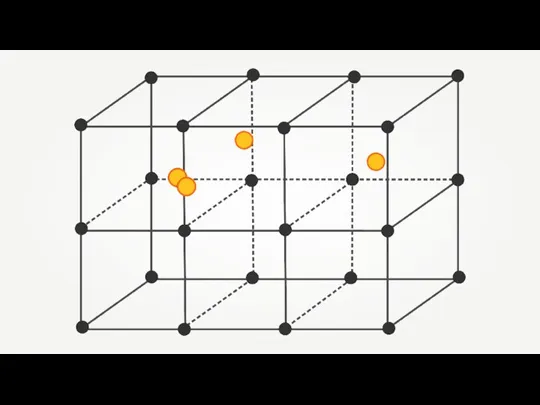
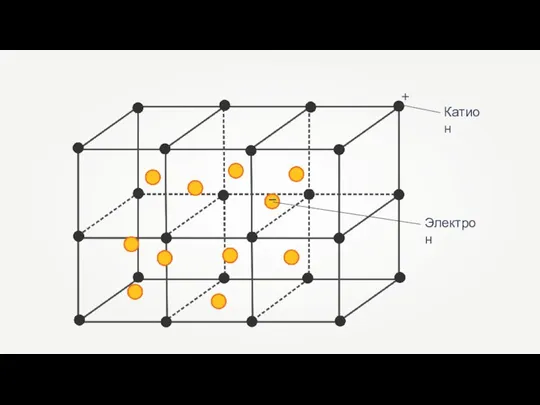
- 21. Структура металлов характеризуется металлической кристаллической решеткой, в узлах которой находятся атом-ионы Катион Электрон + -
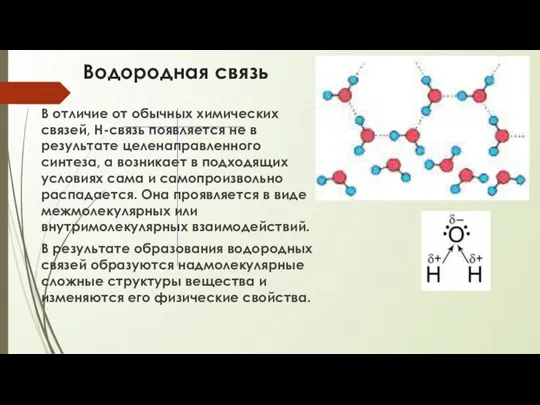
- 22. Водородная связь Водородная связь (Н-связь) – особый тип взаимодействия между атомами, при этом один из них
- 23. Водородная связь В отличие от обычных химических связей, Н-связь появляется не в результате целенаправленного синтеза, а
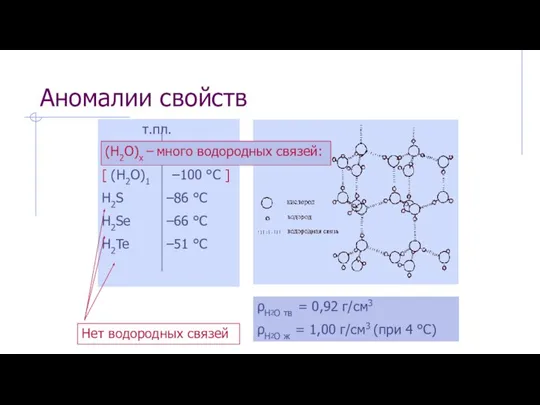
- 24. Аномалии свойств Нет водородных связей (H2O)x – много водородных связей: ρH2O тв = 0,92 г/см3 ρH2O
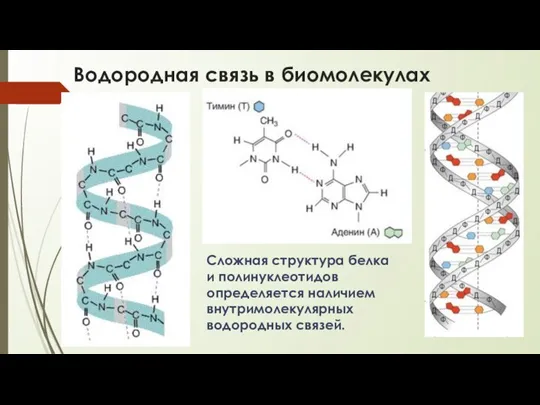
- 25. Водородная связь в биомолекулах Сложная структура белка и полинуклеотидов определяется наличием внутримолекулярных водородных связей.
- 26. Химический диктант 1. Свойства атома притягивать электроны от других атомов, называется… 2. У какого элемента э.о.
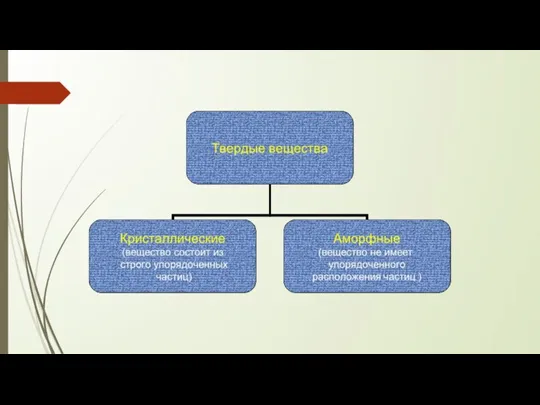
- 28. Кристаллическая решетка — пространственный каркас, образующийся в результате соединения прямыми линиями точек пространства, в которых располагаются
- 29. Определите, имеет ли вещество кристаллическое или аморфное строение Соль поваренная, смола, медный купорос, сода, воск, сахар,
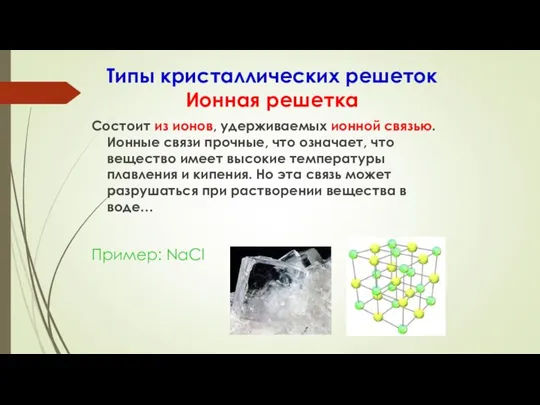
- 30. Типы кристаллических решеток Ионная решетка Состоит из ионов, удерживаемых ионной связью. Ионные связи прочные, что означает,
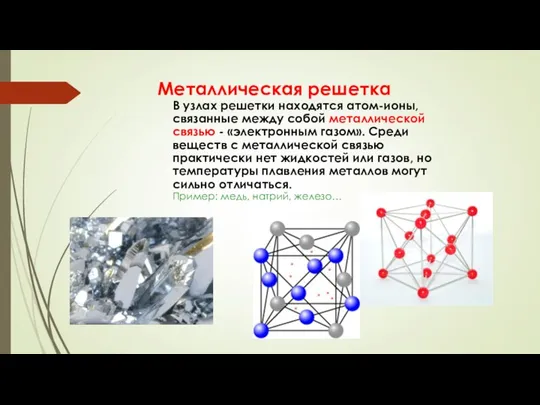
- 31. Металлическая решетка В узлах решетки находятся атом-ионы, связанные между собой металлической связью - «электронным газом». Среди
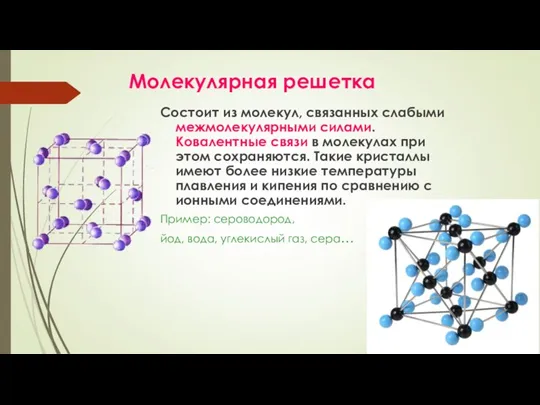
- 32. Молекулярная решетка Состоит из молекул, связанных слабыми межмолекулярными силами. Ковалентные связи в молекулах при этом сохраняются.
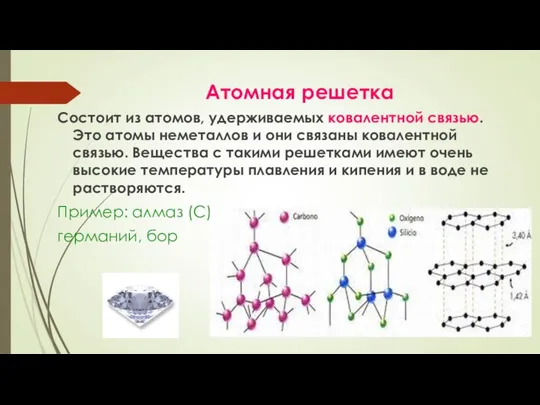
- 33. Атомная решетка Состоит из атомов, удерживаемых ковалентной связью. Это атомы неметаллов и они связаны ковалентной связью.
- 34. Выполните упражнения №1 Распределите вещества на группы, по видам химической связи: O3 , Fe2O3, Cr ,
- 36. Скачать презентацию












 кулонометрия Дастан
кулонометрия Дастан Методы отбора проб воды. Оформление и подготовка к анализу, протокол исследования воды, определение рН
Методы отбора проб воды. Оформление и подготовка к анализу, протокол исследования воды, определение рН Кремнийорганическая гипотеза
Кремнийорганическая гипотеза Известняк. Разновидности известняка. Области применения
Известняк. Разновидности известняка. Области применения Строение атома
Строение атома Галогеноводородные кислоты
Галогеноводородные кислоты Сухой метод определения глюкозы. Глюкометры
Сухой метод определения глюкозы. Глюкометры Современные сплавы на основе циркония
Современные сплавы на основе циркония Комплексное задание по дисциплине основы материаловедения для группы 18
Комплексное задание по дисциплине основы материаловедения для группы 18 Соли
Соли Минералы и горные породы
Минералы и горные породы lektsia_6 (1)
lektsia_6 (1) Подготовка к контрольной работе химические реакции 8 класс
Подготовка к контрольной работе химические реакции 8 класс Азотосодержащие соединения: Амины. Аминокислоты. Белки
Азотосодержащие соединения: Амины. Аминокислоты. Белки Угольная кислота и её соли
Угольная кислота и её соли Комплексные соединения
Комплексные соединения Альдегиды, строение и свойства
Альдегиды, строение и свойства Презентация на тему Алкены. Строение. Изомерия. Химические свойства. Получение
Презентация на тему Алкены. Строение. Изомерия. Химические свойства. Получение  Распределение электронов в атомах
Распределение электронов в атомах Разработка системы подготовки лаборанта химического анализа
Разработка системы подготовки лаборанта химического анализа Пищевые добавки: вред и польза
Пищевые добавки: вред и польза Строение и функции нуклеиновых кислот. Лекция №3
Строение и функции нуклеиновых кислот. Лекция №3 Исследование биодеградации полимерных материалов методом АСМ
Исследование биодеградации полимерных материалов методом АСМ Коррозия металлов
Коррозия металлов Кислород. Физические и химические свойства. Получение
Кислород. Физические и химические свойства. Получение Классификация сложных неорганических веществ. Оксиды
Классификация сложных неорганических веществ. Оксиды Виготовлення водних розчинів з заданою масовою часткою розчиненої речовини
Виготовлення водних розчинів з заданою масовою часткою розчиненої речовини Стелс-материалы
Стелс-материалы