Содержание
- 2. ТЕМА УРОКА: «ОБЩАЯ ХАРАКТЕРИСТИКА НЕМЕТАЛЛОВ»
- 3. НЕМЕТАЛЛЫ - это химические элементы, для атомов которых характерна способность принимать электроны до завершения внешнего уровня.
- 4. 1.НЕМЕТАЛЛЫ Общая характеристика Кислород и кремний составляют 76% от массы земной коры (О – 49%, Si
- 5. НЕМЕТАЛЛЫ Общая характеристика В состав земной атмосферы входят простые и сложные вещества, образованные элементами-неметаллами (N2-75,5%, O2-23,2%,
- 6. 2.РАСПРОСТРАНЕННОСТЬ ХИМИЧЕСКИХ ЭЛЕМЕНТОВ НЕМЕ
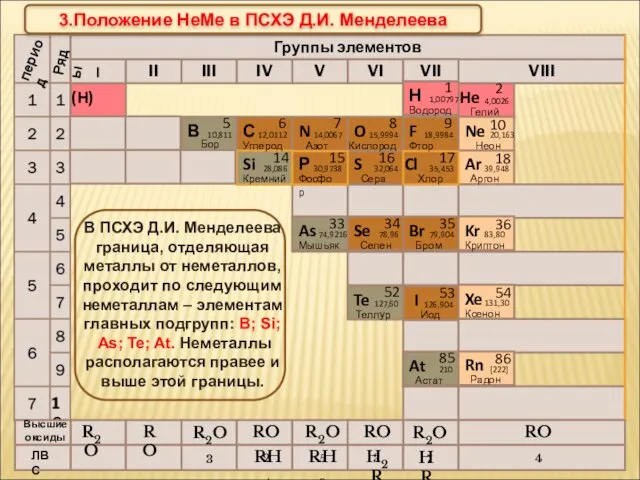
- 7. R2O RO R2O3 RO2 R2O5 RO3 R2O7 RO4 RH4 RH3 H2R HR Высшие оксиды ЛВС 3.Положение
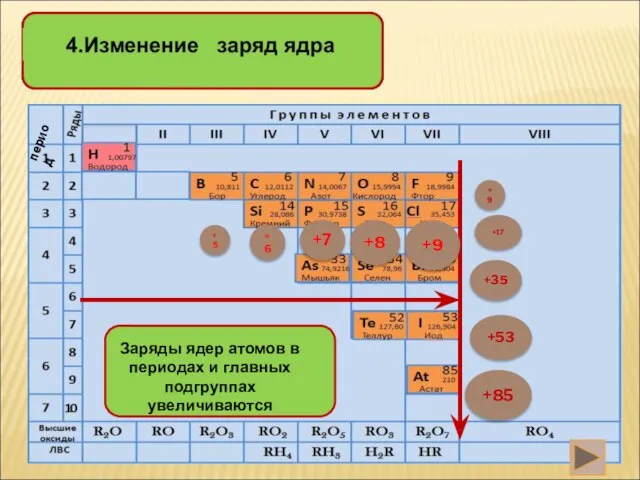
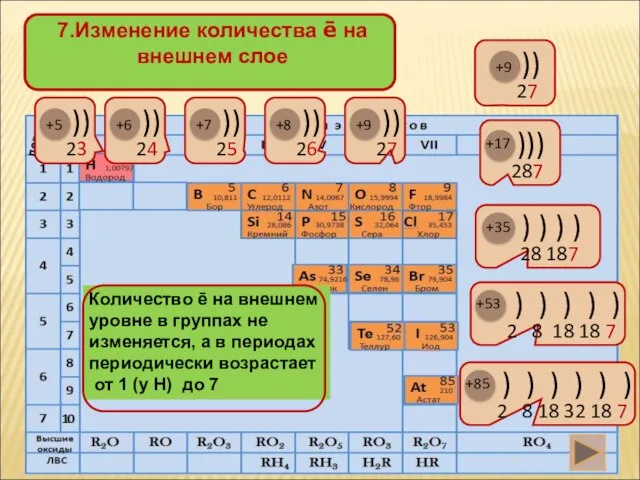
- 8. +5 +6 +7 +8 +9 +85 +17 +9 +53 +35 период
- 9. период
- 10. период
- 11. период
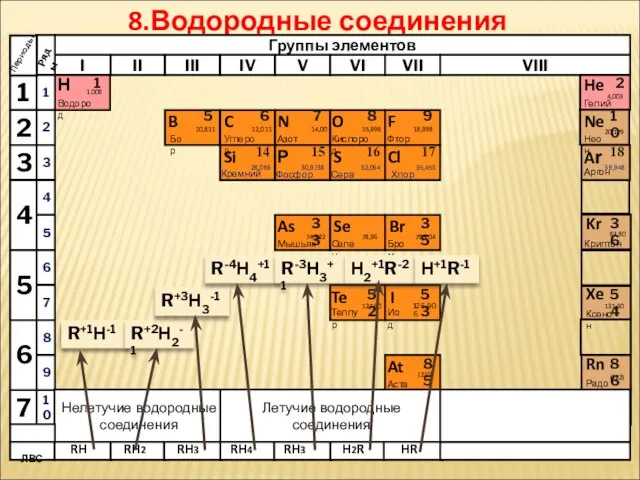
- 12. 8.Водородные соединения НеМе Н Водород 1 1.008 Периоды B C N As He Se Te F
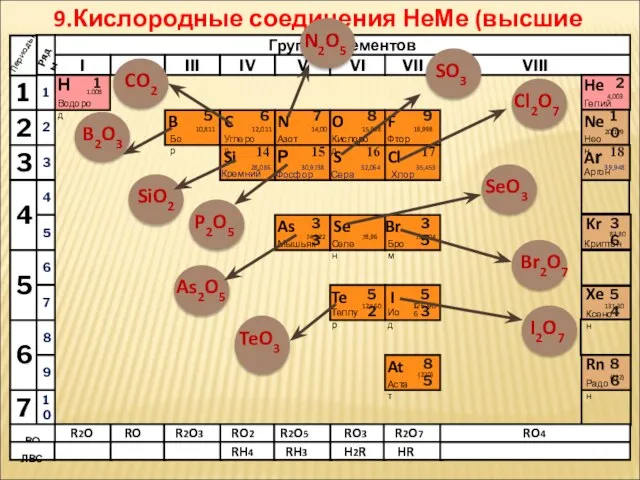
- 13. 9.Кислородные соединения НеМе (высшие оксиды) Н Водород 1 1.008 Периоды B C N As He Se
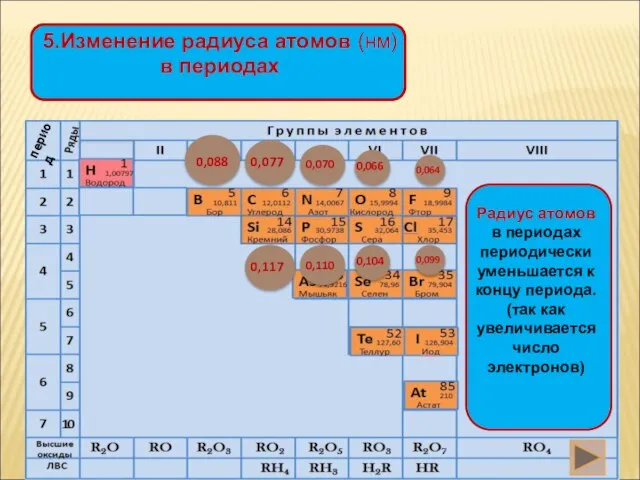
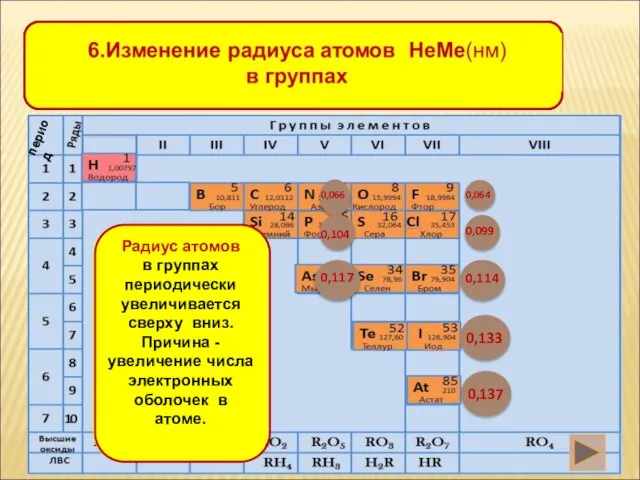
- 14. 10.Выводы: Изменение св-в НеМе в главной подгруппе: 1.число электронов на внешнем слое не изменяется 2.радиус атома
- 15. 1.Назовите распределение е на оболочках у:серы, фтора, хлора , брома S 2 8 6 F 2
- 16. 11.НАХОЖДЕНИЕ НЕМЕТАЛЛОВ В ПРИРОДЕ В свободном виде НеМе могут быть : Газообразные: Фтор-F₂ , хлор-Cl₂ ,
- 17. Ребята, берегите зрение! Ребята, берегите зрение!
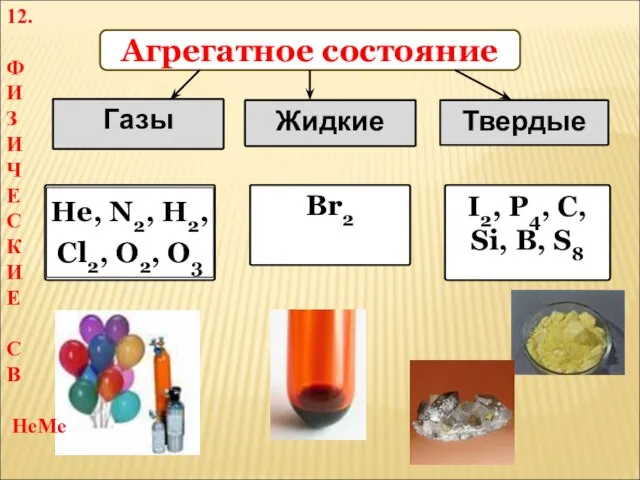
- 18. Агрегатное состояние Газы Жидкие Твердые Br2 I2, P4, C, Si, B, S8 12. Ф И З
- 19. ЦВЕТА НЕМЕТАЛЛОВ БЕЛЫЙ ЧЕРНЫЙ ФОСФОР ФОСФОР ГРАФИТ ЖЕЛТО-ЗЕЛЕНЫЙ ХЛОР
- 20. КРАСНЫЙ ЖЕЛТЫЙ ФИОЛЕТОВЫЙ ФОСФОР СЕРА ЙОД БЕСЦВЕТНЫЙ УГЛЕРОД ЦВЕТА НЕМЕТАЛЛОВ
- 21. Чаще неметаллы находятся в химически связанном виде: вода, минералы, горные породы, различные соли силикаты, фосфаты, сульфиды.
- 22. 1.Какого газа ( по объему) больше всего в атмосфере Земли ? А З О Т А
- 23. Гость из космоса пришел, в воздухе приют себе нашел ВОДОРОД 2.В доме выше всех живем, вдвоем
- 24. 7.Прокаленный уголек дышать пожарнику помог. АКТИВИРОВАННЫЙ УГОЛЬ 8.Белый воздуха боится, покраснел чтоб сохраниться. БЕЛЫЙ И КРАСНЫЙ
- 25. 14.ХИМИЧЕСКИЕ СВОЙСТВА НЕМЕТАЛЛОВ Окислительные свойства простых веществ неметаллов: 1. Реагируют с металлами 2K + S⁰ =
- 26. Самостоятельная работа 1.Допишите уравнения реакций : Na + Br₂ → ? Mg + P → ?
- 27. Самостоятельная работа 2.Допишите уравнения реакций : Si + F₂→ H₂ + WO₃ → Li + N₂
- 28. 1.Неметаллы, расположенные в порядке усиления их неметалличности, - это азот, углерод, бор 2) сера, хлор, фтор
- 29. 3. Ковалентная полярная связь образуется в соединении: 1) NaCl 2) 3) P₄ 4) BaCl₂ 15.Т Е
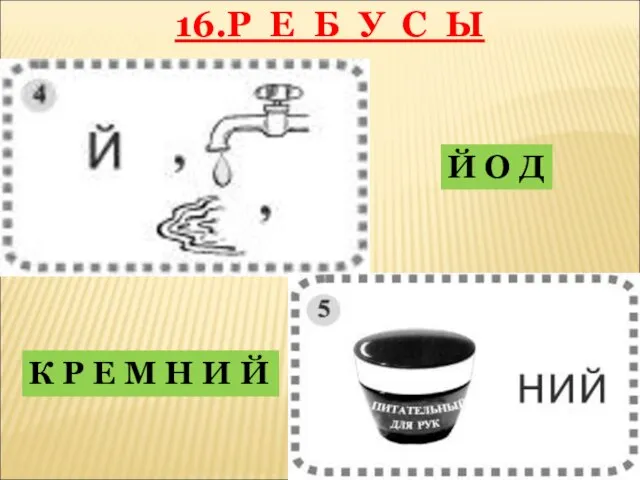
- 30. 16.Р Е Б У С Ы Й О Д К Р Е М Н И Й
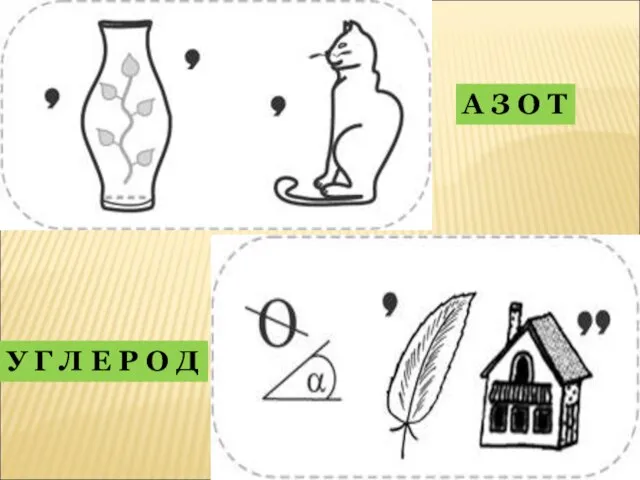
- 31. А З О Т У Г Л Е Р О Д
- 33. Скачать презентацию




















 Применение алкенов
Применение алкенов Кристаллы и минералы
Кристаллы и минералы Презентация по химии на тему _Высокомолекулярные Соединения_ (1)
Презентация по химии на тему _Высокомолекулярные Соединения_ (1) Презентация на тему Коллоидная химия
Презентация на тему Коллоидная химия  Хімічні формули
Хімічні формули Презентация на тему Витамин C
Презентация на тему Витамин C  Полимеры. Получение и применение полимеров
Полимеры. Получение и применение полимеров Материалы космической техники
Материалы космической техники Сера
Сера Презентация по Химии "Соединения алюминия"
Презентация по Химии "Соединения алюминия"  Основания: номенклатура, классификация, применение, физические свойства
Основания: номенклатура, классификация, применение, физические свойства Химический элемент калий
Химический элемент калий Химическая термодинамика. Термодинамические потенциалы
Химическая термодинамика. Термодинамические потенциалы Серная кислота H2SO4
Серная кислота H2SO4 Характеристика элемента по его положению в периодической системе
Характеристика элемента по его положению в периодической системе Ароматические углеводороды
Ароматические углеводороды Соли
Соли Масс-спектрометрия – аналитический метод определения молекулярной массы свободных ионов в высоком вакууме
Масс-спектрометрия – аналитический метод определения молекулярной массы свободных ионов в высоком вакууме Валентность химических элементов
Валентность химических элементов Презентация на тему Химические свойства алкенов
Презентация на тему Химические свойства алкенов  proekt_TTU_3_1
proekt_TTU_3_1 Полиморфизм кристаллов изатина
Полиморфизм кристаллов изатина Химия в быту
Химия в быту Количество вещества. Моль
Количество вещества. Моль Презентация на тему Угольная и кремниевая кислоты и их соли
Презентация на тему Угольная и кремниевая кислоты и их соли  Классификация методов переработки пластмасс
Классификация методов переработки пластмасс Презентация на тему Химические реакции
Презентация на тему Химические реакции  Сера. Физические и химические свойства. Нахождение в природе
Сера. Физические и химические свойства. Нахождение в природе