Содержание
- 2. Химический диктант Валентность – это ……. Валентные электроны – это Высшая валентность по кислороду равна ………..
- 3. 6. Коэффициент показывает …… 7. Индекс показывает ………… 8. Качественный состав вещества показывает……. 9. Количественный состав
- 4. Составьте формулу оксида хлора (III). Рассчитайте W (О) в этом веществе.
- 5. ЗАДАЧА Как атомы соединяются в молекулы?
- 6. Электроотрицательность – Значение электроотрицательности химических элементов второго периода это способность атомов элемента притягивать к себе электроны,
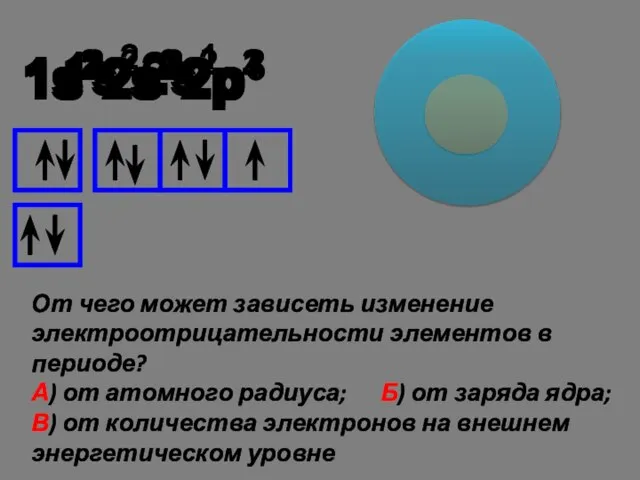
- 7. 1s22s1 1s22s2 1s22s22p1 1s22s22p3 1s22s22p4 1s22s22p5 1s22s22p2 От чего может зависеть изменение электроотрицательности элементов в периоде?
- 8. Нарисуйте электронные конфигурации атомов элементов главной подгруппы I группы +1)1 +3)2)1 +11)2)8)1 +19)2)8)8)1 +37)2)8)18)8)1 +55)2)8)18)18)8)1 Как
- 9. 1.Обозначьте с помощью знака >, какой из двух элементов обладает большим значением электроотрицательности. Mg Ca Na
- 10. ХИМИЧЕСКАЯ СВЯЗЬ - ЭТО СИЛЫ ВЗАИМОДЕЙСТВИЯ, КОТОРЫЕ СОЕДИНЯЮТ ОТДЕЛЬНЫЕ АТОМЫ В МОЛЕКУЛЫ, ИОНЫ, КРИСТАЛЛЫ.
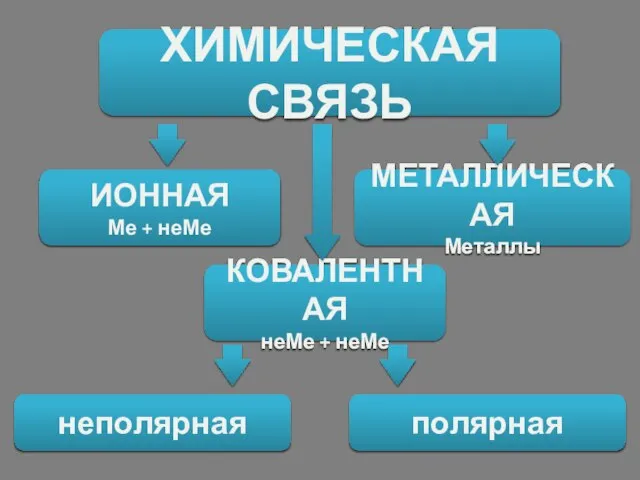
- 11. ХИМИЧЕСКАЯ СВЯЗЬ КОВАЛЕНТНАЯ неМе + неМе ИОННАЯ Ме + неМе МЕТАЛЛИЧЕСКАЯ Металлы неполярная полярная
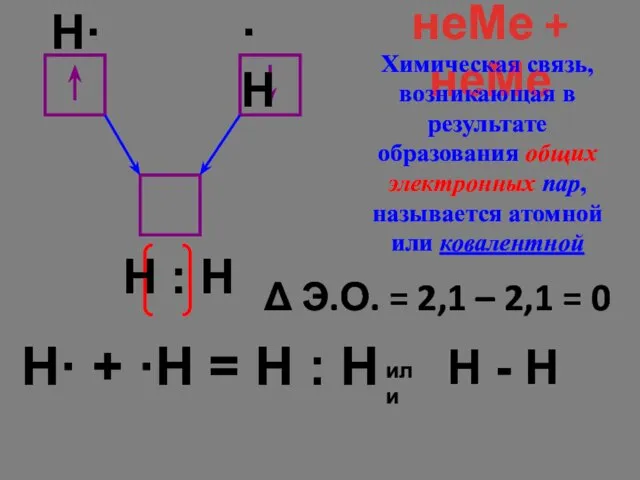
- 12. H· + ·Н = Н : Н Δ Э.О. = 2,1 – 2,1 = 0 неМе
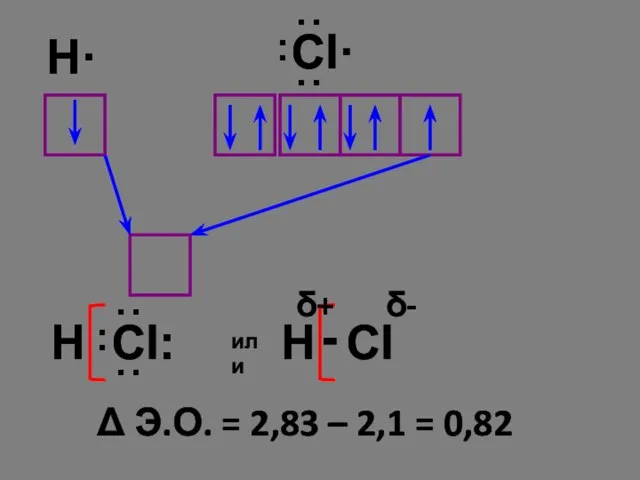
- 13. H· Δ Э.О. = 2,83 – 2,1 = 0,82
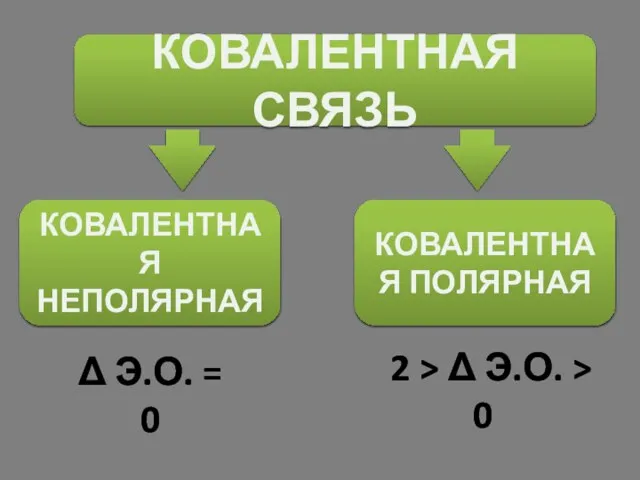
- 14. КОВАЛЕНТНАЯ СВЯЗЬ КОВАЛЕНТНАЯ НЕПОЛЯРНАЯ КОВАЛЕНТНАЯ ПОЛЯРНАЯ Δ Э.О. = 0 2 > Δ Э.О. > 0
- 15. Какой тип связи в молекулах веществ? H2 H2O NH3 Cl2 H2S Напишите электронные формулы этих веществ.
- 16. Составьте электронную схему строения атома серы. Подчеркните валентные электроны и обозначьте их точками вокруг символа элемента.
- 18. Скачать презентацию










 Эмульсия. Основные типы эмульсий
Эмульсия. Основные типы эмульсий Квантовая химия
Квантовая химия Алкены Бутен
Алкены Бутен Металлы
Металлы Химический диктант по органической химии. 9 класс
Химический диктант по органической химии. 9 класс Химические реакции. Классификация
Химические реакции. Классификация Знакомство с химией
Знакомство с химией Применение каучука
Применение каучука Неорганический мозговой штурм
Неорганический мозговой штурм Практическая работа: Очистка загрязнённой поваренной соли
Практическая работа: Очистка загрязнённой поваренной соли Буферные системы
Буферные системы Cеминар 6 -Алканы-2
Cеминар 6 -Алканы-2 Химические реакции
Химические реакции Электроосмос. Практическое применение электроосмоса
Электроосмос. Практическое применение электроосмоса Магматические горные породы
Магматические горные породы 1_
1_ Физические и химические свойства металлов
Физические и химические свойства металлов Строение электронных оболочек атома
Строение электронных оболочек атома Железо
Железо Производные салициловой, пара-аминобензойной кислот, применяемые в медицине
Производные салициловой, пара-аминобензойной кислот, применяемые в медицине коррозия металлов
коррозия металлов Индикаторная бумага
Индикаторная бумага Тренажер - Валентность. 8 класс
Тренажер - Валентность. 8 класс Потенциометрический анализ, титрование
Потенциометрический анализ, титрование Алкины
Алкины Лучший тест для подготовки к ЕГЭ по химии
Лучший тест для подготовки к ЕГЭ по химии Тривиальные названия веществ, наиболее часто встречаемых в ЕГЭ
Тривиальные названия веществ, наиболее часто встречаемых в ЕГЭ Блок колонн на установке замедленного коксования производительностью 730000 тонн/год гудрона (поз.к-1, кх-1)
Блок колонн на установке замедленного коксования производительностью 730000 тонн/год гудрона (поз.к-1, кх-1)