Слайд 11Атомно-молекулярная теория
Автор этой теории английский химик Джон Дальтон. Его атомистическая теория, опубликованная

в 1803-1807 годах, прочно основывалась на экспериментальных данных.
Ее основные постулаты заключались в следующем:
Каждый химический элемент состоит из чрезвычайно мелких частиц, называемых атомами;
Все атомы одного элемента одинаковы;
Атомы различных элементов обладают разными свойствами (в том числе имеют разные массы);
Атомы одного элемента в результате химических реакций не превращаются в атомы других элементов; атомы не создаются и не разрушаются в химических реакциях;
Химические соединения образуются в результате комбинаций атомов двух или нескольких элементов;
В данном соединении относительные количества атомов различных сортов, а также сорта этих атомов всегда постоянны.
Слайд 13Идею сохранения энергии в химических реакциях экспериментально доказал в 1848 г. немецкий

ученый Роберт Майер, которого и считают первооткрывателем этого закона.
Слайд 15Закон эквивалентов: все вещества реагируют между собой в эквивалентных количествах.

Слайд 32Закон парциальных давлений Дальтона
в смеси газов каждый газ оказывает такое давление (парциальное),

какое оказывал бы он при отсутствии других газов, занимая весь объем смеси при той же температуре, а общее давление смеси равно сумме парциальных давлений ее компонентов:
p = p1+ p2 + p3 + … .




























 Строение вещества. Виды химической связи
Строение вещества. Виды химической связи Решение задач на основные законы и понятия химии
Решение задач на основные законы и понятия химии Спирты и их производные
Спирты и их производные Строение, свойства, биологическая роль дезоксисахаров и аминосахаров
Строение, свойства, биологическая роль дезоксисахаров и аминосахаров Гетерогенные химические системы и поверхностные явления в них
Гетерогенные химические системы и поверхностные явления в них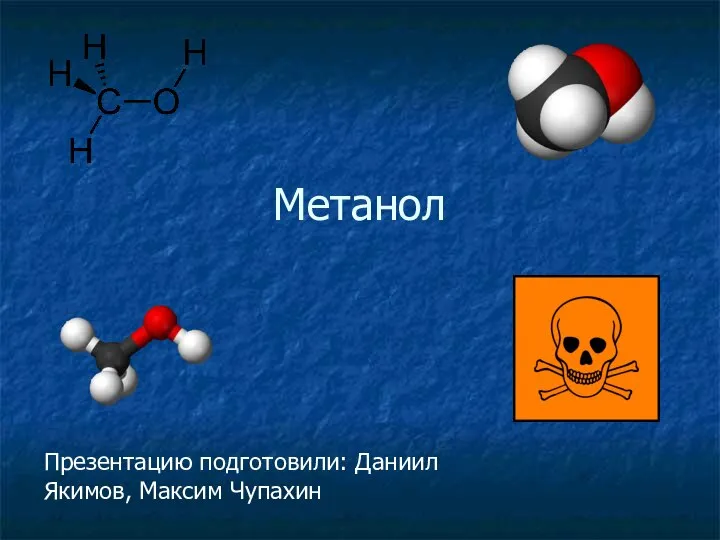 Метанол. Краткая характеристика
Метанол. Краткая характеристика Использование катионных красителей в экстракционно-флуориметрическом анализе
Использование катионных красителей в экстракционно-флуориметрическом анализе Основания. Простые и сложные ионы
Основания. Простые и сложные ионы Строение и химические свойства галогенов
Строение и химические свойства галогенов Методы пробоотбора и пробоподготовки донных отложений, почв и грунтов
Методы пробоотбора и пробоподготовки донных отложений, почв и грунтов Основные понятия и законы химии
Основные понятия и законы химии Разбор задач
Разбор задач Классы веществ
Классы веществ Предельные углеводороды. Урок №4
Предельные углеводороды. Урок №4 Презентация на тему Природный и попутный газ
Презентация на тему Природный и попутный газ  Лекарственные средства – производные пиримидин 2,4,6-триона
Лекарственные средства – производные пиримидин 2,4,6-триона Условия, замедляющие выход водорастворимых питательных веществ из удобрений на примере аммофоса
Условия, замедляющие выход водорастворимых питательных веществ из удобрений на примере аммофоса Очистка поверхности медного сплава
Очистка поверхности медного сплава Роль М.В. Ломоносова и Дж. Дальтона в создании атомно-молекулярного учения
Роль М.В. Ломоносова и Дж. Дальтона в создании атомно-молекулярного учения Сульфиды
Сульфиды Alkini
Alkini Критерии оценки качества природного газа
Критерии оценки качества природного газа Современные способы защиты ОТТ
Современные способы защиты ОТТ Определение химического эквивалента, эквивалентной и атомной массы металла
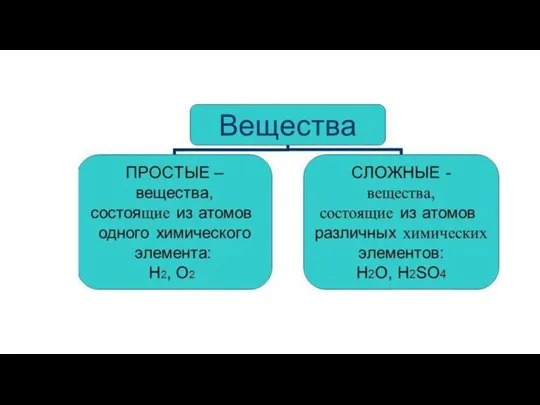
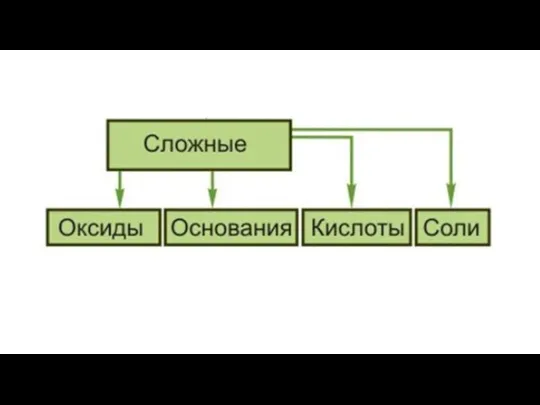
Определение химического эквивалента, эквивалентной и атомной массы металла Простые и сложные вещества. Основные классы неорганических веществ
Простые и сложные вещества. Основные классы неорганических веществ Азотная кислота и ее соли. Специфические свойства азотной кислоты
Азотная кислота и ее соли. Специфические свойства азотной кислоты Интеллектуальная игра по химии Металлы
Интеллектуальная игра по химии Металлы Метод высокоэффективной жидкостной хроматографии и тандемной масс-спектрометрии
Метод высокоэффективной жидкостной хроматографии и тандемной масс-спектрометрии