Содержание
- 2. Оглавление Глава1 – понятие о степени окисления. Глава2 – определение степени окисления. Глава3 – степень окисления
- 3. Степень окисления – это условный заряд атома химического элемента в соединении, вычисленный на основе предположения, что
- 4. Степень окисления простых веществ равна нулю Например: S0, H02, Cl02, O02, Na0. Максимальная (высшая) степень окисления
- 5. Алгебраическая сумма степеней окисления в веществе равна нулю
- 6. Определение степени окисления +6 -2 SO3 +7 -2 Mn2O7 +5 -2 P2O5 +1 -2 Li2O +3
- 7. Алгебраическая сумма степеней окисления в ионе Правило: алгебраическая сумма степеней окисления в сложном ионе равна суммарному
- 8. Zn+2S-2, Ca+23N-32
- 9. Правило креста Правило креста: для составления химических формул по названию вещества надо записать соответствующие знаки химических
- 10. Составление формул по степени окисления Оксид натрия - Хлорид железа (III) - Нитрид магния - Оксид
- 11. Тренировочные задания (подготовка к с/р) Расставьте степени окисления в соединениях и в ионах: MgO Zn KNO3
- 12. Правильные ответы Mg+2O-2 , Zn0
- 13. Хлорид железа(III) – Fe+3Cl3 -1 Оксид серы(VI) – S+6O3-2 Гидрид калия – K+1H-1 Нитрид бария –
- 14. II вариант CaBr2 KClO4 S8 Na2Cr2O7 Li2SO4 MgSiO3 (ClO2)- ,(NO3)- I вариант H2SO3 H4P2O7 ZnF2 BaCO3
- 15. Ответы к проверочной работе I вариант 1 H2+1S+4O3-2 H4+1P2+5O7-2 Zn+2F2-1 Ba+2C+4O3-2 O20 Na2+1S+6O4-2 (P+5O4-2)3- (Mn+7O4-2)- II
- 16. 2. Хлорид магния- MgCl2, Сульфид железа (III)- Fe2S3 Оксид бора - B2O3 Нитрид кальция - Ca3N2
- 18. Скачать презентацию






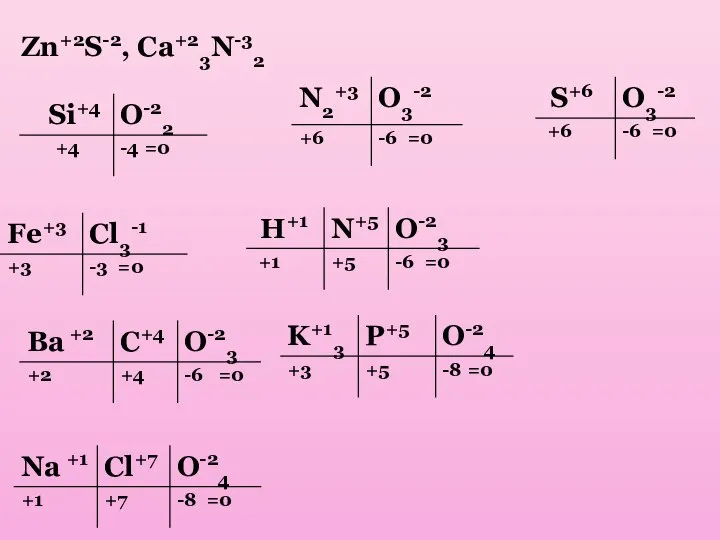








 Органическая химия
Органическая химия Трансляция. Активирование аминокислоты
Трансляция. Активирование аминокислоты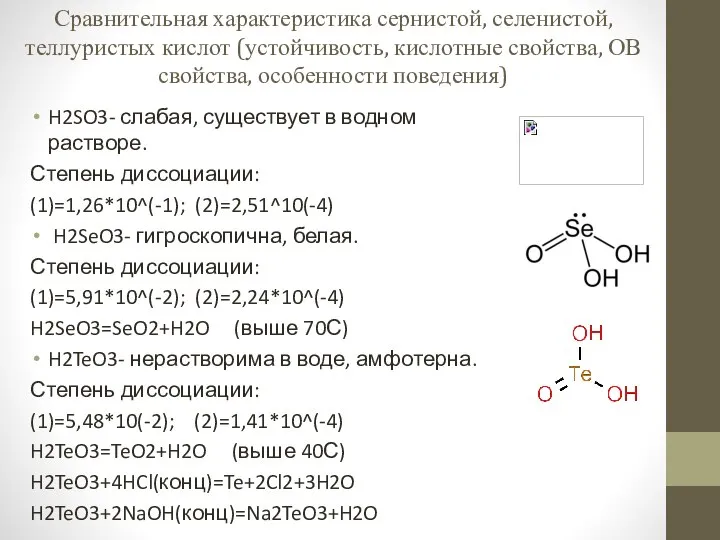 Сравнительная характеристика сернистой, селенистой, теллуристых кислот
Сравнительная характеристика сернистой, селенистой, теллуристых кислот Химические реакции
Химические реакции Кинетика и равновесие. Лекция №3
Кинетика и равновесие. Лекция №3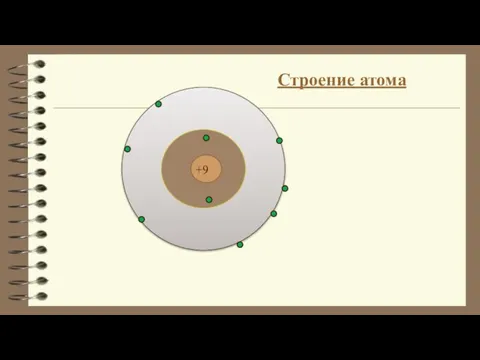 Строение атома
Строение атома Химия элементов
Химия элементов Химик белемнәрне тормышта куллану
Химик белемнәрне тормышта куллану Ацетиленди гидратациялау
Ацетиленди гидратациялау Химический элемент азот N и его соединения
Химический элемент азот N и его соединения Презентация на тему Аллотропные видоизменения неметаллов
Презентация на тему Аллотропные видоизменения неметаллов  Химическая связь
Химическая связь Основы строения и свойства материалов
Основы строения и свойства материалов Влияние бытовой химии на здоровье человека
Влияние бытовой химии на здоровье человека Нуклеиновые кислоты
Нуклеиновые кислоты Про краски
Про краски Углеродистые стали
Углеродистые стали Реакции ионного обмена и условия их протекания
Реакции ионного обмена и условия их протекания Экстракционное разделение радионуклидов
Экстракционное разделение радионуклидов Альдегиды и кетоны
Альдегиды и кетоны Осмотическое давление
Осмотическое давление Степень окисления
Степень окисления Условия среды, вызывающие коррозию металла
Условия среды, вызывающие коррозию металла Физические и химические явления в химии. Признаки химических реакций
Физические и химические явления в химии. Признаки химических реакций Химическая связь. Ковалентная связь
Химическая связь. Ковалентная связь Замедленное коксование гудрона
Замедленное коксование гудрона Структура, свойства и термическая обработка железоуглеродистых сплавов
Структура, свойства и термическая обработка железоуглеродистых сплавов Самородные металлы
Самородные металлы