Слайд 2Общее условие равновесия в гетерогенных системах
Равновесия в гетерогенных системах, в которых

не происходит химического взаимодействия между компонентами, а имеют место лишь фазовые переходы, т. е. процессы перехода компонентов из одной фазы в другую (или в другие), будем называть фазовыми равновесиями.
Компонентом, или составной частью системы называется каждое из содержащихся в ней химически однородных веществ, которое может быть выделено из нее и может существовать в изолированном виде длительное время.
Слайд 4Из какого бы числа компонентов и из какого бы числа фаз ни

состояла гетерогенная система, условием равновесия между фазами в ней: химический потенциал любого данного компонента должен быть одинаковым во всех фазах системы.
Если dG < 0, то μi(а) > μi(β). Следовательно, самопроизвольный переход любого данного компонента i из фазы а в фазу β может происходить только в том случае, если его химический потенциал в фазе а был больше, чем в фазе β. При продолжении процесса эти химические потенциалы будут все больше сближаться, и когда они станут равными, будет достигнуто состояние равновесии между фазами в отношении распределения между ними компонента i.
Слайд 5Равновесные соотношения при фазовых переходах

Слайд 9Уравнение содержит две индивидуальные (т. е. различные для разных веществ) постоянные (ΔH

и С). Если одна из них известна (ΔH испарения), то достаточно знать давление при одной температуре, чтобы определить С и иметь возможность применять уравнение для расчета давлении при других температурах или для расчета температур кипения при различных давлениях.
Возможность приведения какой-нибудь исследуемой зависимости к линейной форме всегда сильно облегчает задачу, так как для определения положения прямой достаточно знать всего две точки (т. е. в данном случае — давления пара при двух температурах). Положение других точек в этом случае определяется интерполяцией или частично экстраполяцией (графическим или аналитическим путем).
Слайд 10Если же ΔH неизвестна, то необходимо знать давления при двух температурах и,

подставив их в уравнение, получить два уравнения с двумя неизвестными (ΔH и С). Последние определяются путем решения системы этих двух уравнений.
Подставляя найденные значения в уравнение, получаем возможность применить его как для определения давлений при заданной температуре, так и для обратного расчета.
Вычисленные значения ΔH часто обладают практически такой же точностью, как получаемые непосредственным измерением теплоты испарения.
Слайд 11Зависимость температур плавления и полиморфного превращения от внешнего давления

Слайд 13Плавление почти всех веществ сопровождается увеличением объема, т. е. ΔV > 0.
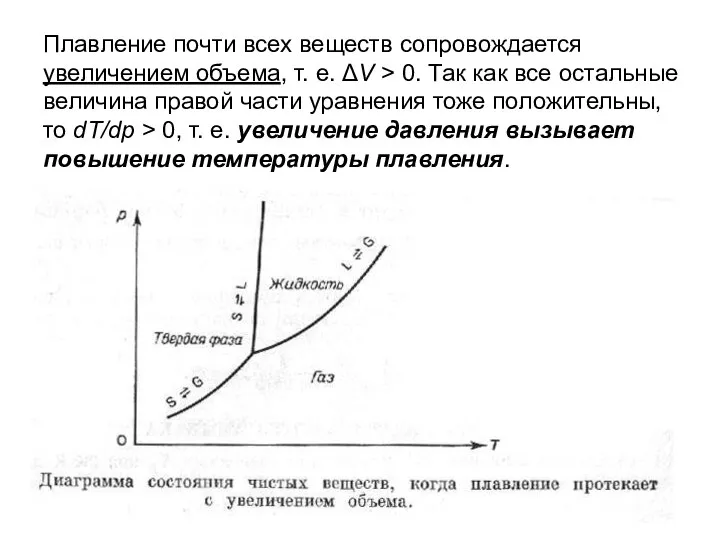
Так как все остальные величина правой части уравнения тоже положительны, то dT/dp > 0, т. е. увеличение давления вызывает повышение температуры плавления.












 Развитие познавательной активности творческих способностей и индивидуализация на уроках химии
Развитие познавательной активности творческих способностей и индивидуализация на уроках химии Углеродистые стали
Углеродистые стали Целестин
Целестин Презентацию выполнила ученица 10 класса Поликарпова Диана 2010 год
Презентацию выполнила ученица 10 класса Поликарпова Диана 2010 год Гальванический элемент
Гальванический элемент Углеводы. Классификация углеводов
Углеводы. Классификация углеводов Степень окисления. Классификация неорганических соединений
Степень окисления. Классификация неорганических соединений Катаболизм пуриновых нуклеотидов
Катаболизм пуриновых нуклеотидов Органическая химия
Органическая химия Соединения азота в атмосфере. Лекция 4
Соединения азота в атмосфере. Лекция 4 Структура к свойства веществ
Структура к свойства веществ Химические вещества парабены
Химические вещества парабены Влияние меди на коррозию низколегиованных сталей
Влияние меди на коррозию низколегиованных сталей Серная кислота
Серная кислота Основные свойства и опасности нефти. Безопасность для танкеров
Основные свойства и опасности нефти. Безопасность для танкеров Окислители в пиросоставах
Окислители в пиросоставах Вода. Строение молекулы. Водородная связь. Физические и химические свойства
Вода. Строение молекулы. Водородная связь. Физические и химические свойства Презентация на тему Гидролиз
Презентация на тему Гидролиз  Электролиз
Электролиз Презентация на тему Глюкоза (10 класс)
Презентация на тему Глюкоза (10 класс)  Основания и их свойства
Основания и их свойства Презентация на тему Многоатомные спирты
Презентация на тему Многоатомные спирты  Жидкое состояние вещества
Жидкое состояние вещества Поделочный камень родонит
Поделочный камень родонит Фосфор. Аллотропия фосфора. Физические и химические свойства фосфора
Фосфор. Аллотропия фосфора. Физические и химические свойства фосфора Кремний и 4 группа. 9 класс
Кремний и 4 группа. 9 класс Получение металлов
Получение металлов Степени окисления
Степени окисления