Содержание
- 2. Написать уравнения реакций взаимодействия между веществами а) Li, Na, Ca, Fe c O2, Cl2, S, N2,
- 3. Цель урока: познакомиться с природными соединениями металлов и с самородными металлами; дать понятие о рудах и
- 4. Металлы в природе встречаются в трёх формах: В свободном виде В самородном виде и в виде
- 5. Золото бывает в распыленном состоянии, а иногда собирается в большие массы самородки Так в Австралии в
- 6. Самый большой самородок в мире «Плита Хольтермана» - был найден в 1872 году в австралийском посёлке
- 7. "Желанный незнакомец» 71 кг
- 8. Самородок «Рука судьбы», 27,2 кг.
- 9. Самородки золота имеют вес более 1 г. Самый крупный российский самородок «Большой треугольник» весит более 36
- 10. Крупные самородки имеют собственные названия
- 11. В середине XVII века в Колумбии испанцы, промывая золото, находили вместе с ним тяжелый серебристый металл.
- 12. Его считали случайной вредной примесью или преднамеренной подделкой драгоценного золота. Она получила такие нелестные прозвища, как
- 13. В 1735 году испанский король издаёт указ, повелевающий платину впредь в Испанию не ввозить. При разработке
- 14. Месторождения платины находятся и на Урале.
- 15. В самородном виде и в форме соединений могут находиться в природе Серебро Ртуть Медь Олово
- 16. Все металлы, которые в ряду напряжений находятся до олова, встречаются только в виде соединений Хлоридов: Сильвинит
- 17. Нитратов: Чилийская селитра NaNO3
- 18. Сульфатов: Глауберова соль Na2SO4 * 10 H2O Гипс CaSO4 • 2Н2О
- 19. Карбонатов: Доломит CaCO3 • MgCO3 Магнезит MgCO3 Мел, мрамор, известняк СаСО3
- 20. Сульфидов: Серный колчедан FeS2 Киноварь HgS Цинковая обманка ZnS
- 21. Фосфатов: Фосфориты, апатиты Ca3(PO4)2
- 22. Оксидов: Магнитный железняк Fe3O4 Красный железняк Fe2O3 Бурый железняк Fe2O3 • Н2О
- 23. Металлургия – это отрасль промышленности, которая занимается получением металлов из руд.
- 24. Получение металлов из руд их восстановлением. Восстановители: Пирометаллургия
- 25. Алюмотермия
- 26. Получение металлов восстановлением из растворов солей: Гидрометаллургия
- 27. Получение металлов электролизом: Электрометаллургия
- 28. Напишите уравнения реакций: Fe2O3 + Al = Fe2O3 + H2 = Fe2O3 + CO =
- 30. Скачать презентацию



























 Нуклеиновые кислоты
Нуклеиновые кислоты Золото
Золото Азот N2
Азот N2 Получение алканов
Получение алканов Изомерия. Виды изомерии
Изомерия. Виды изомерии Кальций и его соединения. 9 класс
Кальций и его соединения. 9 класс Сульфиты. Виды сульфидов
Сульфиты. Виды сульфидов Кремний и его соединения
Кремний и его соединения Презентация на тему День Земли, Воды и Чистого воздуха
Презентация на тему День Земли, Воды и Чистого воздуха  rastvory_-_kopia
rastvory_-_kopia Введение в дисциплину Процессы и аппараты химической технологии
Введение в дисциплину Процессы и аппараты химической технологии Окислительно – восстановительные реакции ОВР (9 класс)
Окислительно – восстановительные реакции ОВР (9 класс) Мило. Вищі карбонові кислоти
Мило. Вищі карбонові кислоти Свойства бензола
Свойства бензола Строение атома. Ядро и электронная оболочка
Строение атома. Ядро и электронная оболочка Презентация на тему Способы получения металлов
Презентация на тему Способы получения металлов  Очистка поваренной соли методом кристаллизации в домашних условиях
Очистка поваренной соли методом кристаллизации в домашних условиях Понятие о скорости химической реакции
Понятие о скорости химической реакции Характеристика щелочных металлов (9 класс)
Характеристика щелочных металлов (9 класс) Презентация на тему Природные источники углеводородов и их переработка
Презентация на тему Природные источники углеводородов и их переработка  Алкадиены
Алкадиены Методы выделения и разделения радионуклидов
Методы выделения и разделения радионуклидов Степень окисления
Степень окисления Никель
Никель Химические методы. Золь-гель метод
Химические методы. Золь-гель метод Оксосоединения. Альдегиды и кетоны
Оксосоединения. Альдегиды и кетоны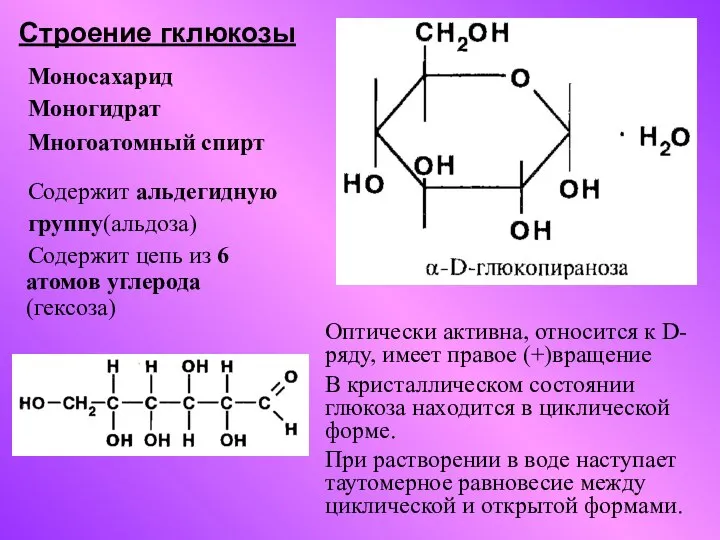 Строение гклюкозы
Строение гклюкозы Азотистые основания. Нуклеотиды и нуклеозиды. ДНК и РНК
Азотистые основания. Нуклеотиды и нуклеозиды. ДНК и РНК