Слайд 2НОМЕНКЛАТУРА
Пропиловый спирт (пропан-1-ол, 1-пропанол) — СН3-СН2-СН2-ОН — относится к простейшим первичным одноатомным

спиртам
Изомер 1-пропанола — изопропиловый спирт (пропан-2-ол, 2-пропанол) — СН3-CH(OH)СН3 — простейший вторичный одноатомный спирт
Слайд 3ФИЗИЧЕСКИЕ СВОЙСТВА
Представляет собой бесцветную жидкость со слабым запахом, легко воспламеняется
Растворим в этаноле,

диэтиловом эфире, ацетоне, бензоле и других органических растворителях.
Хорошо растворяет многие органические вещества
Безводный (абсолютный) спирт кипит при 97,4oС
Получаемый в промышленности спирт-ректификат представляет собой азеотропную смесь 71,8% этанола и 28,1% воды, которая кипит при 87,5-88,0oС
Слайд 4ФИЗИЧЕСКИЕ СВОЙСТВА
Бесцветная легкоподвижная жидкость с характерным запахом и жгучим вкусом
Сμ (25 °С) 2,45

Дж/(моль·К)
∆Hoкип 749,01 кДж/моль
∆Hoпл 89,43 кДж/моль
∆Hoсгор -33,57 кДж/г
∆Hoобр -5071,4 кДж/моль
So298 192.8 Дж/(моль·К)
Слайд 5НАХОЖДЕНИЕ В ПРИРОДЕ
Встречается в природе в небольших количествах как продукт ферментации. Также

он является компонентом сивушного масла.
Слайд 6ПРОПИЛОВЫЙ СПИРТ
Химические свойства

Слайд 7ДЛЯ 1-ПРОПАНОЛА ВОЗМОЖНЫ РЕАКЦИИ, ПРОТЕКАЮЩИЕ С УЧАСТИЕМ:
— атома водорода гидроксильной группы;
— гидроксильной

группы;
— атома водорода гидроксильной группы и связи Cα-H;
— гидроксильной группы и связи Cβ-H.
Слайд 8ТАКИМ ОБРАЗОМ, ВСЕ ХИМИЧЕСКИЕ ПРЕВРАЩЕНИЯ, ХАРАКТЕРНЫЕ ДЛЯ ПРОПИЛОВОГО СПИРТА СОПРОВОЖДАЮТСЯ РАСЩЕПЛЕНИЕМ СВЯЗЕЙ:
1)

O-H
— взаимодействие с активными металлами
2C3H7OH + 2Na → 2C3H7ONa + H2↑.
— взаимодействие с органическими и кислородсодержашими неорганическими кислотами
C3H7OH + CH3COOH ↔C3H7-O-C(O)-CH3 + H2O (H2SO4 (conc), t0);
C3H7OH + HONO2↔C3H7ONO2 + H2O (H2SO4 (conc), t0).
Слайд 9ТАКИМ ОБРАЗОМ, ВСЕ ХИМИЧЕСКИЕ ПРЕВРАЩЕНИЯ, ХАРАКТЕРНЫЕ ДЛЯ ПРОПИЛОВОГО СПИРТА СОПРОВОЖДАЮТСЯ РАСЩЕПЛЕНИЕМ СВЯЗЕЙ:
2)

C-OH;
— взаимодействие с галогеноводородами
C3H7OH + HCl→ C3H7Cl + H2O (ZnCl2, t0).
— взаимодействие с тригалогенидамифосфора
3C3H7OH + PCl3→ 3C3H7Cl + H3PO3.
— взаимодействие с аммиаком
C3H7OH + NH3→ C3H7NH2 + H2O (Al2O3, t0).
Слайд 10ТАКИМ ОБРАЗОМ, ВСЕ ХИМИЧЕСКИЕ ПРЕВРАЩЕНИЯ, ХАРАКТЕРНЫЕ ДЛЯ ПРОПИЛОВОГО СПИРТА СОПРОВОЖДАЮТСЯ РАСЩЕПЛЕНИЕМ СВЯЗЕЙ:
3)

O-H и Cα-H;
— дегидрирование
CH3-CH2-CH2-OH → CH3-CH2-C(O)H + H2↑ (kat = Cu, t0).
— окисление
CH3-CH2-CH2-OH + 2[O] → CH3-CH2-COOH + H2O (kat, t0).
Слайд 11ТАКИМ ОБРАЗОМ, ВСЕ ХИМИЧЕСКИЕ ПРЕВРАЩЕНИЯ, ХАРАКТЕРНЫЕ ДЛЯ ПРОПИЛОВОГО СПИРТА СОПРОВОЖДАЮТСЯ РАСЩЕПЛЕНИЕМ СВЯЗЕЙ:
4)

C-OH и Cβ-H
— внутримолекулярная дегидратация
CH3-CH2-CH2-OH → CH3-CH=CH2 + H2O (Al2O3, t0).
Слайд 12ПРОПИЛОВЫЙ СПИРТ
Общие методы получения

Слайд 13ПОЛУЧЕНИЕ
В промышленности 1-пропанол получают путём гидроформилирования этилена с последующим гидрированием образовавшегося пропаналя:
C2H4

+ CO + H2 → CH3-CH2-CHO
CH3-CH2-CHO + H2 → CH3-CH2-CH2-OH
1-Пропанол получается в качестве побочного продукта при сбраживании зерна на этанол, но этот способ получения не имеет особого промышленного значения.
Слайд 14ПРОПИЛОВЫЙ СПИРТ
Лабораторные методы получения

Слайд 15ЛАБОРАТОРНЫЙ СПОСОБ
Взаимодействие галогенопроизводных со щелочью (гидролиз галогеналканов):
С3H7-Cl + NaOH → С3H7-ОН +

NaCl
Синтез из альдегидов при помощи реактива Гриньяра:
HCOH+C2H5MgCl → С2H5-CН2-O-MgCl
С2H5-CН2-O-MgCl + H2O → С3H7-ОН
Слайд 16ПРОПИЛОВЫЙ СПИРТ
Физико-химические методы исследования

Слайд 17ФИЗИКО-ХИМИЧЕСКИЕ МЕТОДЫ ИССЛЕДОВАНИЯ
Титриметрические методы
Фотометрические методы
Метод тонкослойной хроматографии
Метод масс-спектрометрии
Метод газожидкостной хроматографии
Метод хромато-масс-спектрометрии
Радиоуглеродный анализ

Слайд 18ПРОПИЛОВЫЙ СПИРТ
Методы идентификации

Слайд 19МЕТОДЫ ИДЕНТИФИКАЦИИ
(КАЧЕСТВЕННЫЕ РЕАКЦИИ)
Проба Лукаса заключается в действии на спирт смеси соляной кислоты

и хлорида цинка. При этом происходит образование алкилхлорида, который сначала образует эмульсию со спиртом, а затем отслаивается в виде второй фазы. Проба позволяет различить спирты с разным строением углеродной цепи: третичные спирты реагируют практически мгновенно, вторичные — примерно через 5 минут, а первичные реагируют очень медленно.
Слайд 20МЕТОДЫ ИДЕНТИФИКАЦИИ
(КАЧЕСТВЕННЫЕ РЕАКЦИИ)
Спирты можно отличить от алкенов и алкинов — и в

действительности от почти любого другого класса соединений по их окислению хромовым ангидридом в водном растворе серной кислоты: в течение двух секунд прозрачный оранжевый раствор становится голубовато-зеленым и мутнеет. Третичные спирты не дают этой реакции
Слайд 21МЕТОДЫ ИДЕНТИФИКАЦИИ
(КАЧЕСТВЕННЫЕ РЕАКЦИИ)
Наличие в молекуле ОН-группы часто обнаруживают по образованию сложного эфира

при действии хлористого ацетила или ангидрида. Некоторые сложные эфиры имеют приятный запах; другие представляют собой твердые вещества с четкими температурами плавления, и их можно использовать в качестве производных для идентификации.
Слайд 22МЕТОДЫ ИДЕНТИФИКАЦИИ
(КАЧЕСТВЕННЫЕ РЕАКЦИИ)
Проба Мейера позволяет дифференцировать первичные, вторичные и третичные спирты по

реакции получаемых из них нитропроизводных с азотистой кислотой. На первой стадии спирты превращают в галогенопроизводные, а затем — в нитроалканы. При взаимодействии нитросоединений с HNO2 раствор приобретает красную окраску при подщелачивании, если исходный спирт был первичным; раствор в хлороформе становится синим, если спирт был вторичным. Третичные спирты дают отрицательную реакцию (бесцветный раствор).
Слайд 24ПРИМЕНЕНИЕ
1-Пропанол применяют в качестве растворителя для восков, полиамидных чернил, природных и синтетических

смол, полиакрилонитрила; в производстве полиэтилена низкого давления; для получения карбометоксицеллюлозы; как обезжириватель металлов; сорастворитель поливинилхлоридных адгезивов; желатинирующий и пластифицирующий агент целлюлозноацетатных плёнок; алкилирующий агент. Его используют также для синтеза пропионовой кислоты, пропионового альдегида, пропилацетата, пропиламина, ПАВ, пестицидов, некоторых фармацевтических препаратов.
Слайд 25ПРОПИЛОВЫЙ СПИРТ
Список использованной литературы

























 Строение атома
Строение атома Углеводороды. Урок-игра
Углеводороды. Урок-игра Проектная работа Кристаллизация
Проектная работа Кристаллизация Стеариновая кислота
Стеариновая кислота Лекция 6 Смазочные масла
Лекция 6 Смазочные масла Презентация по Химии "Фосфор - элемент жизни и мысли"
Презентация по Химии "Фосфор - элемент жизни и мысли"  Бериллий, магний и щелочно-земельные металлы
Бериллий, магний и щелочно-земельные металлы Жаңа синтетикалық есірткілер
Жаңа синтетикалық есірткілер Технологии получения и преобразования текстильных материалов. Синтетические волокна (9 класс)
Технологии получения и преобразования текстильных материалов. Синтетические волокна (9 класс) Набор для выращивания монокристалла. Защита проекта
Набор для выращивания монокристалла. Защита проекта Неметаллы. Агрегатные состояния неметаллов
Неметаллы. Агрегатные состояния неметаллов Аммиак. Свойства (9 класс)
Аммиак. Свойства (9 класс) Чистые вещества и смеси, их разделение
Чистые вещества и смеси, их разделение Основные понятия органической химии
Основные понятия органической химии Первое начало термодинамики (Закон сохранения и превращения энергии)
Первое начало термодинамики (Закон сохранения и превращения энергии) Химический процесс: энергетика и равновесие
Химический процесс: энергетика и равновесие Электролиз растворов и расплавов неорганических и органических электролитов
Электролиз растворов и расплавов неорганических и органических электролитов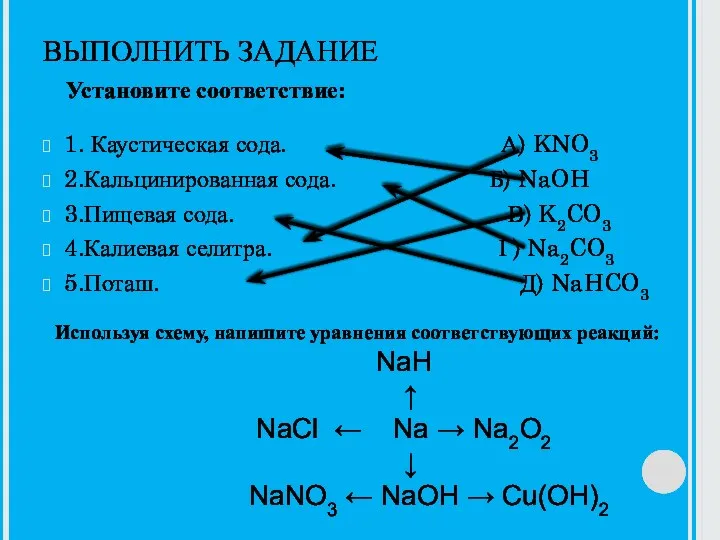 Каустическая сода
Каустическая сода Кислотність бджолиного обніжжя
Кислотність бджолиного обніжжя Золото (Au)
Золото (Au) Понятие аналитической химии, её цели и задачи. Химический анализ, его задачи
Понятие аналитической химии, её цели и задачи. Химический анализ, его задачи Оксиды
Оксиды Соединения щелочных металлов
Соединения щелочных металлов Физика полимеров Ч1
Физика полимеров Ч1 Силикатная промышленность
Силикатная промышленность ПЕРІОДИЧНИЙ ЗАКОН
ПЕРІОДИЧНИЙ ЗАКОН Углеводороды. Природный газ. Алканы
Углеводороды. Природный газ. Алканы Моющие и чистящие средства
Моющие и чистящие средства