Содержание
- 2. Вызов Основная часть Закрепление 1 2 3 Химические свойства Физические свойства Получение кремния Применение Физ. минутка
- 3. 1 2 3 Верю- не -верю Техника безопасности Домашнее задание Вызов Основная часть Закрепление
- 4. Напоминаю, что “красная строка” означает то же самое, что и “новый абзац”. Это название осталось нам
- 5. А) В эпоху палеолита, т.е. 800-1 000 тысячелетий тому назад, кремний помог человеку в борьбе за
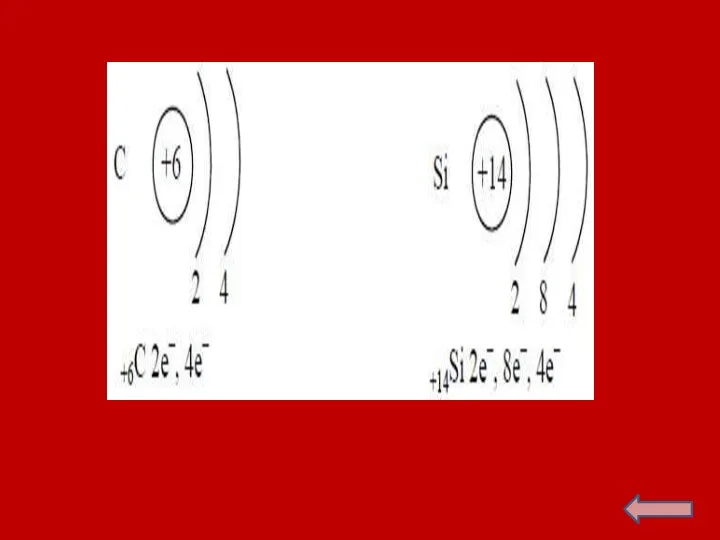
- 6. ХАРАКТЕРИСТИКА ХИМИЧЕСКОГО ЭЛЕМЕНТА НА ОСНОВАНИИ ЕГО ПОЛОЖЕНИЯ В ПЕРИОДИЧЕСКОЙ СИСТЕМЕ Д.И. МЕНДЕЛЕЕВА Положение элемента в Периодической
- 7. Правила выживания в химической лаборатории 1. Если вы откупорили что-либо – закупорьте. 2. Если в руках
- 8. Кристаллический кремний-это вещество темно-серого цвета со стальным блеском. Структура кремния аналогична структуре алмаза: кристаллическая решетка кубическая
- 9. Типичный неметалл, инертен. Как восстановитель: 1) С кислородом Si0 + O2 t˚→ Si+4O2 2) С фтором
- 11. Получение кремния 1) Промышленность – нагревание угля с песком: 2C + SiO2 t˚→ Si + 2CO
- 12. Отрасли силикатной промышленности
- 13. Керамика (греч. keramike - гончарное искусство, от kramos - глина) - изделия и материалы, получаемые спеканием
- 14. Заводское производство стекла в России начинается при царе Михаиле Феодоровиче (1635). Стеклоделие, упавшее было на первых
- 15. В средние века было случайно обнаружено, что продукты обжига загрязнённых глиной известняков по водостойкости не уступают
- 16. Домашнее задание пар.30, упр. 2,6,
- 17. Ответы Катод Растворимость Едкий натр Молекула Неон Ион Йод
- 18. Ответ: Коротко - процесс изготовления процессора выглядит так: из расплавленного кремния на специальном оборудовании выращивают монокристалл
- 20. Скачать презентацию
















 Тренажёр: знаки химических элементов
Тренажёр: знаки химических элементов Алкены. Физические и химические свойства
Алкены. Физические и химические свойства Окислительно-восстановительные реакции
Окислительно-восстановительные реакции Химически опасные объекты Аварии, связанные с выбросом АХОВ
Химически опасные объекты Аварии, связанные с выбросом АХОВ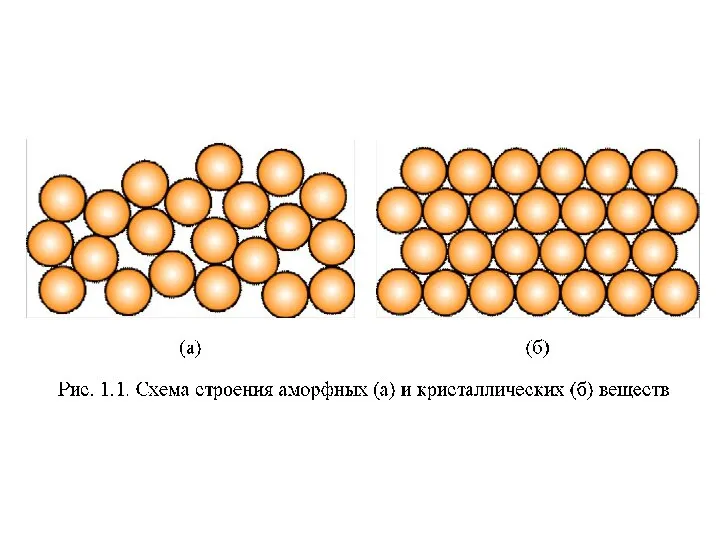 Материаловедение
Материаловедение Синтетические волокна
Синтетические волокна Презентация на тему Неметаллы, особенности строения
Презентация на тему Неметаллы, особенности строения  Электролиз (катод)
Электролиз (катод) Основные принципы работы химических сенсоров
Основные принципы работы химических сенсоров Химическая картина мира
Химическая картина мира Основания: определение, классификация, химические свойства
Основания: определение, классификация, химические свойства Металлы. Общая характеристика, химические свойства. Получение
Металлы. Общая характеристика, химические свойства. Получение Вебинар. Гидролиз солей
Вебинар. Гидролиз солей Свойства радиоактивных элементов
Свойства радиоактивных элементов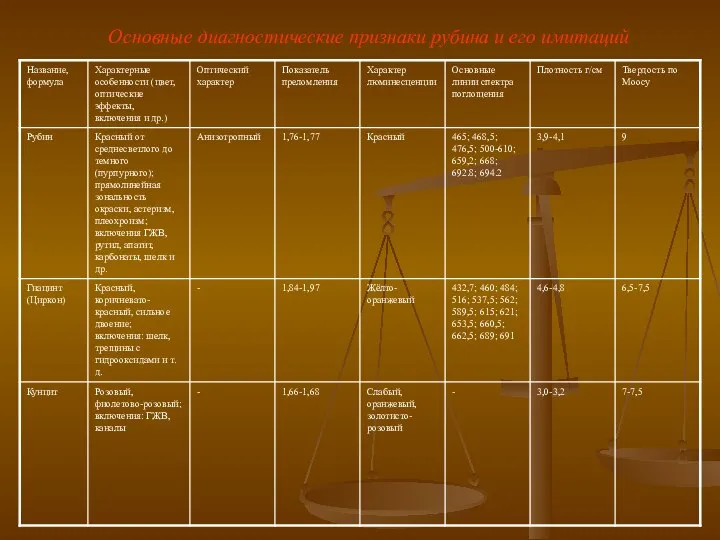 Основные диагностические признаки рубина и его имитаций
Основные диагностические признаки рубина и его имитаций Генетические ряды неорганических соединений
Генетические ряды неорганических соединений Двойные латуни. Диаграмма состояния. Примеси. Структура и свойства
Двойные латуни. Диаграмма состояния. Примеси. Структура и свойства Вуглеводи. Визначення вуглеводів
Вуглеводи. Визначення вуглеводів Галогены. Обобщение знаний
Галогены. Обобщение знаний Подготовка к ГИА по химии
Подготовка к ГИА по химии Предпосылки открытия Периодического закона Д. И. Менделеевым
Предпосылки открытия Периодического закона Д. И. Менделеевым ОВ. Структура и принцип работы параметры ОВ
ОВ. Структура и принцип работы параметры ОВ Абсолютное первенство по химии - 2012
Абсолютное первенство по химии - 2012 строение атома углерода. Валентные состояния атома углерода
строение атома углерода. Валентные состояния атома углерода Общая характеристика элементов IIА группы
Общая характеристика элементов IIА группы Вода… Химические названия
Вода… Химические названия Водород – первый элемент в периодической таблице
Водород – первый элемент в периодической таблице Кристаллы, выращенные учащимися
Кристаллы, выращенные учащимися