Содержание
- 2. Синтез коллоидных КТ в неполярных средах. Для синтеза коллоидных квантовых точек используются химические методы, основанные на
- 3. В коллоидном синтезе можно выделить 4 основные стадии: 1) Химическая реакция, в которой создаются целевые мономеры;
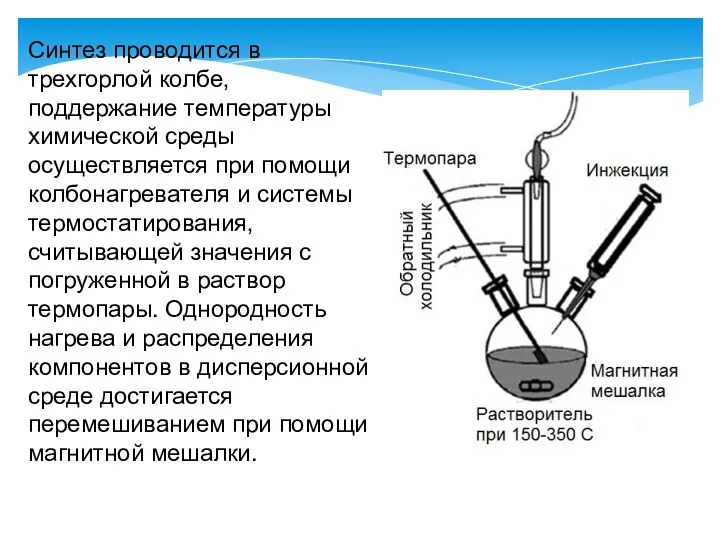
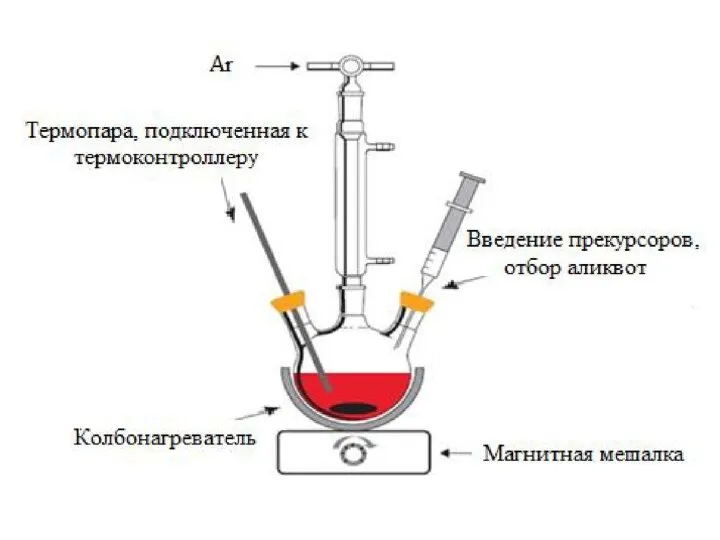
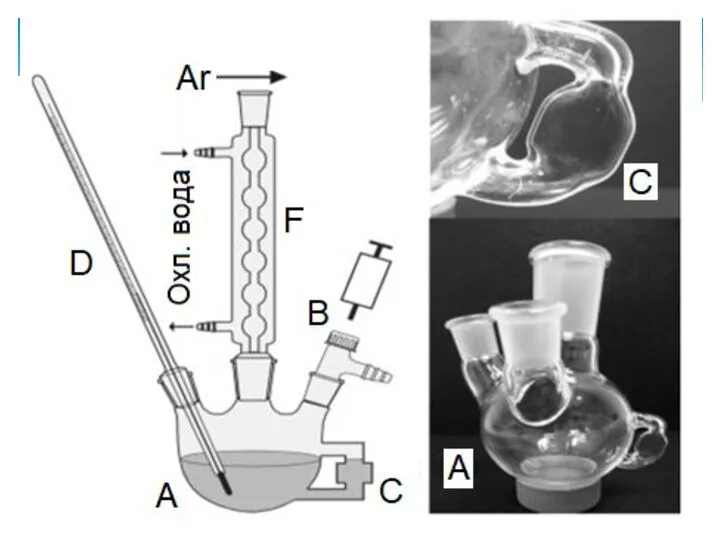
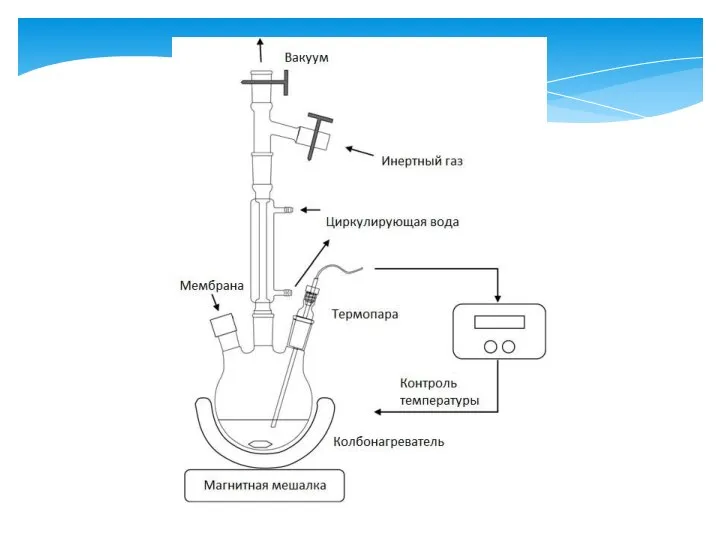
- 4. Синтез проводится в трехгорлой колбе, поддержание температуры химической среды осуществляется при помощи колбонагревателя и системы термостатирования,
- 7. Обратный холодильник Холодильники бывают с воздушным охлаждением, бывают с водяным... Воздушный обратный холодильник применяется для высококипящих
- 9. 1. Химическая реакция В непрерывно перемешиваемую и нагретую до температуры нуклеации (Tn = 200 ‒ 300
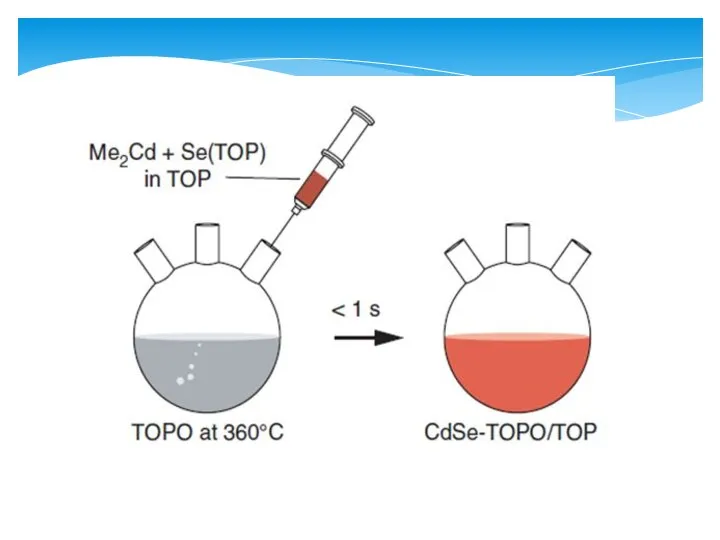
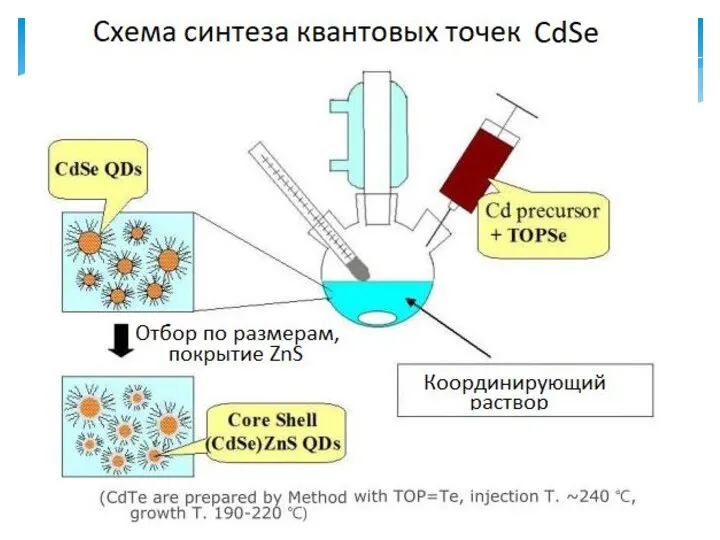
- 10. Так, в пионерской работе группы Бавенди синтез проводился следующим образом (на примере селенида кадмия): Нуклеация проводилась
- 11. Для справок: 1. Триоктилфосфин (TOP) P(C8H17)3 – стабилизатор частиц в неполярной среде, координирующий агент халькогенов (TOP-S,
- 12. После этого растворы обоих компонентов смешивали в шприце и быстро впрыскивали в колбу с TOPO, которая
- 14. Метод основан на том, что образующийся селенид кадмия, в отличие от всех остальных компонентов системы, практически
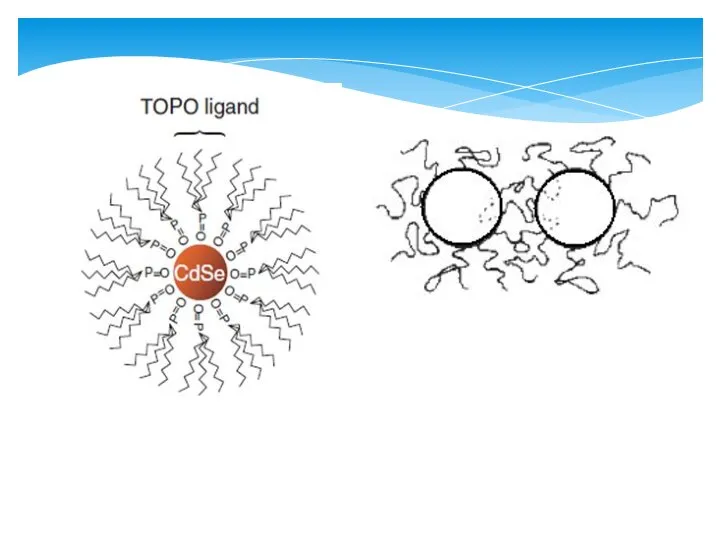
- 16. Помимо прочего TOPO является еще и хорошим стабилизатором наночастиц. Он обволакивает каждую частицу и препятствует их
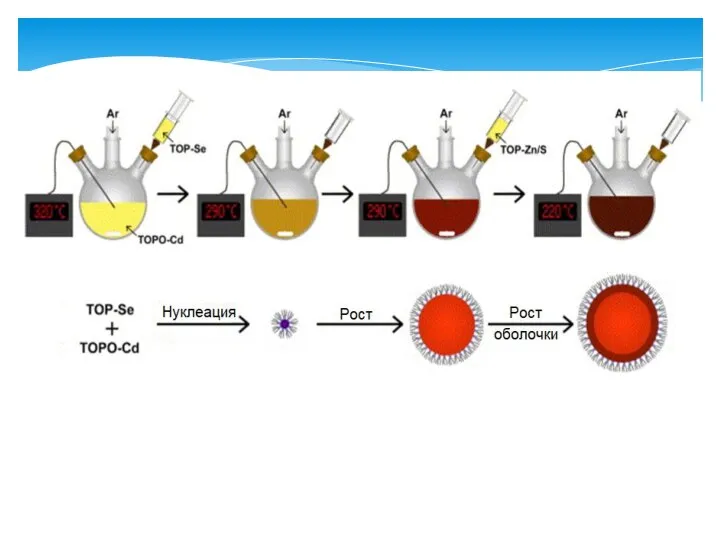
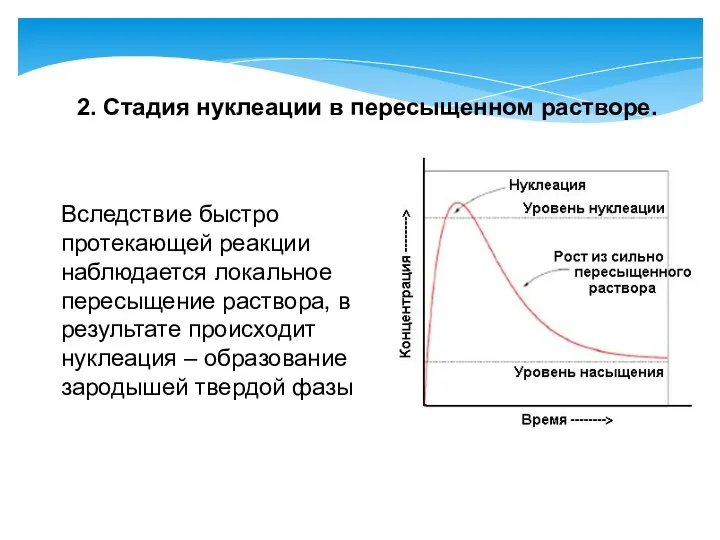
- 17. Вследствие быстро протекающей реакции наблюдается локальное пересыщение раствора, в результате происходит нуклеация – образование зародышей твердой
- 18. Согласно классической теории зародышеобразования нуклеация происходит спонтанно: в некоторых нестабильных участках пересыщенного раствора молекулы или ионы
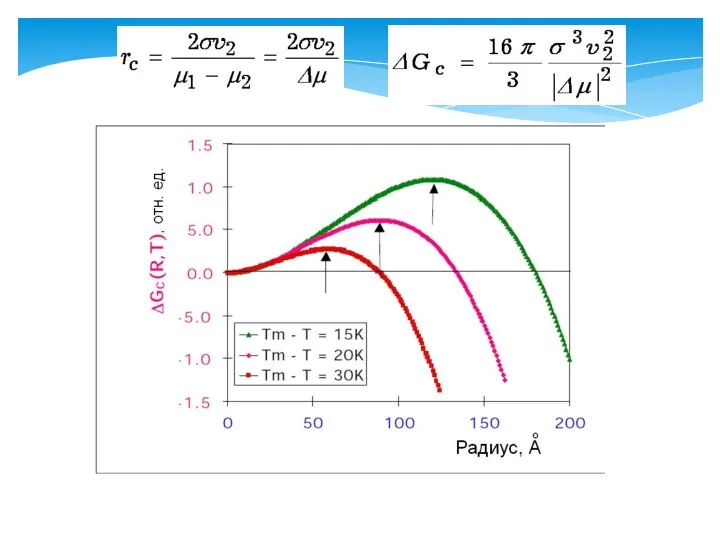
- 21. а) увеличение свободной энергии из-за роста межфазной поверхности, б) снижение свободной энергии из-за фазового превращения, в)
- 23. Кристаллизация из раствора: Применительно к процессу выделения твердой или жидкой фазы из раствора формулы принимают вид:
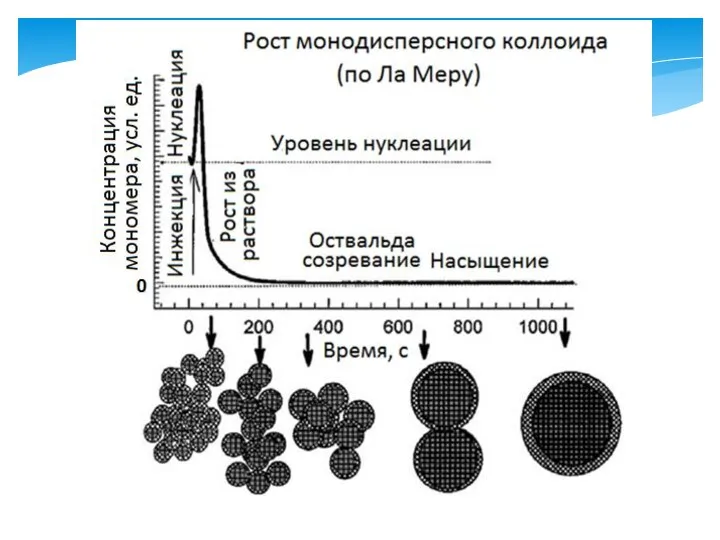
- 24. 3. Рост частиц в растворе Наночастицы с равномерным распределением по размерам, могут быть синтезированы, если все
- 25. Чтобы добиться резкой нуклеации, концентрация растворенного вещества должна увеличиваться резко до очень высокого пересыщения, а затем
- 26. Рост ядер зависит от нескольких шагов, таких как, нуклеация зародышей, диффузия мономеров из раствора к растущей
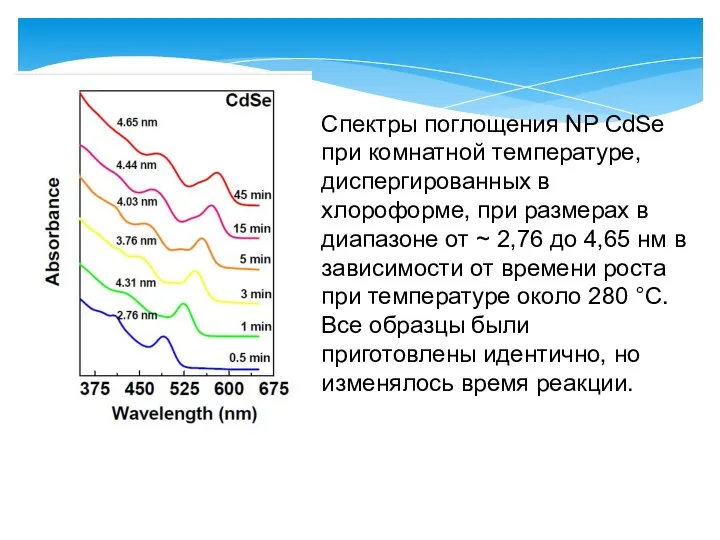
- 27. Спектры поглощения NP CdSe при комнатной температуре, диспергированных в хлороформе, при размерах в диапазоне от ~
- 28. Рассмотрим рост сферического ядра. Если процесс роста контролируется диффузией мономеров из объема раствора к поверхности частиц,
- 29. Если начальный радиус ядра r0, и если концентрация в объеме не существенно меняется со временем, мы
- 30. Если процесс диффузии является быстрым, CS ≈ СЬ, а скорость роста контролируется процессами на самой поверхности.
- 31. Скорость роста при мононуклеарном механизме роста пропорциональна площади поверхности, т.е. ??/??=???2 , (2) где km -
- 32. При полиядерном росте, второй слой начинает расти даже до того, как рост первого слоя завершен. Это,
- 33. Среди трех механизмов, описанных здесь (т.е. диффузионноконтролируемый рост, мононуклеарное включение мономеров в поверхность и многоядерное включение
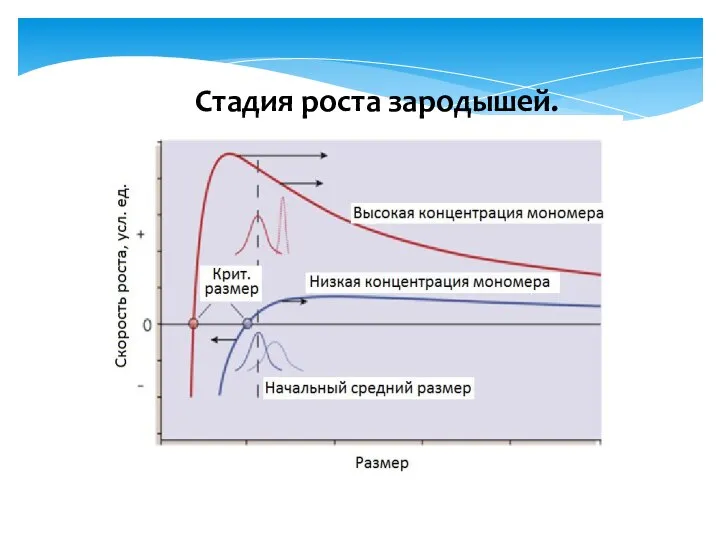
- 35. Стадия роста зародышей.
- 36. Способность производить нанокристаллы с относительно узким распределением по размерам является ключевым требованием к современным методам. Рассмотрим
- 37. Правая часть кривой показывает, что более крупные кристаллы являются стабильными и растут. Но скорость роста у
- 38. Фокусировка по размерам нанокристаллов может происходить в двух различных режимах, "фокусировки" и "расфокусировки", в зависимости от
- 39. Таким образом, распределение будет спонтанно узким или "в фокусе". Понятие фокусировки размерного распределения было четко продемонстрировано
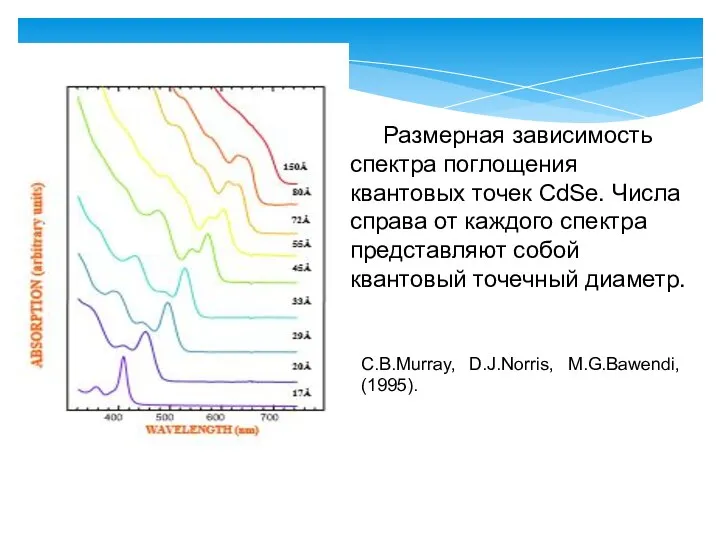
- 40. Размерная зависимость спектра поглощения квантовых точек CdSe. Числа справа от каждого спектра представляют собой квантовый точечный
- 41. Если концентрация мономера находится ниже критического порога, небольшие нанокристаллы растворяются, в то время как более крупные
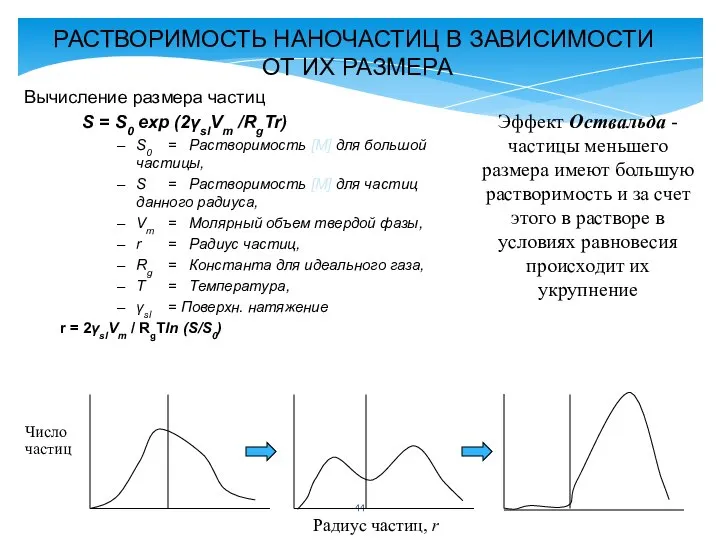
- 42. Процесс созревания Оствальда начинается, когда раствор истощён из-за роста частиц, при этом большие частицы продолжают расти
- 43. Созревание Оствальда хорошо описываеися с помощью Лифшица-Слёзова-Вагнера (LSW) модели, показывающей, что V пропорционален времени реакции t,
- 44. Вычисление размера частиц S = S0 exp (2γslVm /RgTr) S0 = Растворимость [M] для большой частицы,
- 45. На этапе созревания Оствальда невозможно получить монодисперсные частицы. Размер оставшихся после полного исчезновения пересыщения частиц может
- 46. Стабилизация частиц. Нам необходимо достичь не только заданной дисперсности, но и стабилизировать раствор во времени. Этого
- 47. Стабилизатор, во-первых, должен предотвращать агрегацию частиц дисперсной фазы. Во-вторых, не препятствовать диффузионному росту КТ. В-третьих, ориентируясь
- 49. Возможными органическими стабилизаторами могут выступать: 1) Амины – соединения, являющиеся продуктами замещения водорода в аммиаке органическими
- 50. Тиоспирты можно рассматривать как органические производные сероводорода, в которых один или два атома водорода замещены предельными
- 51. Наиболее перспективными стабилизаторами выступает класс карбоновых кислот, а точнее ряд длинноцепочечных (жирных) кислот. Атомом, осуществляющим стабилизацию,
- 52. Размерно-селективное осаждение. «Растворимость» КТ разного размера различна. На этом явлении основан метод размерно-селективного осаждения (РСО). Более
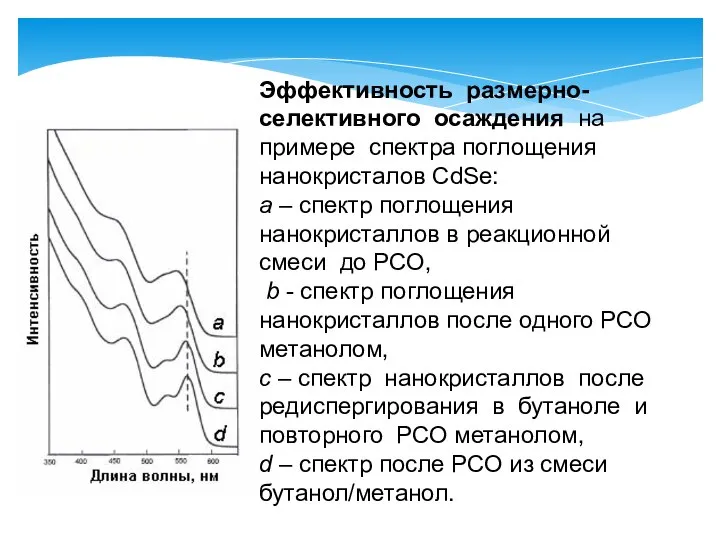
- 53. Эффективность размерно-селективного осаждения на примере спектра поглощения нанокристалов CdSe: a – спектр поглощения нанокристаллов в реакционной
- 54. Очистка коллоидного раствора Непосредственно после того, как получен коллоидный раствор, содержащий частицы нужных размеров, его необходимо
- 55. Решение задачи состоит во введении сильно полярного вещества – осадителя, чаще всего безводного метанола. Частицы из-за
- 56. Флокуляцию ускоряют за счет центрифугирования раствора. Аналогичный подход может быть применен для разделения частиц по размеру.
- 57. Выделение фракций Отделяя центрифугированием осадок (более крупные частицы) и раствор (более мелкие) и заново диспергируя осадок,
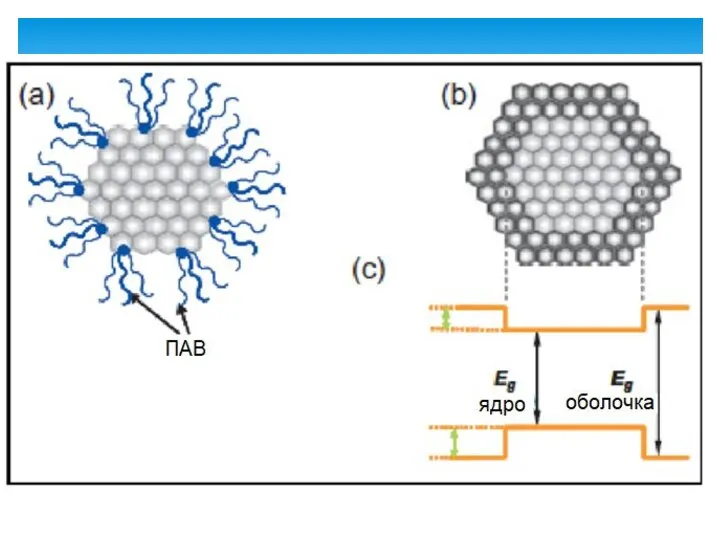
- 58. Стабилизация квантовой точки На заключительном этапе производства КТ полученные нанокристаллы сверху покрывают материалом с широкой запрещенной
- 59. Схематическая иллюстрация: КТ, покрытая ПАВ. (b) КТ, пассивированная неорганической оболочкой (структура КТ ядро / оболочка). (с)
- 62. Коротко о коллоидном синтезе CdSe: соединение кадмия нагревают до 320 °С и растворяют в органическом растворителе.
- 63. Заключение Бесспорным преимуществом метода коллоидного синтеза является возможность массового производства квантовых точек в любых необходимых количествах.
- 64. КТ можно использовать практически во всех сферах, в которых нашли широкое применение современные полупроводники, например, в
- 65. На основе КТ можно изготавливать светодиоды повышенной яркости, а также специальные покрытия для существующих источников света,
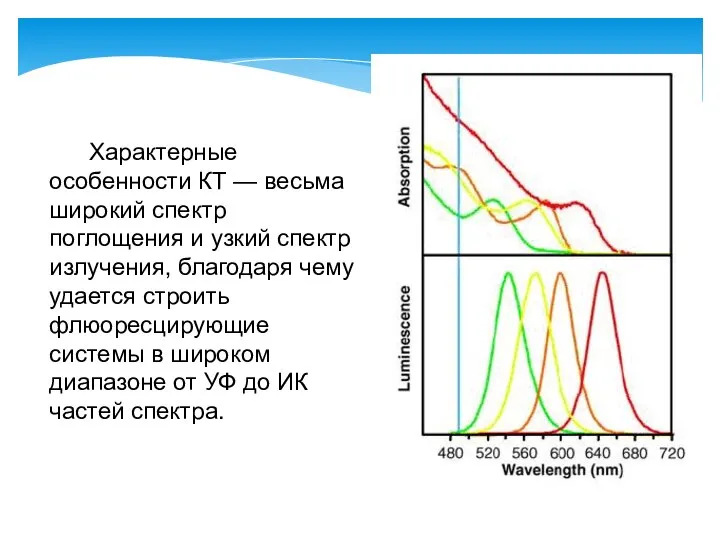
- 66. Характерные особенности КТ — весьма широкий спектр поглощения и узкий спектр излучения, благодаря чему удается строить
- 68. Скачать презентацию















































 1_
1_ Планарные потенциометрические сенсоры на основе пилларарена -DNS-162
Планарные потенциометрические сенсоры на основе пилларарена -DNS-162 Ископаемые углеводороды
Ископаемые углеводороды Презентация на тему Сложные эфиры
Презентация на тему Сложные эфиры  Водород
Водород Кремний Полупроводники в электронике_Горб
Кремний Полупроводники в электронике_Горб Влияние пластифицирующих добавок на свойства декоративного мелкозернистого бетона
Влияние пластифицирующих добавок на свойства декоративного мелкозернистого бетона Переработка нефти
Переработка нефти Металлы. Контрольная работа
Металлы. Контрольная работа Электролитическая диссоциация
Электролитическая диссоциация Исследование физико-химических свойств щавелевой кислоты
Исследование физико-химических свойств щавелевой кислоты Природные источники углеводородов
Природные источники углеводородов Наблюдения в сходящемся свете. Коноскопия
Наблюдения в сходящемся свете. Коноскопия Презентация на тему Биополимеры
Презентация на тему Биополимеры  Разбор заданий
Разбор заданий Турнир знатоков химии
Турнир знатоков химии Неделя химии в МБОУ (викторина)
Неделя химии в МБОУ (викторина) Ліпіди і їх роль в життєдіяльності клітини
Ліпіди і їх роль в життєдіяльності клітини Ароматические углеводороды (арены)
Ароматические углеводороды (арены) Презентация на тему Классификация химических реакций
Презентация на тему Классификация химических реакций  Гидролиз. Виды гидролиза
Гидролиз. Виды гидролиза Применение хидких кристалов в промышленности
Применение хидких кристалов в промышленности Плотность вещества
Плотность вещества Соли в свете теории электролитической диссоциации
Соли в свете теории электролитической диссоциации Физические свойства металлов
Физические свойства металлов Водневий та металічний звязок
Водневий та металічний звязок Основания
Основания Диссоциация веществ
Диссоциация веществ