Слайд 2Метилэтилкетон (МЭК), свойства
Метилэтилкетон (МЭК) - химическое соединение класса кетонов, бесцветная легколетучая жидкость

с запахом, напоминающим запах ацетона, но более слабым по силе.
-Температура вспышки: 2,2 °C, КПВ 1,97-10,2%.
-Взрывоопасен в смеси с воздухом при концентрации 1,97-10,2 %.
-При температуре выше 9°C могут образоваться взрывоопасные смеси пар/воздух. Не допускать открытого огня, искр и курения.
-Пар тяжелее воздуха и может стелиться по земле; возможно возгорание на расстоянии.
-Реагирует бурно с сильными окислителями и неорганическими кислотами с опасностью пожара и взрыва. Агрессивно в отношении некоторых пластиков.
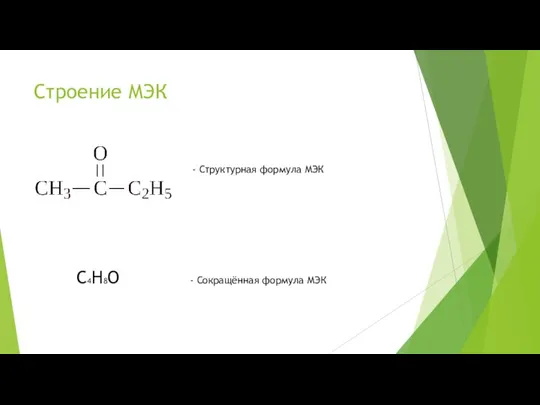
Слайд 3Строение МЭК
- Структурная формула МЭК
С4Н8О - Сокращённая формула МЭК
Слайд 4Химические свойства МЭК
1. Реакция горения:
2. Гидрирование:
3. Гидратация:

Слайд 65.Реакции жёсткого окисления:
а) В кислой среде
б) В нейтральной среде

Слайд 76. Альфа-галогенирование:
7. Взаимодействие с пентахлоридом фосфора:

Слайд 8Получение и применение МЭК
В промышленности метилэтилкетон получают из бутенов, содержащихся в бутан-бутиленовой фракции

газов переработки нефти. Первая стадия — гидратация бутенов 70-85%-ной H2SO4 при 30-40 °C и давлении ~ 0,1 МПа в 2-бутанол с промежуточным образованием 2-бутилсульфата CH3CH(OSO3H)C2H5. 2-Бутанол выделяют ректификацией и окисляют в метилэтилкетон дегидрированием при 400—500 °C (кат.: ZnO на пемзе, цинк-медный) или при 500 °C (в присутствии Ag на пемзе). Селективность гидратации бутенов составляет 80—85 %, дегидрирования 2-бутанола — около 99 %, окислительного дегидрирования — 85—90 %. Недостатки процесса: образование большого количества сточных вод на стадии гидратации, высокие энергозатраты, связанные с необходимостью концентрирования H2SO4 (разбавляется при гидратации до 35%-ной). Разработаны и внедрены (Япония, ФРГ) процессы прямой гидратации бутенов с использованием гетерополикислот и сульфокатионитов в качестве катализаторов, не имеющие указанных недостатков. Перспективно получение метилэтилкетона окислением бутенов на гомогенном катализаторе — водном растворе соли палладия и обратимо действующего окислителя (например, фосфорномолибденванадиевой гетерополикислоты). В лабораторных условиях метилэтилкетон можно получить дегидрированием 2-бутанола.







 Развитие познавательной активности творческих способностей и индивидуализация на уроках химии
Развитие познавательной активности творческих способностей и индивидуализация на уроках химии Углеродистые стали
Углеродистые стали Целестин
Целестин Презентацию выполнила ученица 10 класса Поликарпова Диана 2010 год
Презентацию выполнила ученица 10 класса Поликарпова Диана 2010 год Гальванический элемент
Гальванический элемент Углеводы. Классификация углеводов
Углеводы. Классификация углеводов Степень окисления. Классификация неорганических соединений
Степень окисления. Классификация неорганических соединений Катаболизм пуриновых нуклеотидов
Катаболизм пуриновых нуклеотидов Органическая химия
Органическая химия Соединения азота в атмосфере. Лекция 4
Соединения азота в атмосфере. Лекция 4 Структура к свойства веществ
Структура к свойства веществ Химические вещества парабены
Химические вещества парабены Влияние меди на коррозию низколегиованных сталей
Влияние меди на коррозию низколегиованных сталей Серная кислота
Серная кислота Основные свойства и опасности нефти. Безопасность для танкеров
Основные свойства и опасности нефти. Безопасность для танкеров Окислители в пиросоставах
Окислители в пиросоставах Вода. Строение молекулы. Водородная связь. Физические и химические свойства
Вода. Строение молекулы. Водородная связь. Физические и химические свойства Презентация на тему Гидролиз
Презентация на тему Гидролиз  Электролиз
Электролиз Презентация на тему Глюкоза (10 класс)
Презентация на тему Глюкоза (10 класс)  Основания и их свойства
Основания и их свойства Презентация на тему Многоатомные спирты
Презентация на тему Многоатомные спирты  Жидкое состояние вещества
Жидкое состояние вещества Поделочный камень родонит
Поделочный камень родонит Фосфор. Аллотропия фосфора. Физические и химические свойства фосфора
Фосфор. Аллотропия фосфора. Физические и химические свойства фосфора Кремний и 4 группа. 9 класс
Кремний и 4 группа. 9 класс Получение металлов
Получение металлов Степени окисления
Степени окисления