Содержание
- 2. Общие положения Синтез полимеров возможен: Из НМС-мономеров : Цепными процессами, протекающими по а) радикальному механизму; б)
- 3. 1. Реакции полимеризации Способность мономеров к полимеризации Условия: А) структурные 1. Наличие кратных связей >С =
- 4. Общая схема процесса полимеризации инициирование - процесс образования активного центра (R или К+, А-) J →
- 5. Цепные процессы Процессы, в которых превращение мономеров в полимер осуществляется путем последовательного чередования нескольких реакций активных
- 6. Длина кинетической цепи - число химических актов, возбужденных одной исходной активной частицей (радикалом, ионом)
- 7. Особенности полимеризационных (цепных) процессов не сопровождаются выделением побочных продуктов Протекают без изменения элементарного состава реагирующих мономеров
- 8. Способность к полимеризации ненасыщенных мономеров Мономер Тип инициирования радикальн. Катион. Анион. Этилен + + + 1-алкилолефин
- 9. Радикальная полимеризация - цепной метод синтеза макромолекул из мономеров, протекающий через образование свободных радикалов
- 10. 1 стадия – инициирование* * образование свободных радикалов. Происходит под действием: тепла (термическое инициир.) света (фотоиницииорование)
- 11. Химическое иницииорование
- 12. Примеры химических инициаторов Пероксид бензоила (Т распада = 70-80 0С) Персульфат калия (Т распада = 40-50
- 13. Выбор инициатора обусловлен: его растворимостью в мономере или растворителе Температурой (влияние на скорость распада инициатора) Для
- 14. 2 стадия – рост цепи* * Происходит за счёт последовательного присоединения мономеров в растущему макрорадикалу
- 15. 3 стадия – обрыв цепи* гибель макрорадикала за счёт - 1) рекомбинации
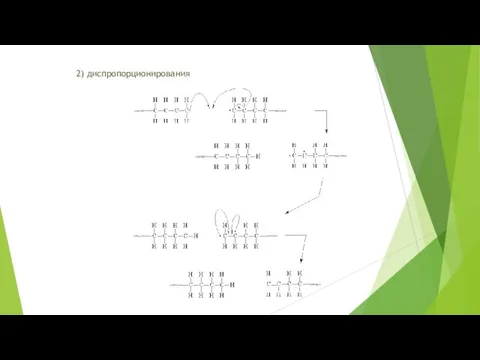
- 16. 2) диспропорционирования
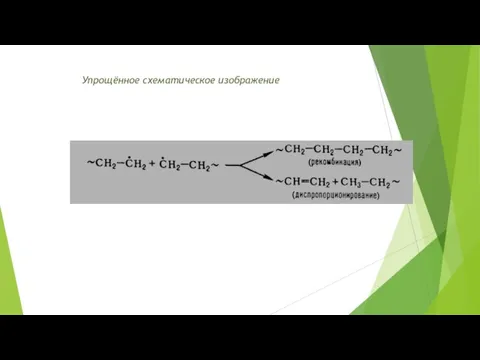
- 17. Упрощённое схематическое изображение
- 18. Растущий макро-радикал отрывает группу атомов (или атом) от какой-либо молекулы, превращаясь в ненасыщенную нейтральную макромолекулу, а
- 19. Передача цепи через: молекулу мономера Молекулу растворителя Специально вводимые вещества (регуляторы)
- 20. Влияние различных факторов на процесс радикальной полимеризации Температура Концентрация инициатора Концентрация мономера Давление
- 21. Ингибиторы и регуляторы полимеризации Хиноны Ароматичекие амины Нитросоединения Фенолы Органические соли Cu, Fe, Zn, Pb
- 23. Скачать презентацию


















 Определение формул органических веществ
Определение формул органических веществ Определение времени прохождения диффузии
Определение времени прохождения диффузии Кроссворд Интересные факты в химии
Кроссворд Интересные факты в химии Карбоновые кислоты. Тест. 10 класс
Карбоновые кислоты. Тест. 10 класс Презентация на тему Медь
Презентация на тему Медь  Топливо и расчеты его горения
Топливо и расчеты его горения Магний (Mg, Magnesium). Общая характеристика магния
Магний (Mg, Magnesium). Общая характеристика магния Окислительно-восстановительные реакции
Окислительно-восстановительные реакции Презентация на тему Неогранические соединения. Периодическая таблица
Презентация на тему Неогранические соединения. Периодическая таблица  10.1С_Серная кислота
10.1С_Серная кислота Использование комбинаторных задач для подсчета вероятностей
Использование комбинаторных задач для подсчета вероятностей Строение молекул. Метод валентных связей. Лекция 5
Строение молекул. Метод валентных связей. Лекция 5 Процестер және аппараттар курсының пәні (1 дәріс)
Процестер және аппараттар курсының пәні (1 дәріс) Фуллерены (шары Бакминстера)
Фуллерены (шары Бакминстера) Презентация на тему Пластмасса
Презентация на тему Пластмасса  Лакокрасочные материалы
Лакокрасочные материалы Окисли́тельно-восстанови́тельные реа́кции
Окисли́тельно-восстанови́тельные реа́кции Оксиды, получение и свойства
Оксиды, получение и свойства h-m-chniy-zv-yazok-budova-rechovin
h-m-chniy-zv-yazok-budova-rechovin Алкины
Алкины Химия. Вещества. 8 класс
Химия. Вещества. 8 класс Молекулярная струйная печать
Молекулярная струйная печать Салициловая кислота
Салициловая кислота Углеводы
Углеводы Химическое равновесие
Химическое равновесие Химическая связь в органических соединениях
Химическая связь в органических соединениях Алкены. Гомологический ряд алкенов. Изомерия алкенов. Химические свойства алкенов
Алкены. Гомологический ряд алкенов. Изомерия алкенов. Химические свойства алкенов Основные классы неорганических веществ
Основные классы неорганических веществ