Содержание
- 2. Реакции, протекающие с изменением степени окисления называются окислительно-восстановительными.
- 3. Окислитель и восстановитель Окислителем называют реагент, который принимает электроны в ходе окислительно-восстановительной реакции. Восстановителем называют реагент,
- 4. ПРОЦЕСС ОКИСЛЕНИЯ И ВОССТАНОВЛЕНИЯ Окислением называют процесс отдачи электронов атомом, молекулой или ионом, который сопровождается повышением
- 5. Окисление - процесс отдачи электронов атомом, молекулой или ионом. Атом превращается в положительно заряженный ион: Zn0
- 6. Восстановление - процесс присоединения электронов атомом, молекулой или ионом. Атом превращается в отрицательно заряженный ион S0
- 7. Определение степени окисления химических элементов в формуле вещества. Правила: 1. Отрицательная степень окисления = 8 -
- 8. Определение степеней окисления атомов химических элементов С.о. атомов х/э в составе простого вущества = 0 Алгебраическая
- 9. Необходимо запомнить! В соединениях с ионной связью степени окисления элементов равны зарядам ионов. Na+1Cl-1, Ca+2F2-1, Mg+2O-2.
- 10. Элементы с постоянной степенью окисления Щелочные металлы ( I группа, главная подгруппа) +1 Li, Na, K,
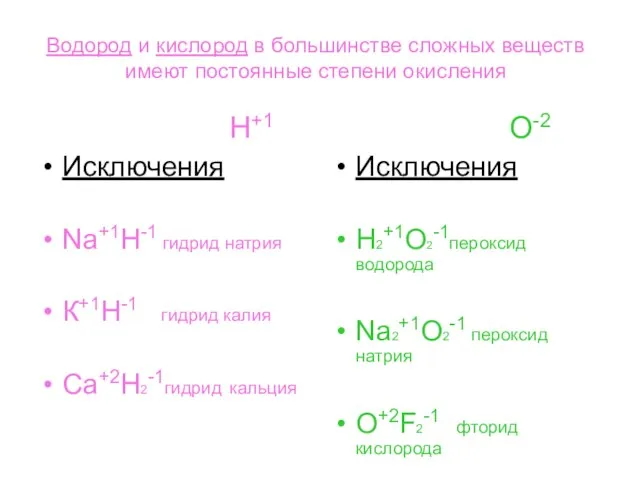
- 11. Водород и кислород в большинстве сложных веществ имеют постоянные степени окисления Н+1 О-2 Исключения Na+1H-1 гидрид
- 12. Порядок определения значений с.о. элементов: 1.Выпишем с. о. кислорода и обозначим неизвестную степень окисления хлора через
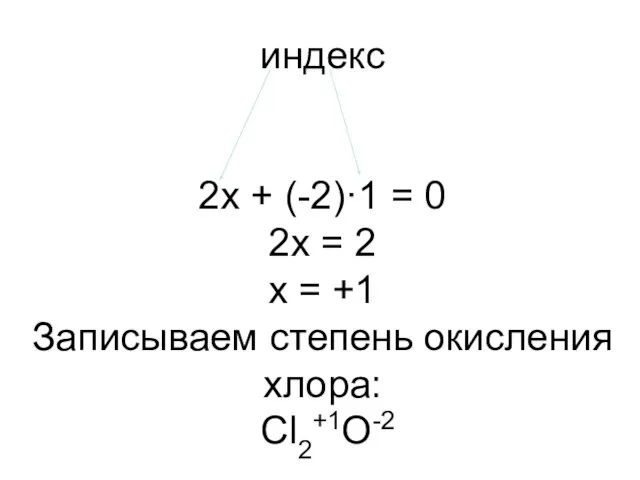
- 13. индекс 2х + (-2)·1 = 0 2х = 2 х = +1 Записываем степень окисления хлора:
- 15. Скачать презентацию










 О чем не узнаешь на уроке
О чем не узнаешь на уроке Обобщение сведений об основных классах неорганических веществ. 8 класс
Обобщение сведений об основных классах неорганических веществ. 8 класс Скорость химических реакций. Факторы, влияющие на скорость химической реакции
Скорость химических реакций. Факторы, влияющие на скорость химической реакции Кислородные соединения углерода
Кислородные соединения углерода Сущность химических реакций и признаки их протекания
Сущность химических реакций и признаки их протекания Свойства аминов
Свойства аминов Презентация на тему Дисперсные системы и растворы
Презентация на тему Дисперсные системы и растворы 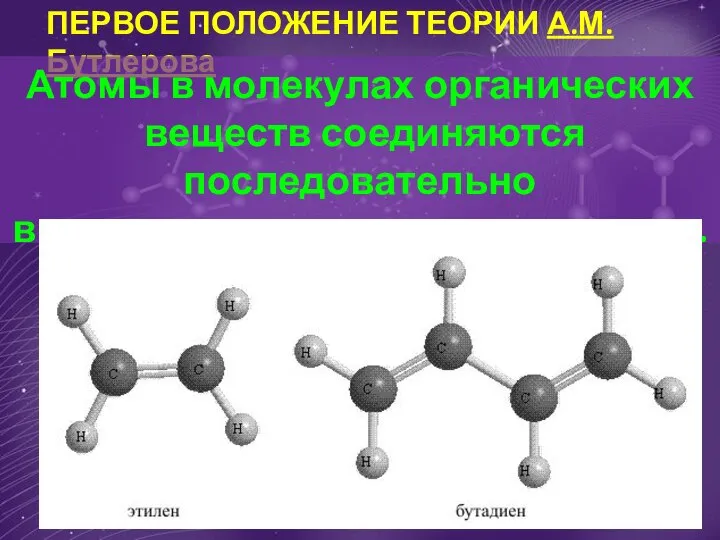 Первое положение теории А.М. Бутлерова Атомы в молекулах органических веществ соединяются последовательно
Первое положение теории А.М. Бутлерова Атомы в молекулах органических веществ соединяются последовательно Простые и сложные вещества
Простые и сложные вещества Комплексное изучение системы NiO-ZnO-CoO с целью модифицирования свойств исходной матрицы никель-цинкового феррита xZnxFe2O4
Комплексное изучение системы NiO-ZnO-CoO с целью модифицирования свойств исходной матрицы никель-цинкового феррита xZnxFe2O4 Свойства алкенов
Свойства алкенов Относительная молекулярная масса вещества
Относительная молекулярная масса вещества Витамины и их роль в жизни людей
Витамины и их роль в жизни людей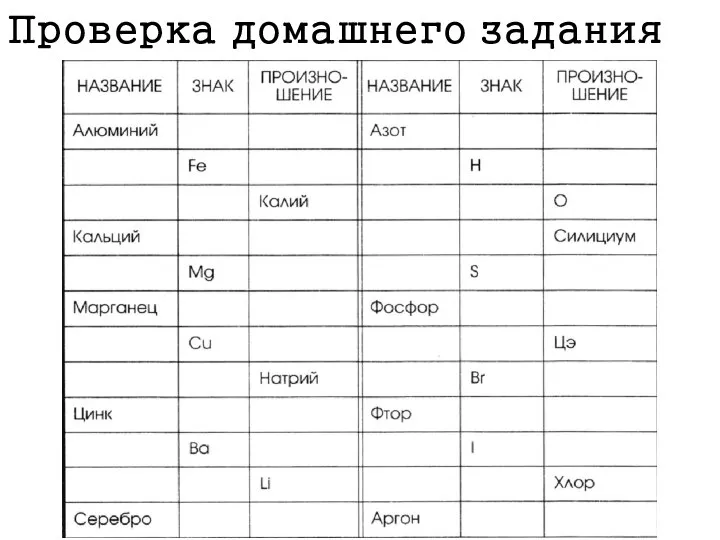 Основные сведения о строении атома
Основные сведения о строении атома Метод окислительно - восстановительного титрования
Метод окислительно - восстановительного титрования Здравствуйте, химия! Что изучает химия
Здравствуйте, химия! Что изучает химия G11. Химический состав
G11. Химический состав Особо чистые вещества. Занятие 12
Особо чистые вещества. Занятие 12 Бишофит - новый старый антигололедный реагент
Бишофит - новый старый антигололедный реагент Типы химических связей
Типы химических связей Физическая химия, термодинамика
Физическая химия, термодинамика Уравнения химических реакций
Уравнения химических реакций Химические структуры
Химические структуры teoria_Butlerova
teoria_Butlerova Тренажёр: знаки химических элементов
Тренажёр: знаки химических элементов Получение функциональных плёнок на основе TiO2
Получение функциональных плёнок на основе TiO2 Гармонизации терминологии аналитической химии с использованием электронной системы на основе MS WSS (Windows SharePoint Services) Широкова В.И.,
Гармонизации терминологии аналитической химии с использованием электронной системы на основе MS WSS (Windows SharePoint Services) Широкова В.И.,  Производство органических препаратов ароматического ряда
Производство органических препаратов ароматического ряда