Содержание
- 2. Цели урока: Систематизировать и углубить знания об элементах – металлах. Сформировать понятие о строении простых веществ.
- 3. Общая характеристика металлов
- 4. Определения Химический элемент – это определённый вид атомов. Простое вещество – это вещество, образованное атомами одного
- 5. Строение атомов Положение в периодической системе
- 6. Типичные металлы: S-элементы (1-2 ē на внешнем E ур.) D-элементы (1-2 ē на внешнем Е ур.)
- 8. Ме0 + Еi Ме+n + nē Еi – энергия ионизации Ме0 – nē Ме+n процесс окисления
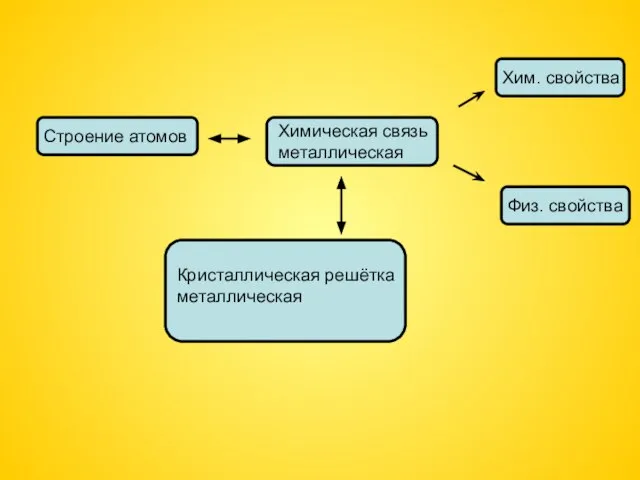
- 9. Строение атомов Химическая связь металлическая Хим. свойства Физ. свойства Кристаллическая решётка металлическая
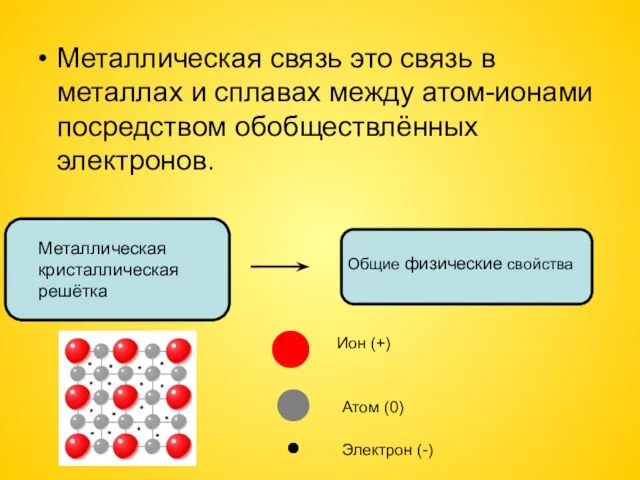
- 10. Металлическая связь это связь в металлах и сплавах между атом-ионами посредством обобществлённых электронов. Металлическая кристаллическая решётка
- 11. Общие физические свойства: Металлический блеск Электропроводность Ковкость Теплопроводность
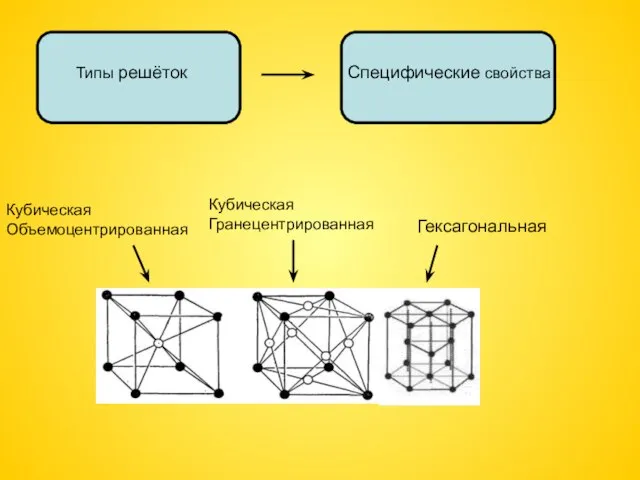
- 12. Типы решёток Специфические свойства Гексагональная Кубическая Объемоцентрированная Кубическая Гранецентрированная
- 13. Кубическая объемоцентрированная ? Низкие t0 плавления и кипения, малая твёрдость (Li, K, Na, Ba) Кубическая гранецентрированная
- 19. Тест 1) Какой металл при н.у. является жидким? А) Mg Б) Cd В) Hg Г) Pb
- 20. Интересные факты: 2 км самой тонкой золотой проволоки весят всего 1 г Сусальное золото в 4
- 21. Самый тугоплавкий металл – W, (вольфрам) tпл = 33800C Самый твёрдый металл – Cr(хром) приближенный по
- 22. Тест по теме «Положение металлов в ПСХЭ, их физические свойства» 1 вариант 1. В каких группах
- 23. 6. Электропроводность металлов обусловлена 1)скольжением слоев атом-ионов в кристаллах относительно друг друга 2)присутствием подвижных электронов в
- 25. Скачать презентацию
















 Кремний – химический элемент или природный дар
Кремний – химический элемент или природный дар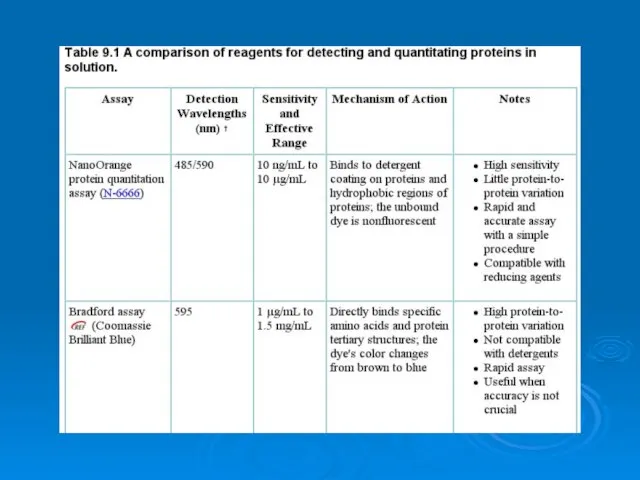 Analysis of proteins
Analysis of proteins Химическое равновесие. Примеры
Химическое равновесие. Примеры Сульфаниламидные препараты. Хинолоны
Сульфаниламидные препараты. Хинолоны Полимеры. Пластмассы
Полимеры. Пластмассы Амины. 10 класс
Амины. 10 класс Опис технологічного процесу отримання смол бекелітових рідких марок
Опис технологічного процесу отримання смол бекелітових рідких марок Ароматические углеводороды
Ароматические углеводороды Периодический закон Менделеева в действии
Периодический закон Менделеева в действии Агрегатные состояния веществ
Агрегатные состояния веществ Винная кислота
Винная кислота Вывод химических формул
Вывод химических формул Процесс диссоциации
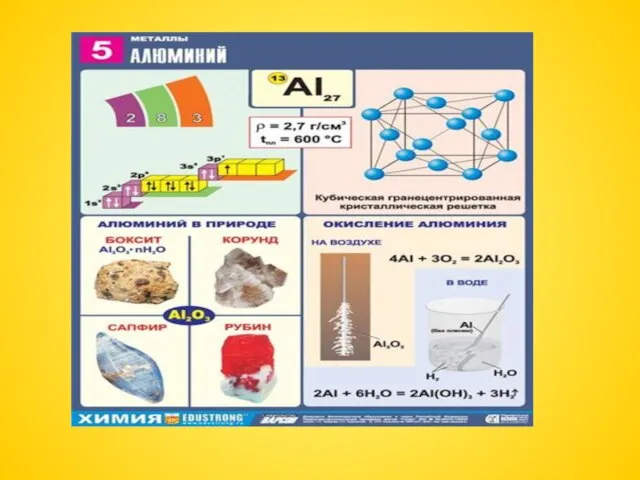
Процесс диссоциации Алюминий. Строение и свойства атома
Алюминий. Строение и свойства атома Соли азотной кислоты
Соли азотной кислоты Перициклические реакции
Перициклические реакции Искусственные полимеры
Искусственные полимеры Циклоалканы. Изомерия циклоалканов
Циклоалканы. Изомерия циклоалканов Презентация на тему Вычисления массовой доли растворенного вещества
Презентация на тему Вычисления массовой доли растворенного вещества  Строение и свойства циклоалканов
Строение и свойства циклоалканов Химическая связь
Химическая связь Средства декоративной косметики
Средства декоративной косметики Электролитическая диссоциация
Электролитическая диссоциация Взаимодействие элементов-неметаллов между собой. 8 класс
Взаимодействие элементов-неметаллов между собой. 8 класс Проектная работа Кристаллизация
Проектная работа Кристаллизация Названия и формулы кислот
Названия и формулы кислот Введение в химию. История химии
Введение в химию. История химии Химическая термодинамика
Химическая термодинамика