Содержание
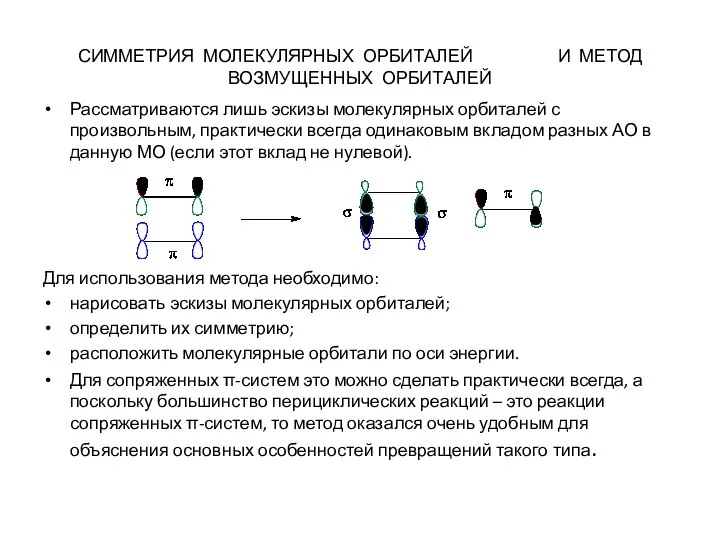
- 2. СИММЕТРИЯ МОЛЕКУЛЯРНЫХ ОРБИТАЛЕЙ И МЕТОД ВОЗМУЩЕННЫХ ОРБИТАЛЕЙ Рассматриваются лишь эскизы молекулярных орбиталей с произвольным, практически всегда
- 3. Теория возмущений молекулярных орбиталей Основной вопрос, на который отвечает теория ВМО: как будет изменяться энергия системы
- 4. Предполагается, что при перекрывании орбиталей реагирующих молекул две (или большее число) первоначально невозмущенные (базисные) орбитали взаимодействуют
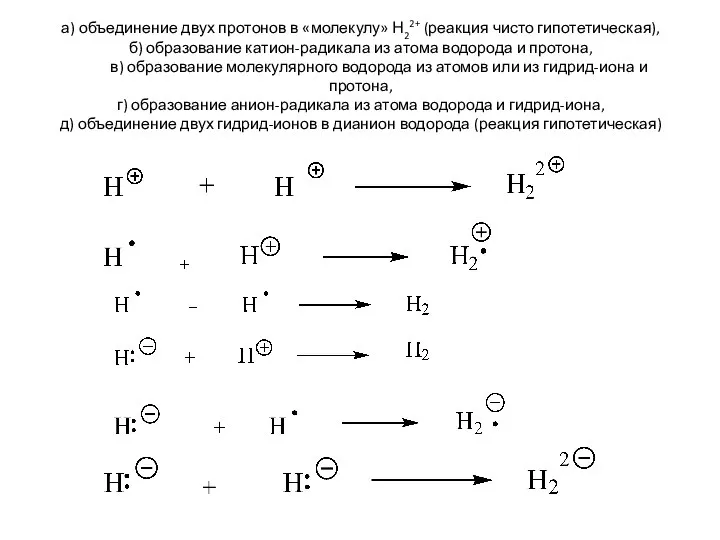
- 5. а) объединение двух протонов в «молекулу» Н22+ (реакция чисто гипотетическая), б) образование катион-радикала из атома водорода
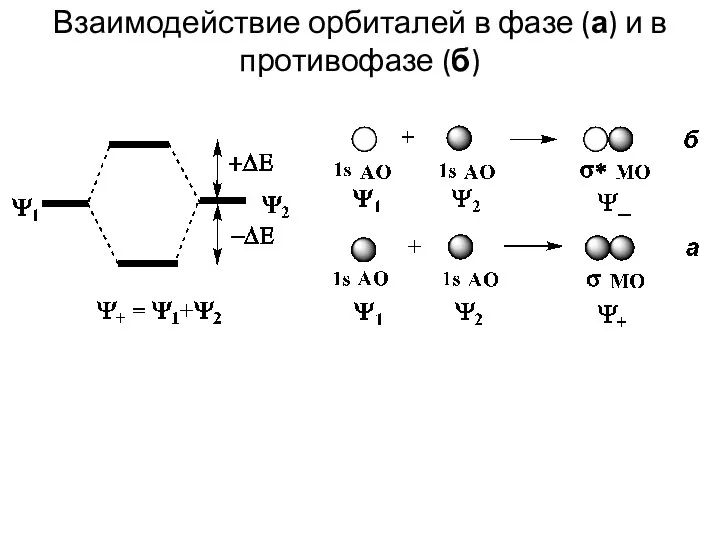
- 6. Во всех этих случаях сближающиеся частицы имеют по одной 1s-атомной орбитали (1s-АО). Согласно теории возмущения, при
- 7. Взаимодействие орбиталей в фазе (а) и в противофазе (б)
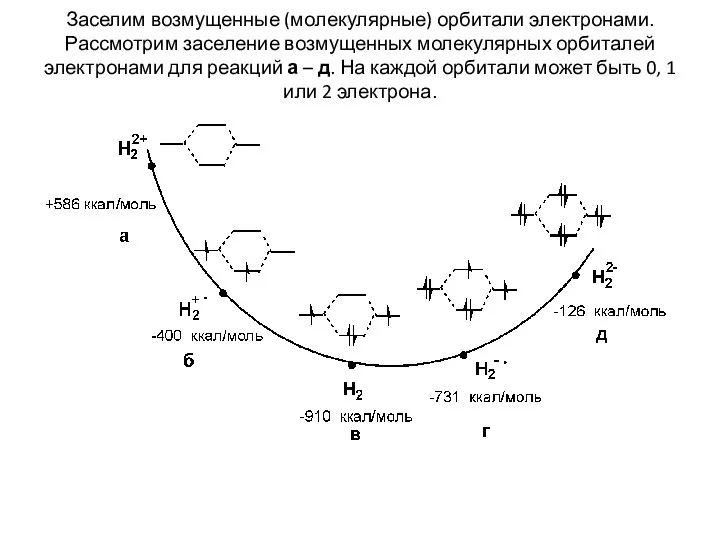
- 8. Заселим возмущенные (молекулярные) орбитали электронами. Рассмотрим заселение возмущенных молекулярных орбиталей электронами для реакций а – д.
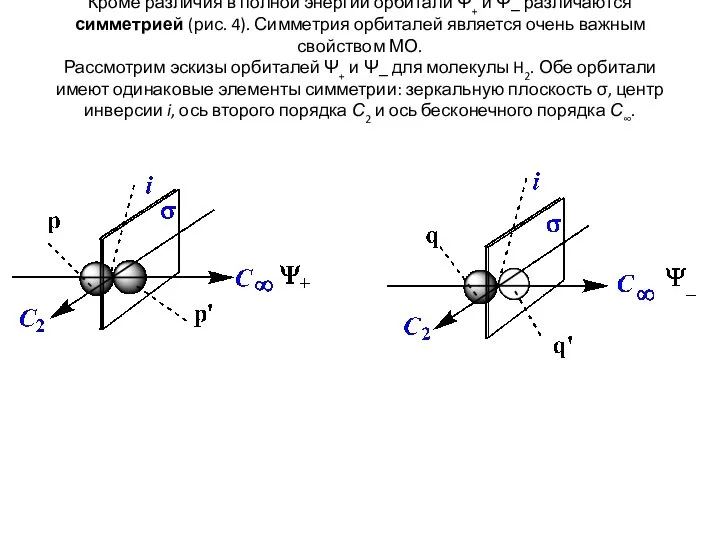
- 9. Кроме различия в полной энергии орбитали Ψ+ и Ψ_ различаются симметрией (рис. 4). Симметрия орбиталей является
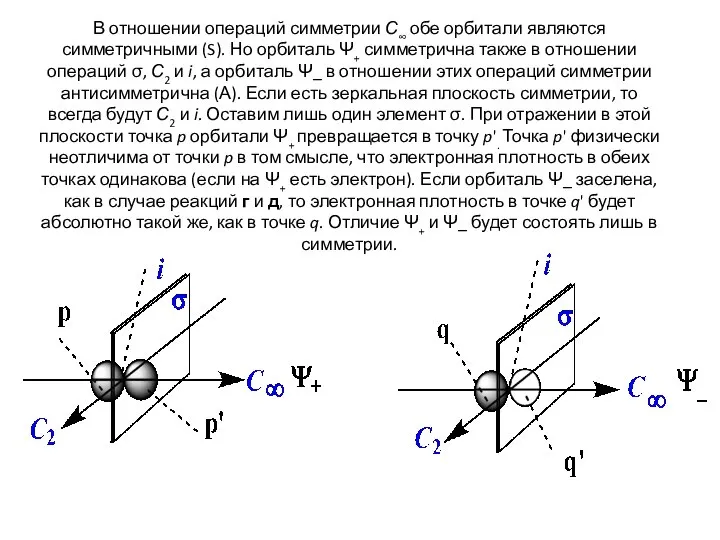
- 10. В отношении операций симметрии С∞ обе орбитали являются симметричными (S). Но орбиталь Ψ+ симметрична также в
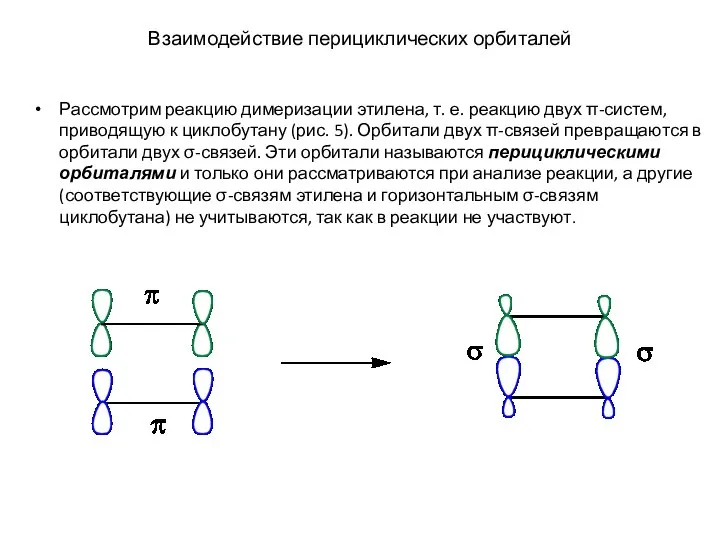
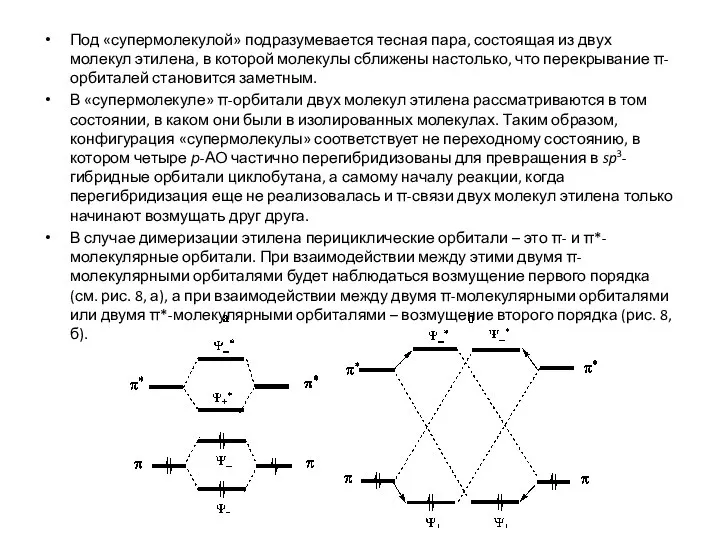
- 11. Взаимодействие перициклических орбиталей Рассмотрим реакцию димеризации этилена, т. е. реакцию двух π-систем, приводящую к циклобутану (рис.
- 12. Перициклические орбитали – это орбитали образующихся и разрывающихся связей. Возможность осуществления реакции при сближении двух молекул
- 13. Возмущение, описывающееся уравнениями (1), называется возмущением первого порядка. Базисные молекулярные орбитали имеют разную энергию (рис. 6,
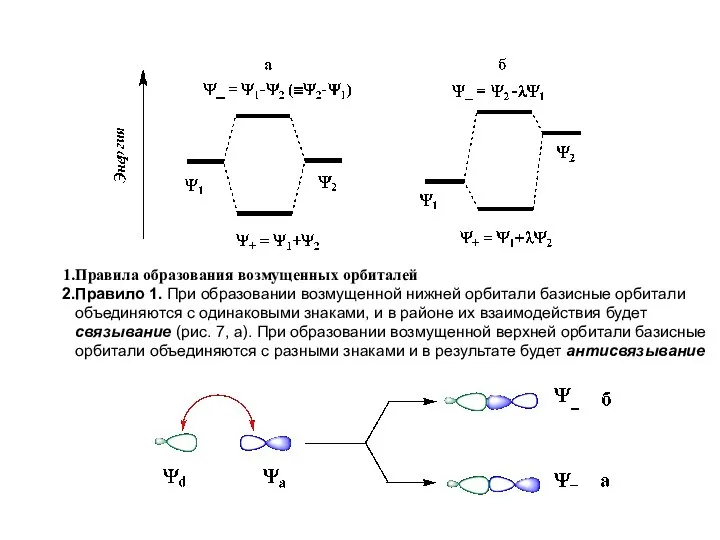
- 14. Правила образования возмущенных орбиталей Правило 1. При образовании возмущенной нижней орбитали базисные орбитали объединяются с одинаковыми
- 15. Правило 2. Если возмущенные орбитали имеют разную энергию, возмущение приводит к тому, что энергия орбиталей, первоначально
- 16. Под «супермолекулой» подразумевается тесная пара, состоящая из двух молекул этилена, в которой молекулы сближены настолько, что
- 17. Симметрия молекулярных орбиталей 2.2.1. Точечные группы симметрии Операции симметрии, которые будут рассмотрены, таковы, что, по крайней
- 18. Собственная ось симметрии. Все молекулы имеют ось С1, поскольку в любом случае поворот на 360о возвращает
- 20. Скачать презентацию








 Альдегиды. Номенклатура, изомерия. Получение альдегидов
Альдегиды. Номенклатура, изомерия. Получение альдегидов Относительная молекулярная масса
Относительная молекулярная масса Основные виды сырья для промышленности органического и нефтехимического синтеза
Основные виды сырья для промышленности органического и нефтехимического синтеза Обобщающий урок по теме «Соединения химических элементов» 8 класс.
Обобщающий урок по теме «Соединения химических элементов» 8 класс. Схема реакций
Схема реакций Технология производства пленок. Свойства полимерных пленочных материалов, модификация, применение
Технология производства пленок. Свойства полимерных пленочных материалов, модификация, применение Белки
Белки Реакции ионного обмена. Электролитическая диссоциация
Реакции ионного обмена. Электролитическая диссоциация Триады, октавы, спираль, таблица
Триады, октавы, спираль, таблица Сложные эфиры. Жиры
Сложные эфиры. Жиры Олеиновая кислота
Олеиновая кислота Элементы и атомы, В менделеевский взяты круг Сделали химию самой богатой И самой творческой из наук.
Элементы и атомы, В менделеевский взяты круг Сделали химию самой богатой И самой творческой из наук. Презентация на тему Вычисления массовой доли растворенного вещества
Презентация на тему Вычисления массовой доли растворенного вещества  Презентация на тему Органическая химия. История развития
Презентация на тему Органическая химия. История развития  Коррозия металлов (9 класс)
Коррозия металлов (9 класс) Виведення плям органічного походження
Виведення плям органічного походження Элемент первой группы, калий
Элемент первой группы, калий Презентация на тему Химическое равновесие
Презентация на тему Химическое равновесие  Сталь 12Х18Н10Т
Сталь 12Х18Н10Т Презентация на тему Аммиак
Презентация на тему Аммиак  ОГЭ химия. Основной государственный экзамен
ОГЭ химия. Основной государственный экзамен Флотационный способ обогащения
Флотационный способ обогащения Определение содержания солей в воде
Определение содержания солей в воде Презентация на тему Подготовка к ЕГЭ. Полезно знать
Презентация на тему Подготовка к ЕГЭ. Полезно знать  Пластификация пластмасс
Пластификация пластмасс Презентация на тему Растворы
Презентация на тему Растворы  Абсорбционная осушка газа
Абсорбционная осушка газа Презентация на тему Соединения серы
Презентация на тему Соединения серы