Содержание
- 2. При изучении любых химических систем используют термодинамический и кинетический подход. В термодинамическом подходе рассматривают конечное и
- 3. Термодинамическая система – тело или группа тел, которые нас интересуют, все остальное – окружающая среда. По
- 4. Первое Начало утверждает, что теплота, переданная системе, идет на увеличение ее внутренней энергии и на работу
- 5. ИЗМЕНЕНИЕ ЭНТАЛЬПИИ СИСТЕМЫ В ХОДЕ ХИМИЧЕСКИХ РЕАКЦИЙ
- 6. Закон Кирхгофа гласит, что температурный коэффициент теплового эффекта химической реакции равен изменению теплоемкости системы в ходе
- 7. Поскольку многие химические процессы являются обратимыми, т.е. протекают в прямом и обратном направлении, необходимо помнить, что
- 8. НАПРАВЛЕННОСТЬ САМОПРОИЗВОЛЬНОГО ПРОТЕКАНИЯ ПРОЦЕССА Стремление системы к минимуму энергии – не единственная причина возможности самопроизвольного протекания
- 9. S = k ln W S – энтропия (функция состояния), от греч.trope – обращение, изменение. Размерность
- 10. ВТОРОЕ НАЧАЛО ТЕРМОДИНАМИКИ. ЭНЕРГИЯ ГИББСА . В ИЗОЛИРОВАННОЙ СИСТЕМЕ ВОЗМОЖНЫ ТОЛЬКО ТАКИЕ ПРОЦЕССЫ, КОТОРЫЕ СОПРОВОЖДАЮТСЯ РОСТОМ
- 11. ЭНЕРГИЯ ГИББСА
- 13. Скачать презентацию
Слайд 2При изучении любых химических систем используют термодинамический и кинетический подход. В термодинамическом
При изучении любых химических систем используют термодинамический и кинетический подход. В термодинамическом

Расчет изменения значений некоторых функций в заданных условиях позволяет сделать вывод о теоретической возможности самопроизвольного протекания какого-либо процесса в данной системе или указать условия, при которых этот процесс возможен.
В кинетическом подходе главное внимание уделяется описанию пути процесса из исходного в конечное состояние (например, стадии реакции, промежуточные вещества, скорость процесса или отдельных его стадий и т.д.).
Исторически термодинамика, как раздел физики, возникла при изучении теплоты, работы и температуры. В термодинамике стали использовать определенные приемы для описания различных процессов, которые используются и для описания химических реакций, так появилась химическая термодинамика.
Таким образом, химическая термодинамика изучает условия устойчивости химических систем и закономерности их перехода из одного состояния в другое и оперирует следующими основными понятиями:
Слайд 3Термодинамическая система – тело или группа тел, которые нас интересуют, все остальное
Термодинамическая система – тело или группа тел, которые нас интересуют, все остальное

изолированные системы – которые не обмениваются ни веществом (массой), ни энергией с окружающей средой;
закрытые (замкнутые) системы - с окружающей средой веществом не обмениваются, но могут обмениваться энергией (обычно, в виде теплоты);
открытые системы – системы, которые обмениваются с окружающей средой и энергией, и веществом. Это реальные, наиболее часто встречающиеся и наиболее сложные системы. Очень часто, теоретически описывая процессы, считают, что они протекают в изолированных или закрытых системах, как в наиболее простых.
Для описания состояния системы пользуются параметрами состояния: T - температура, P - давление, V – объем, n – количество моль, иногда концентрации Ci. Параметры состояния взаимосвязаны, их взаимосвязь – уравнение состояния.
Например, уравнение состояния идеального газа: pV = nRT.
Слайд 4Первое Начало утверждает, что теплота, переданная системе, идет на увеличение ее внутренней
Первое Начало утверждает, что теплота, переданная системе, идет на увеличение ее внутренней

ΔQ = ΔU + ΔA = ΔU + pΔV ( ΔA = pΔV )
ΔU имеет размерность [Дж]
V = const → QV = ΔU => в случае изохорного процесса теплота, переданная системе идет на увеличение ее внутренней энергии
p = const → ΔQp = ΔU + pΔV = Δ(U + pV)
U + pV ≡ H → U = H – pV
ΔH – энтальпия (теплосодержание, от греч. enthalpein - нагревать), размерность [кДж/моль], функция состояния, функция экстенсивная – зависит от количества вещества.
ΔQp = ΔU + pΔV = ΔH => при изобарном процессе теплота, переданная системе, идет на увеличение ее энтальпии.
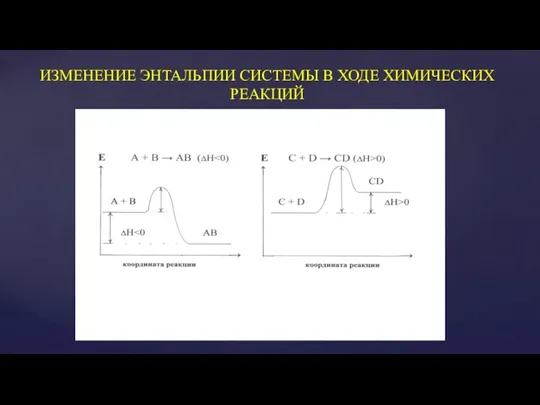
ΔH ˃0 эндотермический процесс, тепло поглощается;
ΔH˂0 экзотермический процесс, тепло выделяется.
ПЕРВОЕ НАЧАЛО ТЕРМОДИНАМИКИ
Слайд 5ИЗМЕНЕНИЕ ЭНТАЛЬПИИ СИСТЕМЫ В ХОДЕ ХИМИЧЕСКИХ РЕАКЦИЙ
ИЗМЕНЕНИЕ ЭНТАЛЬПИИ СИСТЕМЫ В ХОДЕ ХИМИЧЕСКИХ РЕАКЦИЙ
Слайд 6Закон Кирхгофа гласит, что температурный коэффициент теплового эффекта химической реакции равен изменению
Закон Кирхгофа гласит, что температурный коэффициент теплового эффекта химической реакции равен изменению

aA + bB+ … → dD + eE+…
ΔH2 = ΔH1+ ΔCp(T2 – T1),
где ΔH2 и ΔH1 - энтальпии процессов при T1 и T2 соответственно (ΔT невелико).
ΔCp = [dCp(D) + e dCp(E)+….] – [aCp(A)+ bCp(B)+…],
ΔCp(X) – молярная теплоемкость веществ, участвующих в реакции при постоянном давлении (p=const), размерность ΔCp(X) - [Дж/моль•К].
QV = ΔU = nCVΔT, где CV - молярная теплоемкость веществ, участвующих в реакции при постоянном объеме (V =const).
ЗАКОН КИРХГОФА
Слайд 7Поскольку многие химические процессы являются обратимыми, т.е. протекают в прямом и обратном
Поскольку многие химические процессы являются обратимыми, т.е. протекают в прямом и обратном

∆Нпр = - ∆ Нобр,
где ∆Нпр и ∆Нобр – тепловые эффекты (энтальпии) прямой и обратной реакции.
Почему наблюдаются тепловые эффекты при протекании реакций?
Существование тепловых эффектов реакций обусловлено неравенством внутренних энергий реагентов (Up) и продуктов реакций (Uпр), как следует из определения энтальпии: ∆Н=(Uпр-Up)+ p(Vпр-Vp). Чем больше различие (Uпр-Up), тем значительнее величина теплового эффекта ∆Н, работа расширения может отсутствовать. Неравенство внутренних энергий реагентов и продуктов реакции обусловлено различием энергий их химических связей, именно это различие является главной причиной теплового эффекта. Этот вывод подтверждается расчетами величин ΔН с использованием значений энергий связей продуктов и реагентов.
ЭНТАЛЬПИЯ
Слайд 8 НАПРАВЛЕННОСТЬ САМОПРОИЗВОЛЬНОГО ПРОТЕКАНИЯ ПРОЦЕССА
Стремление системы к минимуму энергии – не единственная
НАПРАВЛЕННОСТЬ САМОПРОИЗВОЛЬНОГО ПРОТЕКАНИЯ ПРОЦЕССА Стремление системы к минимуму энергии – не единственная

Слайд 9S = k ln W
S – энтропия (функция состояния), от греч.trope
S = k ln W
S – энтропия (функция состояния), от греч.trope

С ростом температуры энтропия всегда возрастает. Возрастает она и при переходе твердое состояние → жидкое → газообразное. В ходе химических реакций энтропия может как возрастать, так и убывать. Δ S функция экстенсивная, зависит от количества вещества.
CaCO3 (тв) →CaO(тв) + CO2(газ) ΔS˃0; N2(газ) + 3 H2(газ) → 2NH3 (газ) Δ S˂0
М.Планк (1911 г.) «Энтропия идеального кристалла при абсолютном нуле равна нулю».
ЭНТРОПИЯ
Слайд 10ВТОРОЕ НАЧАЛО ТЕРМОДИНАМИКИ. ЭНЕРГИЯ ГИББСА
.
В ИЗОЛИРОВАННОЙ СИСТЕМЕ ВОЗМОЖНЫ ТОЛЬКО ТАКИЕ ПРОЦЕССЫ, КОТОРЫЕ
ВТОРОЕ НАЧАЛО ТЕРМОДИНАМИКИ. ЭНЕРГИЯ ГИББСА
.
В ИЗОЛИРОВАННОЙ СИСТЕМЕ ВОЗМОЖНЫ ТОЛЬКО ТАКИЕ ПРОЦЕССЫ, КОТОРЫЕ

ΔH = ΔG + TΔS (T, p = const ). ΔG = ̶ Амах Если ΔG ˂0 процесс возможен;
если ΔG ˃0 процесс не возможен.
ΔG = ΔH - TΔS (T,p =const).
H2 (газ) + 1/2 O2 (газ) = H2O (ж) ΔH = ̶ 16,3 кДж При низких температурах TΔS мало и
|ΔH |˃˃|TΔS|, а ΔG ≈ ̶ ΔH;
H2 (газ) + 1/2 O2 (газ) → H2O (ж) ;
При высоких температурах Т – велика, следовательно, |ΔH |˂˂|TΔS| и ΔG ≈ ̶ TΔS
H2 (газ) + 1/2 O2 (газ) ← H2O (ж)
Слайд 11
ЭНЕРГИЯ ГИББСА
ЭНЕРГИЯ ГИББСА

 Учение о химических процессах. Лекция 3
Учение о химических процессах. Лекция 3 Жиры. Техническая переработка жиров
Жиры. Техническая переработка жиров Презентация на тему Химия в медицине
Презентация на тему Химия в медицине  Минеральные компоненты молока и молочных продуктов. Макроэлементы
Минеральные компоненты молока и молочных продуктов. Макроэлементы Технологические особенности никеля и никелевых сплавов
Технологические особенности никеля и никелевых сплавов Процесс электролиза
Процесс электролиза Основы химического анализа. Лекция 7
Основы химического анализа. Лекция 7 Биотит и тальк
Биотит и тальк Микроструктура железоуглеродистых сплавов в равновесном состоянии
Микроструктура железоуглеродистых сплавов в равновесном состоянии Великий кислород
Великий кислород Опыты с водой
Опыты с водой Презентация на тему Химические свойства металлов
Презентация на тему Химические свойства металлов  Вещества молекулярного и немолекулярного строения
Вещества молекулярного и немолекулярного строения Свойства растворов электролитов
Свойства растворов электролитов ЛК 2_окислительно-восстановительные процессы
ЛК 2_окислительно-восстановительные процессы Budowa pasmowa ciał stałych
Budowa pasmowa ciał stałych 5 группа элементов
5 группа элементов Окислительно-восстановительные реакции
Окислительно-восстановительные реакции Анализ стабильности экологических характеристик товарных дизельных топлив после перекачки
Анализ стабильности экологических характеристик товарных дизельных топлив после перекачки Решение задач ЕГЭ
Решение задач ЕГЭ Шуточные загадки Периодической системы химических элементов
Шуточные загадки Периодической системы химических элементов Равновесия в растворах электролитов. Окислительно-восстановительные реакции
Равновесия в растворах электролитов. Окислительно-восстановительные реакции Вымораживание воды
Вымораживание воды Тренажер. Химические свойства солей
Тренажер. Химические свойства солей хим связь
хим связь Агрегатные состояния веществ
Агрегатные состояния веществ Метиловый спирт
Метиловый спирт Органическая химия и пищевые добавки
Органическая химия и пищевые добавки