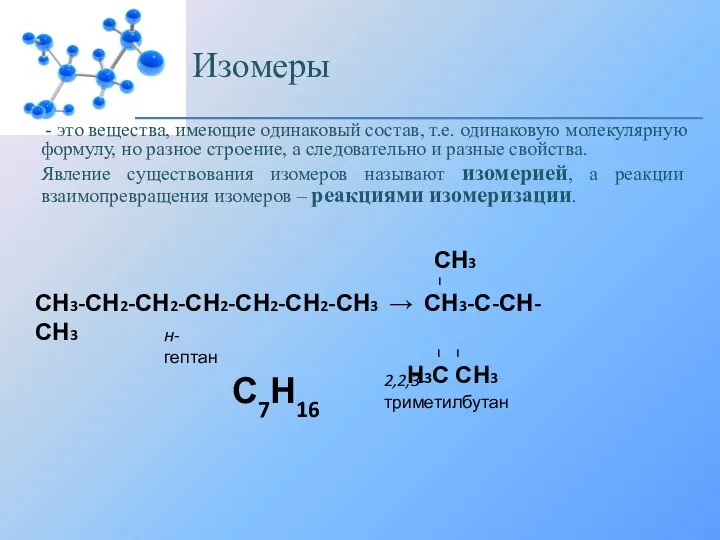
луженых чайниках, которыми снабжали русскую армию.
Морозной зимой 1916 г. партия олова была отправлена по железной дороге с Дальнего Востока в европейскую часть России, но в назначенное место прибыли не серебристо-белые слитки, а мелкий серый порошок.
За четыре года до этого произошла катастрофа с британской экспедицией Роберта Фолкона Скотта.
Достигнув географической точки Южного полюса, Скотт обнаружил остатки чужого лагеря и палатку с флагом норвежской экспедиции под руководством Руала Амундсена, которая побывала там ровно за месяц до этого.
Разочарованный Скотт и его товарищи отправились в обратный путь, но не обнаружили топлива в одной канистре, потом в другой... Они не могли обогреться и приготовить пищу. Топливо вытекло из канистр сквозь швы, пропаянные оловом. Скотт и четверо его товарищей погибли в жестоких снегах Антарктиды.
В начале XX века в Петербурге на складе военного оборудования произошла скандальная история: во время ревизии к ужасу интенданта выяснилось, что оловянные пуговицы для солдатских мундиров исчезли, а ящики, в которых они хранились, доверху заполнены серым порошком. И хотя на складе был лютый холод, горе-интенданту стало жарко. Спасло бедолагу заключение химической лаборатории, куда ревизоры направили содержимое ящиков: "Присланное вами для анализа вещество, несомненно, олово. Очевидно, в данном случае имело место явление, известное в химии под названием "оловянная чума".
-39°С

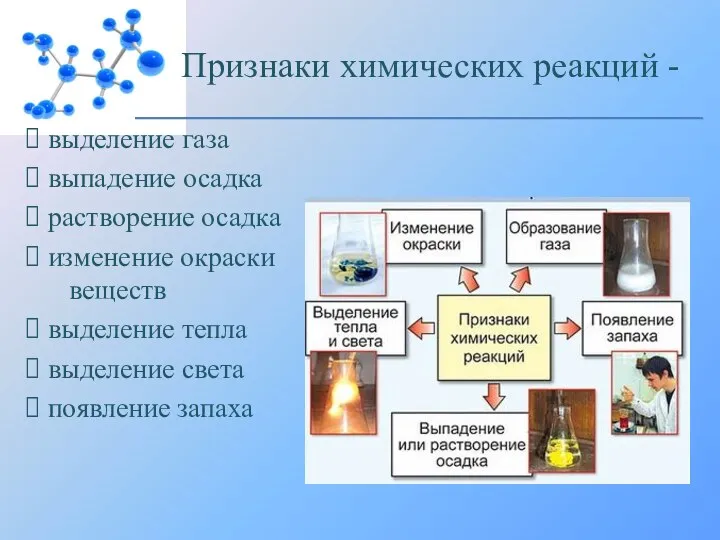



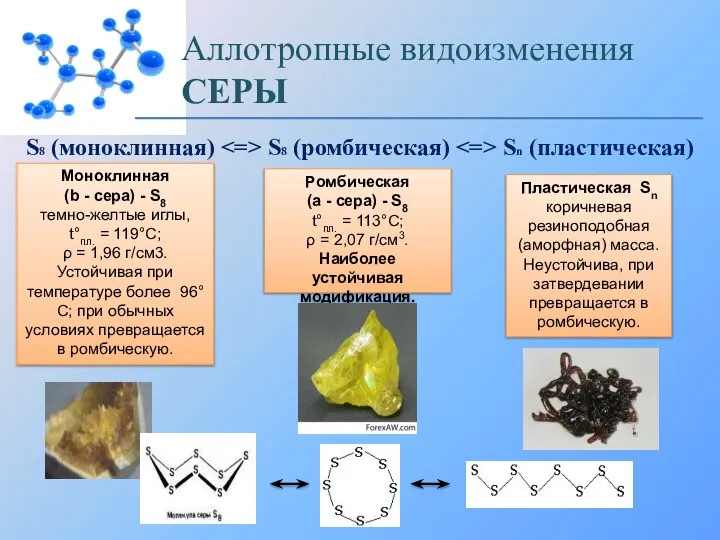
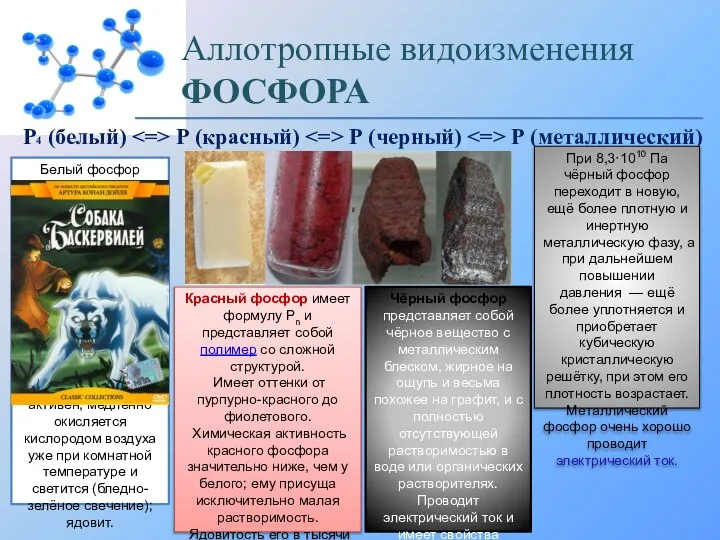



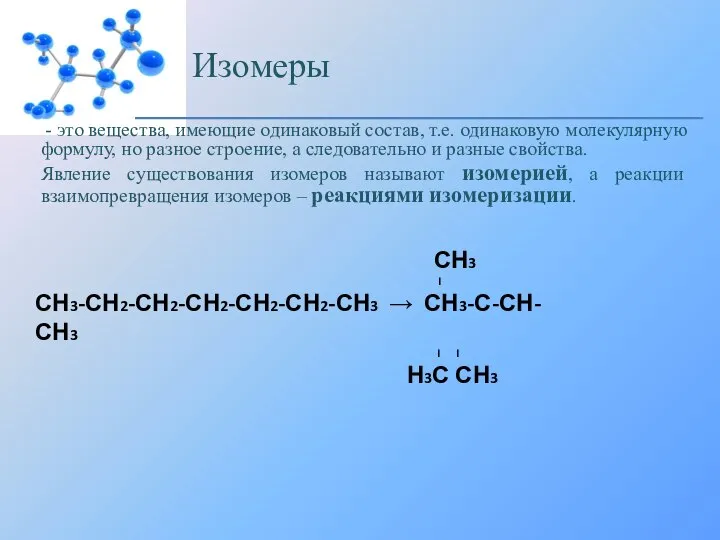
 Вымораживание воды
Вымораживание воды Галогены. Свойства фтора, брома, йода
Галогены. Свойства фтора, брома, йода Железо как химический элемент
Железо как химический элемент Углеводы
Углеводы Презентация на тему Электролитическая диссоциация (8 класс)
Презентация на тему Электролитическая диссоциация (8 класс)  Алюминий и сплавы алюминия
Алюминий и сплавы алюминия Периодический закон Д.И. Менделеева
Периодический закон Д.И. Менделеева Презентация на тему Палладий
Презентация на тему Палладий  Коллоидно-химическая теория схватывания и твердения вяжущих веществ
Коллоидно-химическая теория схватывания и твердения вяжущих веществ Новейшие достижения в области высокомолекулярных соединений
Новейшие достижения в области высокомолекулярных соединений Углерод и его свойства
Углерод и его свойства Презентация на тему Химические волокна
Презентация на тему Химические волокна  Соединения алюминия
Соединения алюминия Ресурс Лови оксиды для систематизации знаний, умений, навыков по теме Оксиды
Ресурс Лови оксиды для систематизации знаний, умений, навыков по теме Оксиды Электролиз
Электролиз Превращения веществ
Превращения веществ Периодическая система химических элементов. Периоды. Группы
Периодическая система химических элементов. Периоды. Группы Знаки химических элементов
Знаки химических элементов Химическая кинетика. Экзаменационные вопросы
Химическая кинетика. Экзаменационные вопросы СПИРТЫ, ФЕНОЛЫ
СПИРТЫ, ФЕНОЛЫ Презентация на тему Общая характеристика неметаллов
Презентация на тему Общая характеристика неметаллов  Методы защиты металлов от электрохимической коррозии. Классификация методов защиты
Методы защиты металлов от электрохимической коррозии. Классификация методов защиты Презентация на тему Спирты (9 класс)
Презентация на тему Спирты (9 класс)  Процесс образования неметаллических включений в стали
Процесс образования неметаллических включений в стали Многообразие веществ
Многообразие веществ Биосинтез пиримидиновых нуклеотидов
Биосинтез пиримидиновых нуклеотидов Химические свойства основных оксидов. 9 класс
Химические свойства основных оксидов. 9 класс Предельные углеводороды (алканы)
Предельные углеводороды (алканы)