Содержание
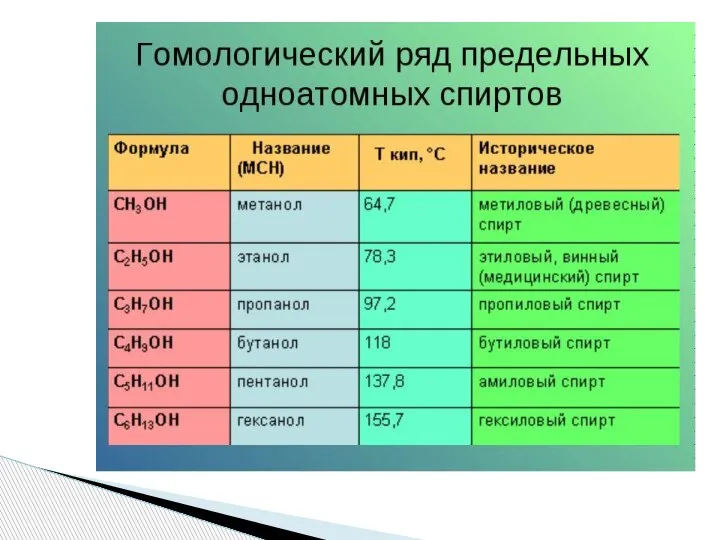
- 2. Предельные одноатомные спирты
- 3. 1. Состав 2. Строение 3. Химические свойства 4. Получение 5. Применение План работы
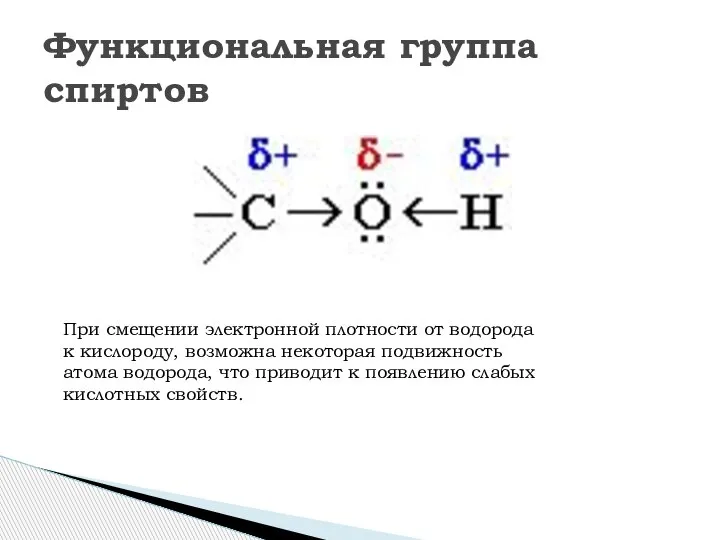
- 5. Функциональная группа спиртов При смещении электронной плотности от водорода к кислороду, возможна некоторая подвижность атома водорода,
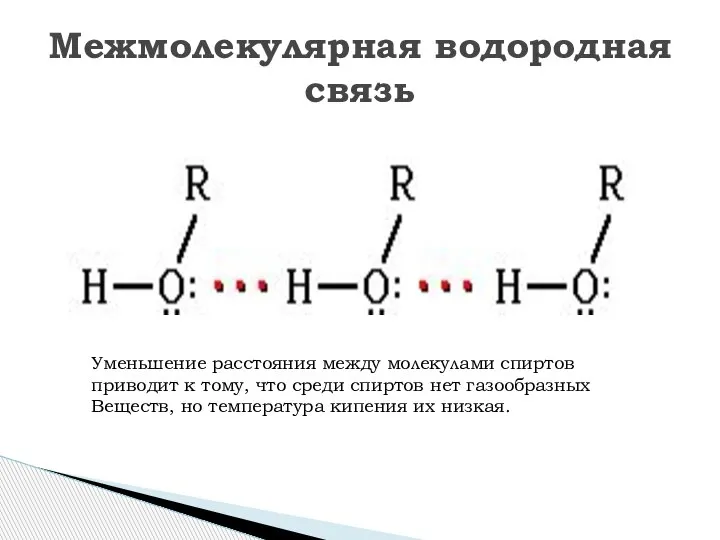
- 6. Межмолекулярная водородная связь Уменьшение расстояния между молекулами спиртов приводит к тому, что среди спиртов нет газообразных
- 7. Номенклатура спиртов Систематические названия даются по названию углеводорода с добавлением суффикса -ол и цифры, указывающей положение
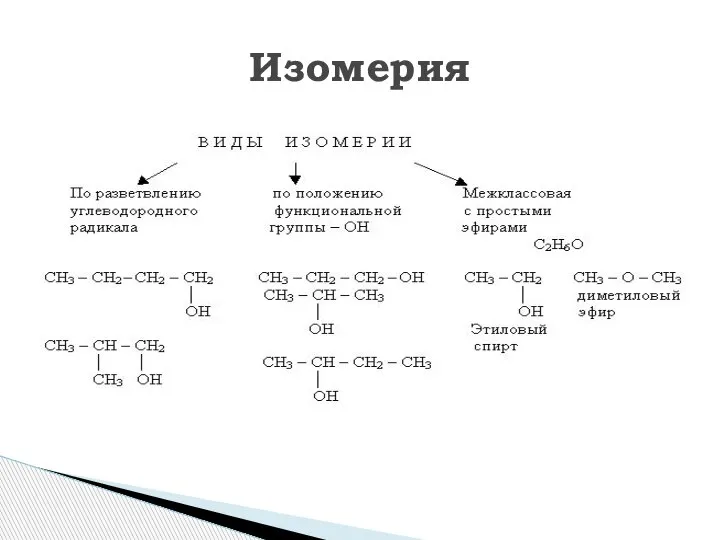
- 8. Изомерия
- 9. Химические свойства спиртов 1. Взаимодействие с галогеноводородами, подобно взаимодействию щелочей с кислотами 2. Дегидротация А). Межмолекулярная
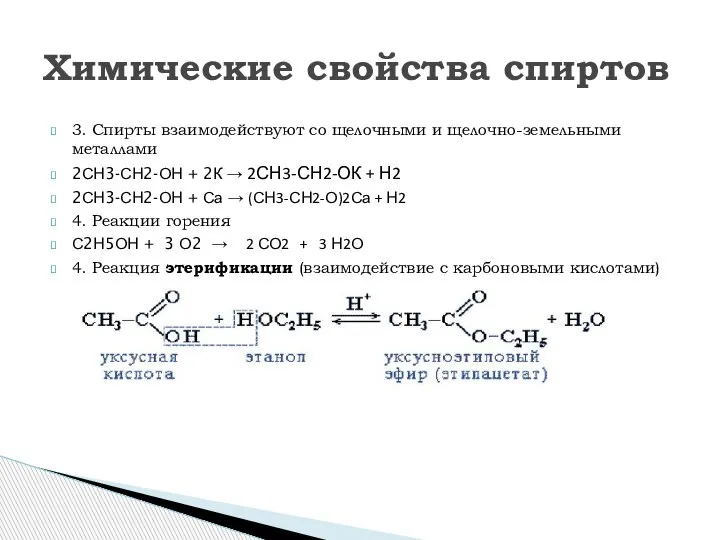
- 10. 3. Спирты взаимодействуют со щелочными и щелочно-земельными металлами 2СН3-СН2-ОН + 2К → 2СН3-СН2-ОК + Н2 2СН3-СН2-ОН
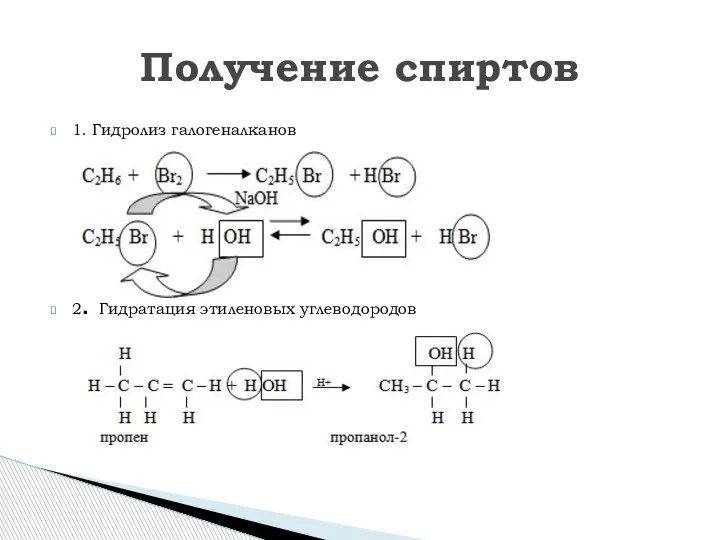
- 11. 1. Гидролиз галогеналканов 2. Гидратация этиленовых углеводородов Получение спиртов
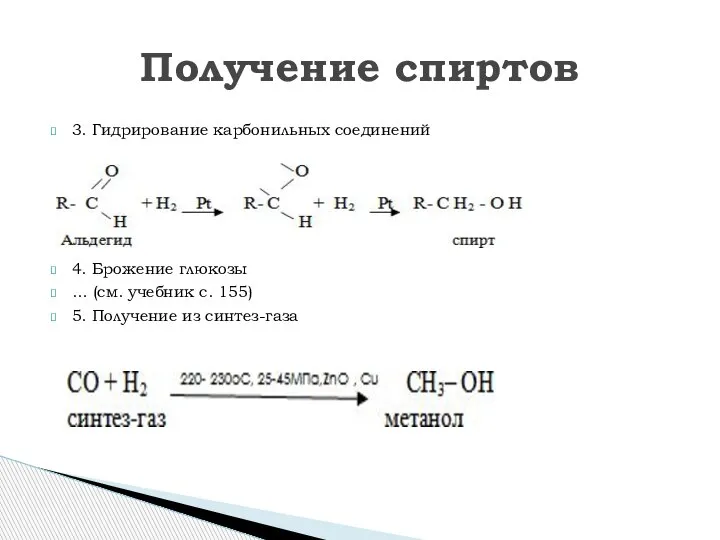
- 12. 3. Гидрирование карбонильных соединений 4. Брожение глюкозы … (см. учебник с. 155) 5. Получение из синтез-газа
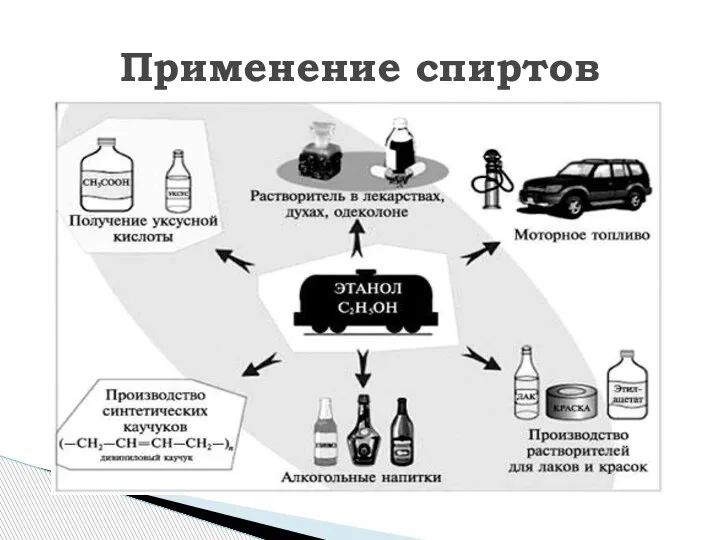
- 13. Применение спиртов
- 14. 1. Общая формула предельных одноатомных спиртов а) CnH2n+2 б) CnH2n в) CnH2n-2 г) CnH2n+1OH Проверь себя
- 15. 2. Функциональная группа предельных одноатомных спиртов а) - СНО б) - СООН в) - ОН г)
- 16. 3. Реакции по разрыву связи в гидроксогруппе а) с галогенами; б) с кислородом; в) с активными
- 17. 4. Реакция с отрывом гидроксогруппы а) окисление; б) гидрирование; в) гидратация; г) дегидратация (+) Проверь себя
- 18. 1. г 2. в 3. в 4. г Ответы:
- 20. Скачать презентацию









 Сложные эфиры. Жиры. Мыла
Сложные эфиры. Жиры. Мыла Щелочные металлы
Щелочные металлы Решение задач на основные законы и понятия химии
Решение задач на основные законы и понятия химии prezentatsia_lektsia_1_LF_Rastvory_Kolligativnye_svoi_774_stva_rastvorov_Osmos
prezentatsia_lektsia_1_LF_Rastvory_Kolligativnye_svoi_774_stva_rastvorov_Osmos Презентация на тему Интерактивная игра "Химический лабиринт"
Презентация на тему Интерактивная игра "Химический лабиринт"  Оценка пригодности природной воды в качестве питьевой по формуле М.Г. Курлова
Оценка пригодности природной воды в качестве питьевой по формуле М.Г. Курлова Проверочные работы по темам: Неметаллы. 9 класс
Проверочные работы по темам: Неметаллы. 9 класс Современные области применения изотопной продукции
Современные области применения изотопной продукции ОВР
ОВР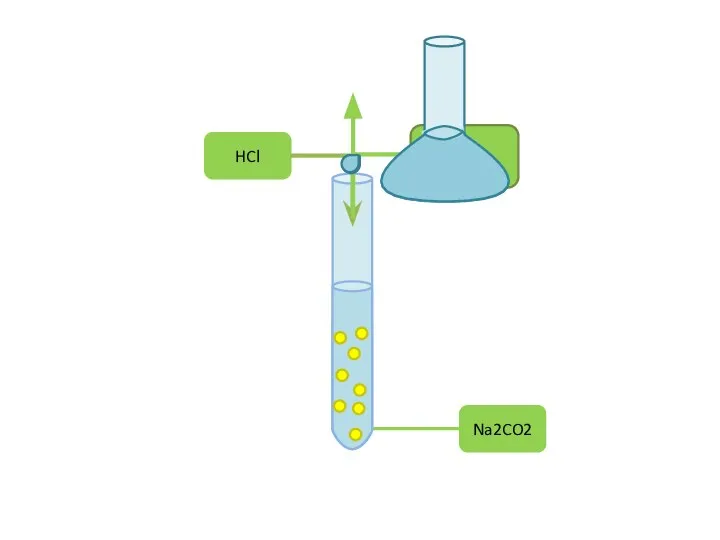 Хімічний експеримент
Хімічний експеримент Коррозия металла
Коррозия металла Химический алфавит. Алфавит
Химический алфавит. Алфавит Фепромарон. Химическое название
Фепромарон. Химическое название Типы химических реакций. Реакции обмена
Типы химических реакций. Реакции обмена Стекло
Стекло Техника титрования и лабораторная посуда
Техника титрования и лабораторная посуда Углерод. 9 класс
Углерод. 9 класс 10_KhimiaKlassifikatsia_organicheskikh_soedieniy (1)
10_KhimiaKlassifikatsia_organicheskikh_soedieniy (1) Обмен и функции нуклеотидов
Обмен и функции нуклеотидов Презентации 1 строение атома
Презентации 1 строение атома Окислительно-восстановительные реакции
Окислительно-восстановительные реакции История создания периодической таблицы
История создания периодической таблицы Спирты
Спирты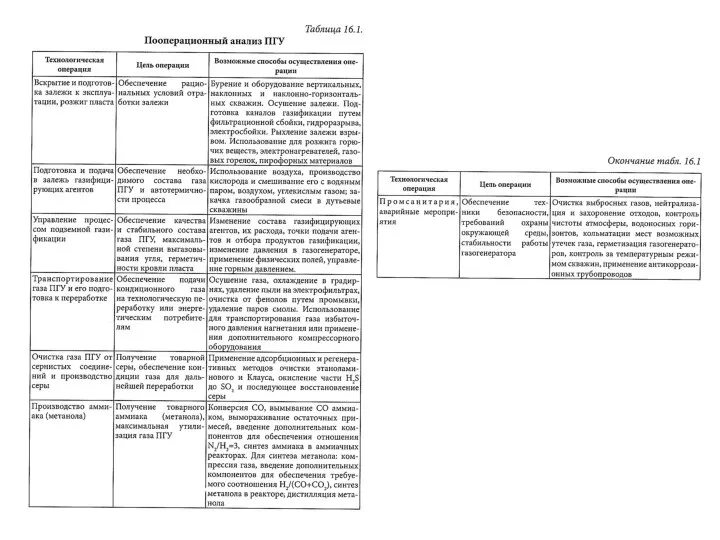 Пооперационный анализ ПГУ
Пооперационный анализ ПГУ Термореактивные пластмассы (реактопласты)
Термореактивные пластмассы (реактопласты)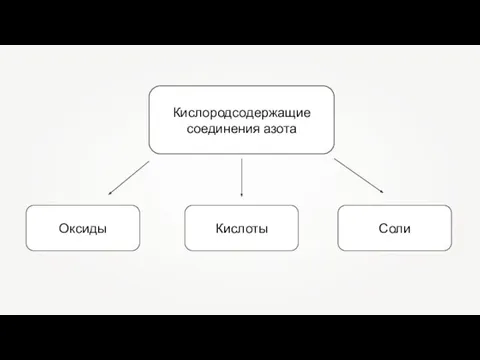 Кислородсодержащие соединения азота
Кислородсодержащие соединения азота Обобщение по теме Теория химического строения органических веществ
Обобщение по теме Теория химического строения органических веществ Презентация на тему Минеральные вещества
Презентация на тему Минеральные вещества