Содержание
- 2. В ходе урока учащиеся должны: — проводить стехиометрические расчеты по уравнению реакции; — вычислять количество или
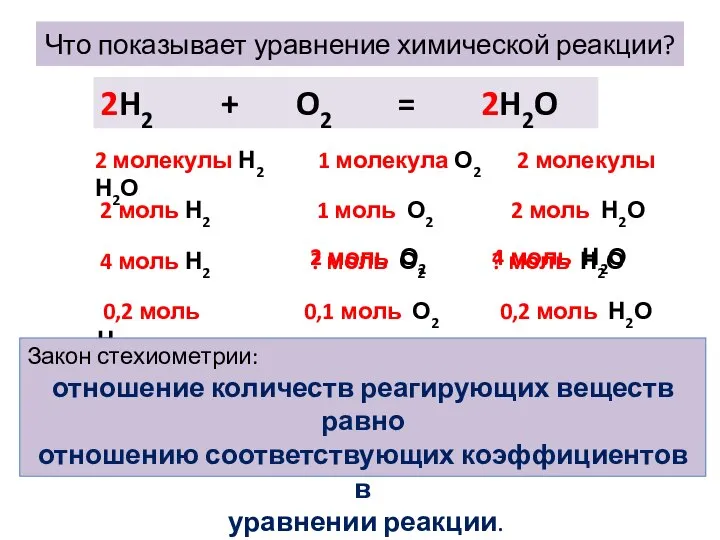
- 3. Что показывает уравнение химической реакции? 2H2 + O2 = 2H2O 2 молекулы Н2 1 молекула О2
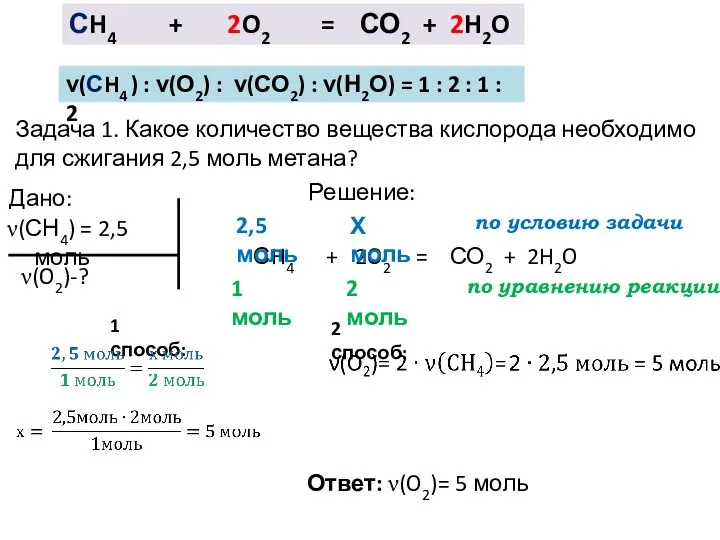
- 4. СH4 + 2O2 = СО2 + 2H2O ν(СH4 ) : ν(О2) : ν(СО2) : ν(Н2О) =
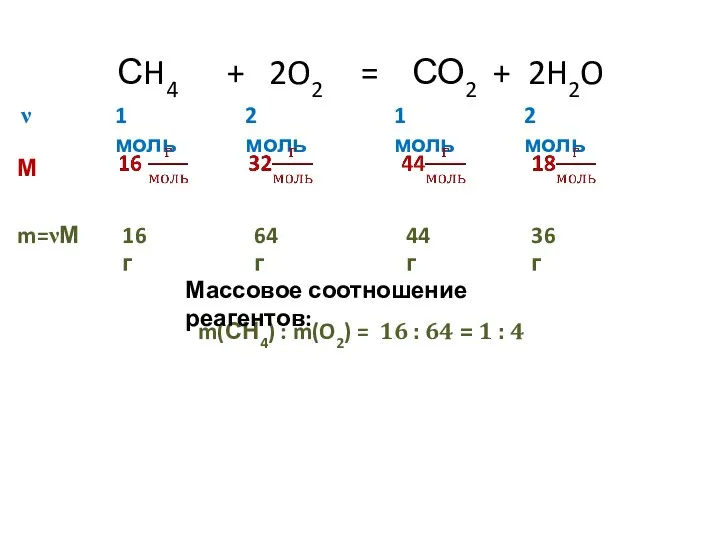
- 5. СH4 + 2O2 = СО2 + 2H2O 1 моль 2 моль 1 моль 2 моль ν
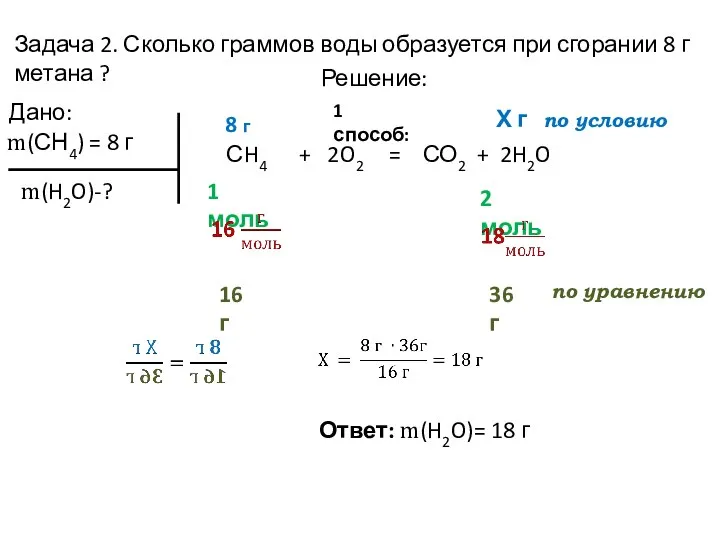
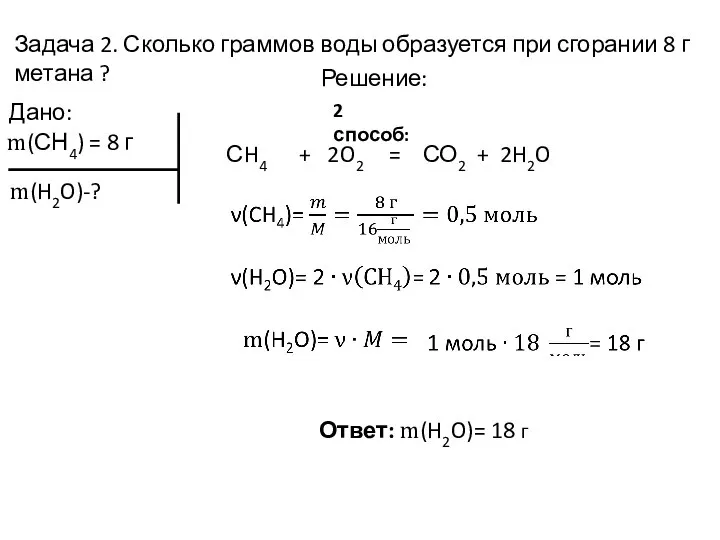
- 6. Задача 2. Сколько граммов воды образуется при сгорании 8 г метана ? Дано: m(СН4) = 8
- 7. Задача 2. Сколько граммов воды образуется при сгорании 8 г метана ? Дано: m(СН4) = 8
- 8. Какая масса оксида железа (II, III) образуется при сгорании в кислороде 5,6 г железа? 1) записать
- 10. Скачать презентацию


 Презентация на тему Менделеев Дмитрий Иванович
Презентация на тему Менделеев Дмитрий Иванович  Классификация оганических соединений. 10 класс
Классификация оганических соединений. 10 класс Алифатические соединения. Тема № 6
Алифатические соединения. Тема № 6 Нуклеиновые кислоты
Нуклеиновые кислоты Презентация по Химии "Ароматические углеводороды в природе. Области их применения"
Презентация по Химии "Ароматические углеводороды в природе. Области их применения"  Вычисление температур стеклования полимера при различных степенях отверждения смолы
Вычисление температур стеклования полимера при различных степенях отверждения смолы Гидролиз солей
Гидролиз солей Метод высокоэффективной жидкостной хроматографии и тандемной масс-спектрометрии
Метод высокоэффективной жидкостной хроматографии и тандемной масс-спектрометрии Спирты
Спирты Воздух и его свойства
Воздух и его свойства Подготовка к контрольной работе
Подготовка к контрольной работе Металлы побочных подгрупп
Металлы побочных подгрупп Важнейшие классы неорганических соединений
Важнейшие классы неорганических соединений Важнейшие классы неорганических соединений
Важнейшие классы неорганических соединений Презентация на тему Электролиз: что полезно знать
Презентация на тему Электролиз: что полезно знать  ОВР
ОВР Нахождение формулы вещества по массовым долям элементов
Нахождение формулы вещества по массовым долям элементов Химия — это наука о веществах, их свойствах и превращениях
Химия — это наука о веществах, их свойствах и превращениях Атомно-емісійна спектрометрія з індуктивно-зв’язаною плазмою та рентгенофлуоресцентний аналіз
Атомно-емісійна спектрометрія з індуктивно-зв’язаною плазмою та рентгенофлуоресцентний аналіз Альфа- и бета- распад. Правило смещения
Альфа- и бета- распад. Правило смещения nukleinovye_kisloty
nukleinovye_kisloty lll-l группы главные подгруппы. 11 класс
lll-l группы главные подгруппы. 11 класс Халькогены. Электронное строение кислорода и серы
Халькогены. Электронное строение кислорода и серы Фосфорная кислота и ее свойства
Фосфорная кислота и ее свойства Типы химических реакций в органической химии
Типы химических реакций в органической химии Закон сохранения массы веществ. 8 класс
Закон сохранения массы веществ. 8 класс Соединения железа
Соединения железа 12_BROMATOMETRIYa_NITRITOMETRIYa
12_BROMATOMETRIYa_NITRITOMETRIYa