Содержание
- 2. Спирты – это производные углеводородов, где один или несколько водородных атомов замещены на гидроксогруппу.
- 3. Гомологический ряд спиртов
- 4. Функциональная группа спиртов При смещении электронной плотности от водорода к кислороду, возможна некоторая подвижность атома водорода,
- 5. Водородная связь Уменьшение расстояния между молекулами спиртов приводит к тому, что среди спиртов нет газообразных Веществ,
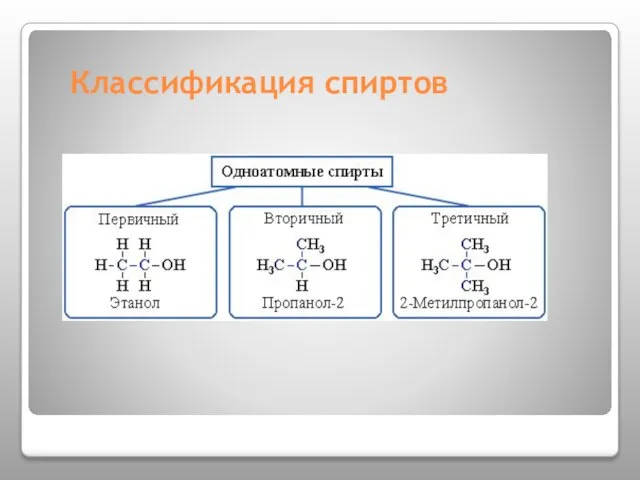
- 6. Классификация спиртов
- 8. Номенклатура спиртов Систематические названия даются по названию углеводорода с добавлением суффикса -ол и цифры, указывающей положение
- 9. Изомерия спиртов 1. Для спиртов характерна структурная изомерия: изомерия положения ОН-группы (начиная с С3) 2. углеродного
- 10. Химические свойства спиртов 1. Взаимодействие с галогеноводородами, подобно взаимодействию щелочей с кислотами 2. Дегидратация. А) внутримолекулярная
- 11. Б) межмолекулярная 3. Горение С2Н5ОН + 3 О2 → 2 СО2 + 3 Н2О С3Н7ОН +
- 12. 4. Спирты взаимодействуют со щелочными и щелочно-земельными металлами 2СН3-СН2-ОН + 2К → 2СН3-СН2-ОК + Н2 2СН3-СН2-ОН
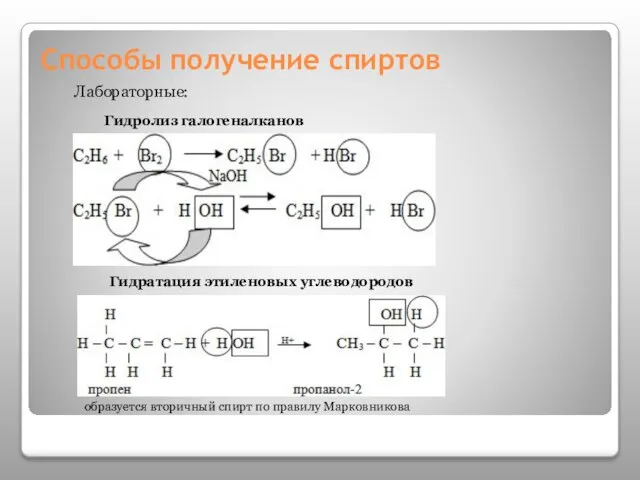
- 13. Способы получение спиртов Лабораторные: Гидролиз галогеналканов Гидратация этиленовых углеводородов образуется вторичный спирт по правилу Марковникова
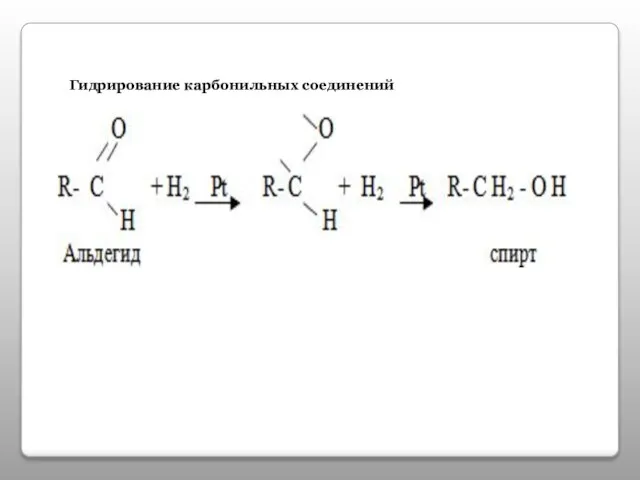
- 14. Гидрирование карбонильных соединений
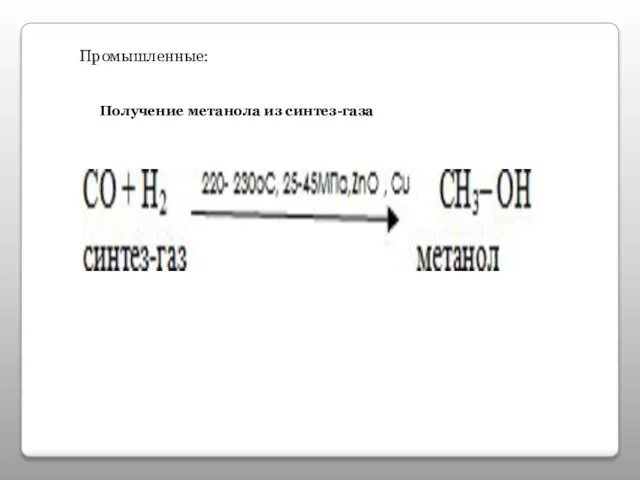
- 15. Промышленные: Получение метанола из синтез-газа
- 16. Применение спиртов Получение лекарств
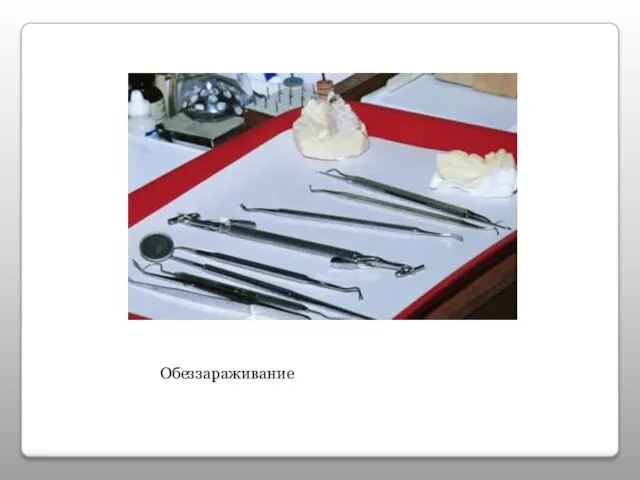
- 17. Обеззараживание
- 18. Производство лаков и красок
- 19. При проведении клинического анализа крови
- 20. В качестве автомобильного топлива
- 21. Как добавка к реактивному топливу
- 22. В качестве растворителя
- 23. Сырье для получения каучука
- 24. Сырье для производства уксусной кислоты
- 25. Проверь себя 1. Общая формула предельных одноатомных спиртов а) CnH2n+2 б) CnH2n в) CnH2n-2 г) CnH2n+1OH
- 26. 2. Функциональная группа предельных одноатомных спиртов а) - СНО б) - СООН в) - ОН г)
- 27. 3. Реакции по разрыву связи в гидроксогруппе а) с галогенами; б) с кислородом; в) с активными
- 29. Скачать презентацию





















 Роль ионов в неживой природе и в жизни людей
Роль ионов в неживой природе и в жизни людей Развитие энергетики и проблемы изменения структуры использования углеводородного сырья
Развитие энергетики и проблемы изменения структуры использования углеводородного сырья Изготовление индикаторной бумаги
Изготовление индикаторной бумаги Липиды молока и молочных продуктов. Группы липидов
Липиды молока и молочных продуктов. Группы липидов Металлы и их соединения
Металлы и их соединения Кислород. 8 класс
Кислород. 8 класс Стан електронів у атомі
Стан електронів у атомі Общая характеристика элементов VII группы главной подгруппы. Хлор
Общая характеристика элементов VII группы главной подгруппы. Хлор Великий кислород
Великий кислород Оценка качества пищевой соли, реализуемой в розничной торговле
Оценка качества пищевой соли, реализуемой в розничной торговле Электроотрицательность (ЭО)
Электроотрицательность (ЭО) Химическая коррозия
Химическая коррозия teoria_Butlerova
teoria_Butlerova Пространственная изомерия органических соединений
Пространственная изомерия органических соединений Презентация на тему Химические средства гигиены и косметика
Презентация на тему Химические средства гигиены и косметика  Органическая химия
Органическая химия Соли в свете теории электролитической диссоциации (ТЭД)
Соли в свете теории электролитической диссоциации (ТЭД) Плазменное состояние вещества
Плазменное состояние вещества Алгоритмы при изучении химии
Алгоритмы при изучении химии Явления, происходящие с веществами
Явления, происходящие с веществами Презентация на тему Природные источники углеводородов (9 класс)
Презентация на тему Природные источники углеводородов (9 класс)  Тесты для самопроверки
Тесты для самопроверки Презентация на тему Полимеры и их получение
Презентация на тему Полимеры и их получение  Презентация на тему Неорганічні речовини живих організмів
Презентация на тему Неорганічні речовини живих організмів  Непредельные углеводороды. Алкадиены. Уроки 22-23
Непредельные углеводороды. Алкадиены. Уроки 22-23 Порох: из грязи в князи
Порох: из грязи в князи Использование информационноко-ммуникационных технологий по формированию УУД на уроках химии
Использование информационноко-ммуникационных технологий по формированию УУД на уроках химии Валентность
Валентность