† 23. September 1882 in Göttingen)
Ab 1820 studierte er Medizin in Marburg und Heidelberg, ab 1821 auch Chemie bei Gmelin. 1823 schloss er sein Medizinstudium in Heidelberg mit Promotion ab und konzentrierte sich fortan nur noch auf die Chemie. In dieser Zeit waren die Grenzen zwischen Philosophie und Naturwissenschaft mangels genauerer Kenntnisse nur vage ausgeprägt. Gmelin war so beeindruckt von Wöhlers experimentellem Geschick bei der Isolierung von Dicyan und Cyanursäure, dass er ihm ein Praktikum bei Berzelius in Stockholm vermittelte.
Wöhler gilt als Pionier der organischen Chemie wegen seiner Synthese von Oxalsäure durch Hydrolyse von Dicyan 1824[4] und von Harnstoff aus Ammoniumcyanat im Jahre 1828. Diese Synthesen eröffneten das Feld der Biochemie, da zum ersten Mal Stoffe, die bisher nur von lebenden Organismen bekannt waren, aus „unbelebter“ Materie künstlich erzeugt werden konnten
Wöhler ist auch bekannt als Entdecker der Synthese von Calciumcarbid (1862, identifizierte auch dessen Hydrolyseprodukt Ethin), von Benzoesäure aus Benzaldehyd und von Hydrochinon aus Chinon. Ferner gelang ihm die Isolierung von Nickel aus Arsennickel.
Korrespondierendes Mitglied der Russischen Akademie der Wissenschaften in Sankt Petersburg seit dem 9. Dezember 1853





















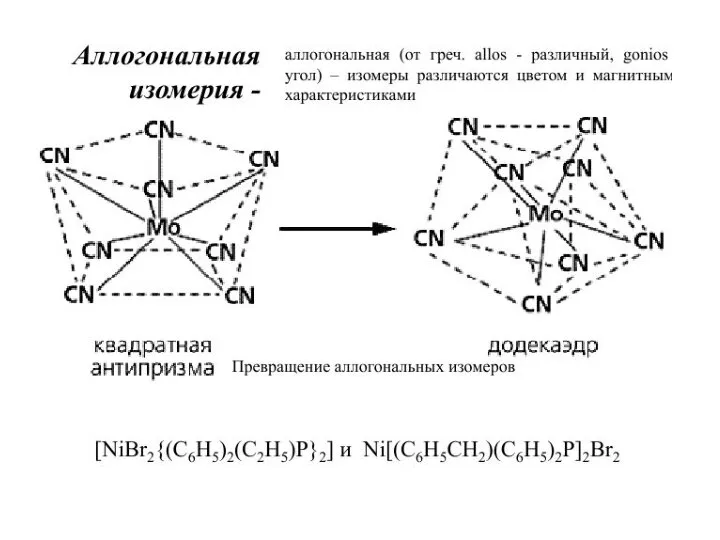
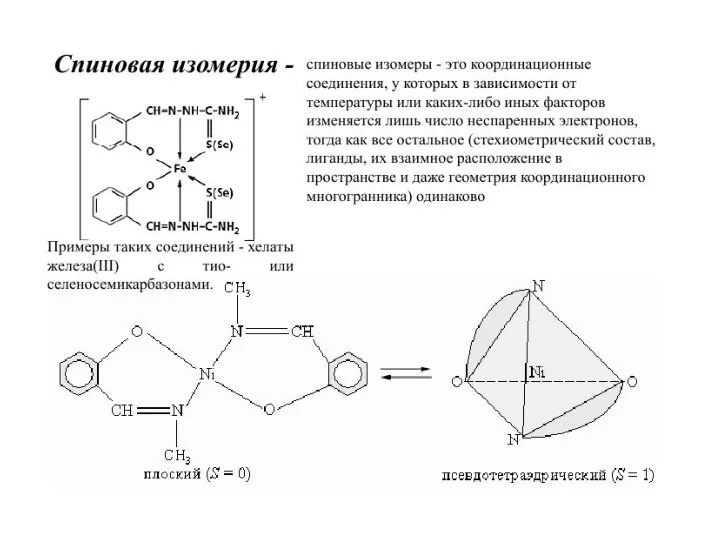
![Cu(I)[Mo(V)(CN)6] и Cu(II)[Mo(IV)(CN)6]](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1042866/slide-48.jpg)
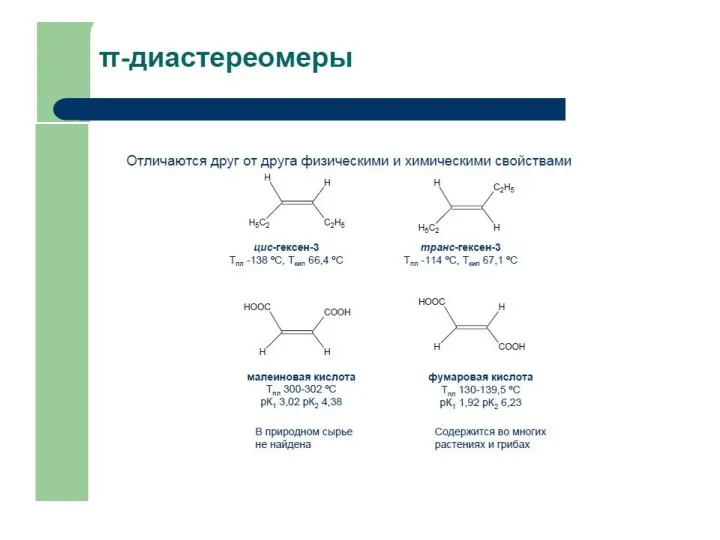
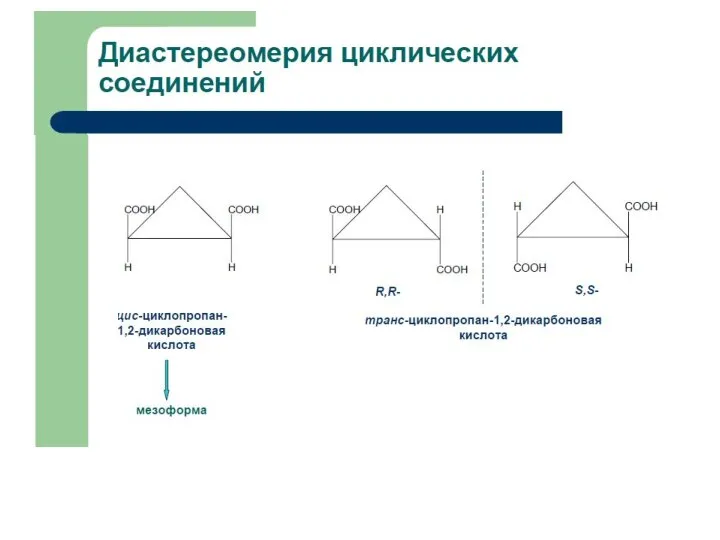
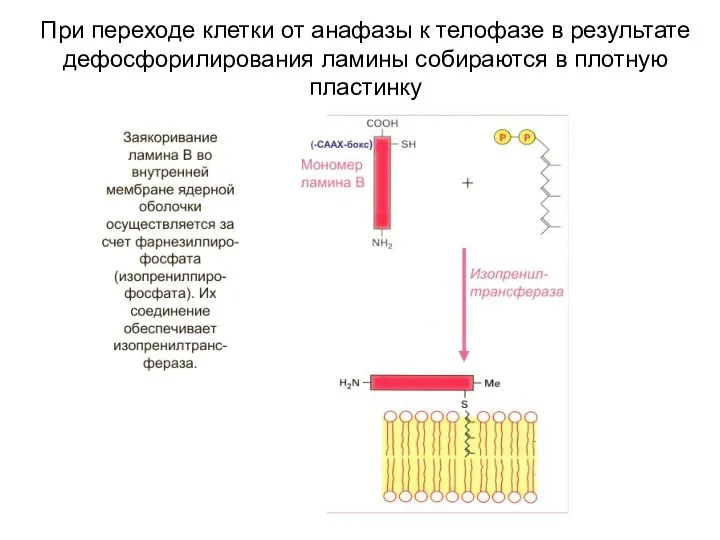






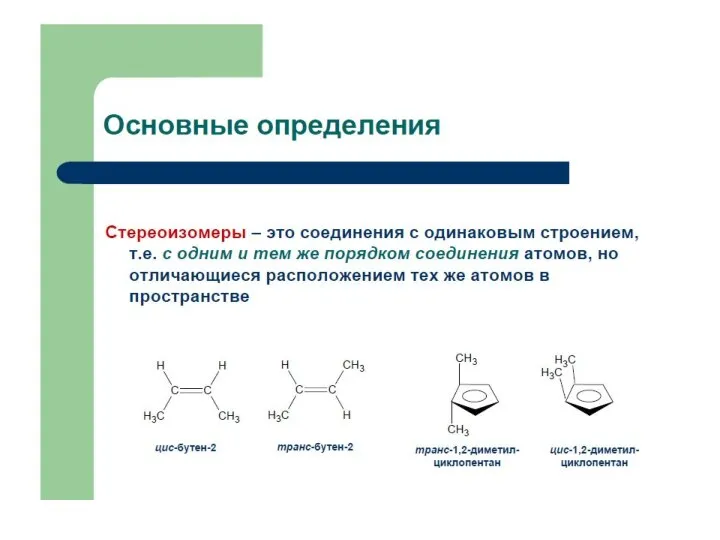
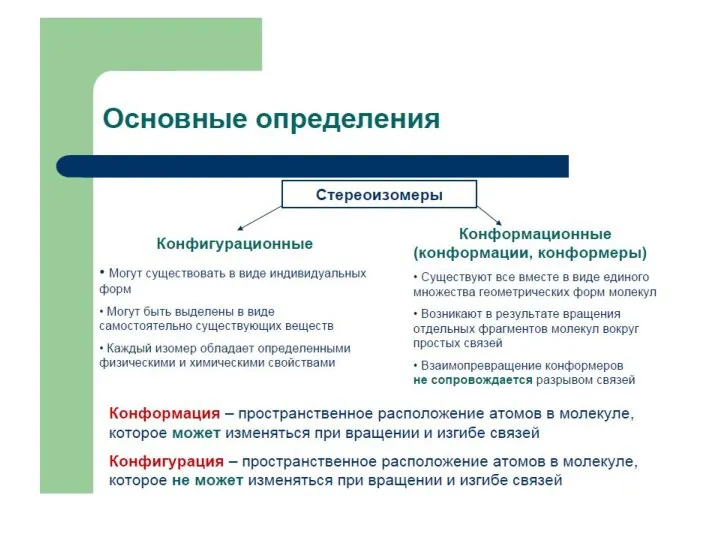
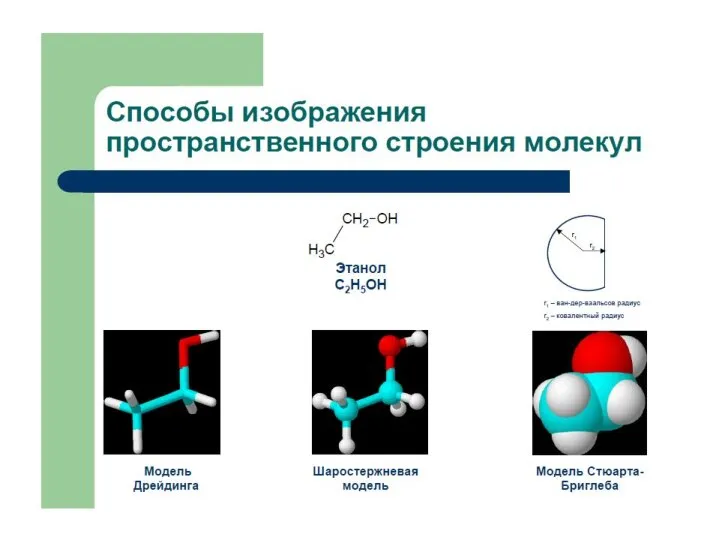
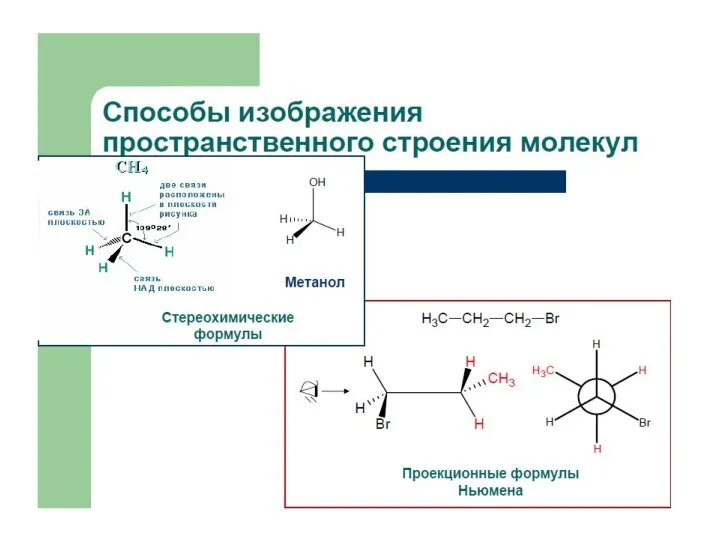
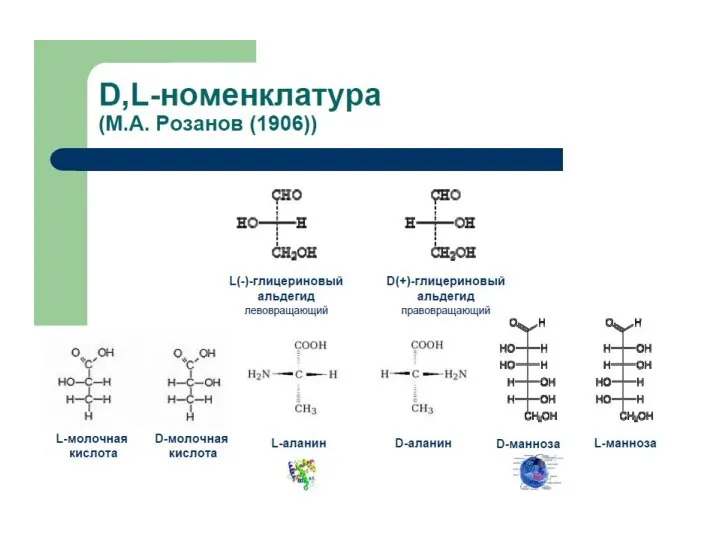
 Химические формулы
Химические формулы 9-8 кислоты в свете ТЭД (1)
9-8 кислоты в свете ТЭД (1) Спирты
Спирты Адсорбционно-десорбционные взаимодействия фосфатов кальция и аминокислот
Адсорбционно-десорбционные взаимодействия фосфатов кальция и аминокислот Соли как производные кислот и оснований
Соли как производные кислот и оснований Интерактивная интеллектуальная игра Юный химик
Интерактивная интеллектуальная игра Юный химик Класс оксиды
Класс оксиды Обобщение знаний об углеводородах
Обобщение знаний об углеводородах ЕГЭ по химии: документы, регламентирующие структуру и содержание контрольных измерительных материалов
ЕГЭ по химии: документы, регламентирующие структуру и содержание контрольных измерительных материалов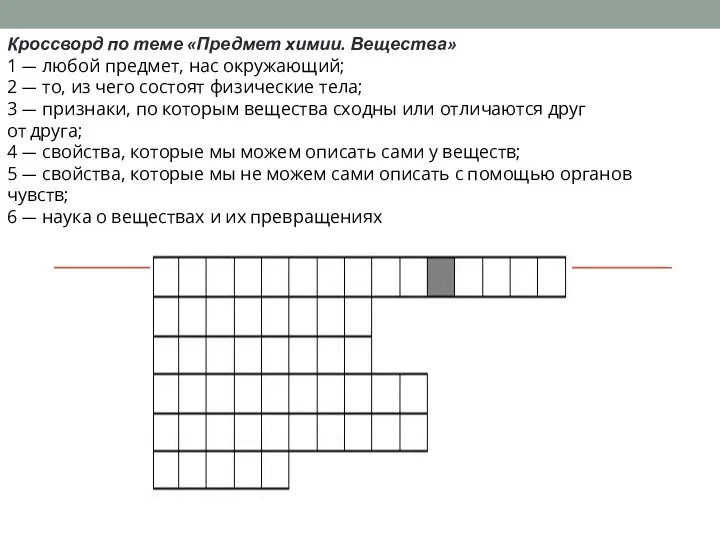 Предмет химии. Вещества
Предмет химии. Вещества 3bc28ca0711047a6880d20a6763f17db
3bc28ca0711047a6880d20a6763f17db Общая характеристика оксидов
Общая характеристика оксидов Золото
Золото Органическая химия. Ароматические углеводороды
Органическая химия. Ароматические углеводороды Методы получения нафтиридинов (всех изомеров)
Методы получения нафтиридинов (всех изомеров) Нефть и её переработка
Нефть и её переработка Оксид кремния
Оксид кремния Основания: номенклатура, классификация, применение, физические свойства
Основания: номенклатура, классификация, применение, физические свойства Алмаз. Свойства алмазов
Алмаз. Свойства алмазов Презентация на тему Соединения серы
Презентация на тему Соединения серы  Свойства солей, оксидов, оснований
Свойства солей, оксидов, оснований Модель химического образования на основе технологического подхода. Методическая система учителя химии
Модель химического образования на основе технологического подхода. Методическая система учителя химии Техника титрования и лабораторная посуда
Техника титрования и лабораторная посуда Уровень С1 в ГИА
Уровень С1 в ГИА Задачи. Периодическая система. Строение атома. Повторение
Задачи. Периодическая система. Строение атома. Повторение Азотсодержащие гетероциклические соединения пиррол
Азотсодержащие гетероциклические соединения пиррол Предельные углеводороды. Тест 19
Предельные углеводороды. Тест 19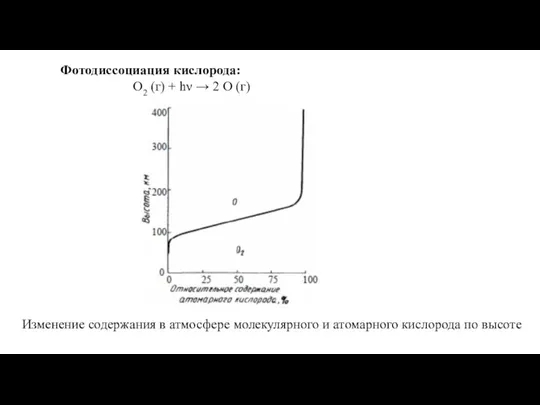 Фотодиссоциация кислорода
Фотодиссоциация кислорода