Содержание
- 2. Тема нашего урока – «Великий кислород»
- 3. План урока: Нахождение в природе. 2. Общая характеристика химического элемента кислорода. 3. Кислород – простое вещество.
- 4. Цель урока: доказать, что кислород вездесущ, всемогущ и невидим.
- 5. Нахождение в природе
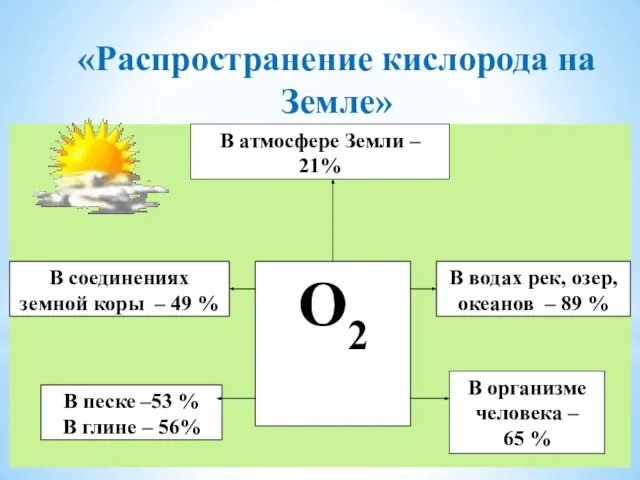
- 6. «Распространение кислорода на Земле»
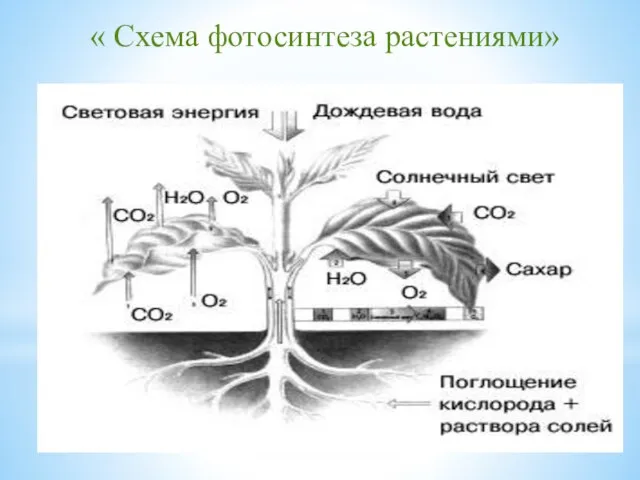
- 7. « Схема фотосинтеза растениями»
- 8. 2. Общая характеристика химического элемента кислорода.
- 9. План характеристика химического элемента: 1. Символ. 2. Положение в ПСХЭ — группа, период, порядковый номер. 3.
- 10. 3. Кислород – простое вещество. Физические свойства кислорода
- 11. Молекула кислорода образована двумя атомами. Химическая формула – О2 Относительная молекулярная масса: Mr (О2)= 32
- 12. ФИЗИЧЕСКИЕ СВОЙСТВА КИСЛОРОДА Кислород – газ, без цвета, без вкуса и без запаха. малорастворим в воде
- 13. 4. История открытия кислорода.
- 14. Трактат китайского алхимика Мао Хао (8век). Китайцы называли «деятельное начало», входящее в состав воздуха, «йын». Труды
- 15. Портрет Джозефа Пристли
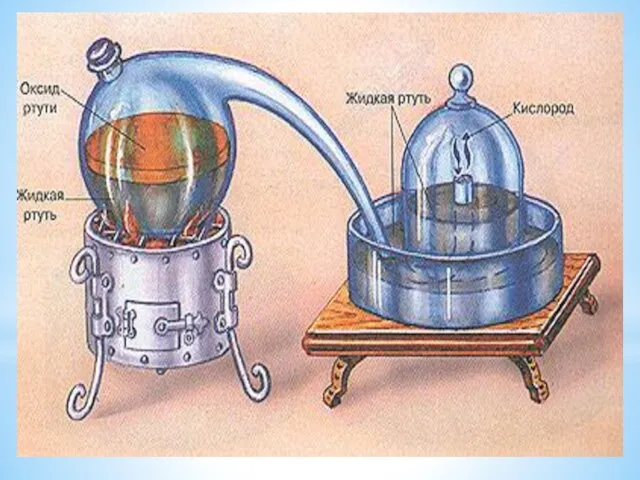
- 18. Джозеф Пристли (английский ученый) в 1774 году разложением оксида ртути (II) открыл кислород и изучил его
- 19. Карл Вильгельм Шееле (шведский химик) в 1772 году получил и детально исследовал «огненный воздух», в котором
- 20. Антуан Лавуазье в 1775 году провел эксперимент и доказал, что воздух состоит на 1/5 часть из
- 21. Тестирование
- 22. Подведение итогов урока
- 23. Цель урока: доказать, что кислород вездесущ, всемогущ и невидим.
- 25. Скачать презентацию


















 Предельные углеводороды. Алканы, насыщенные углеводороды, парафины, циклоалканы
Предельные углеводороды. Алканы, насыщенные углеводороды, парафины, циклоалканы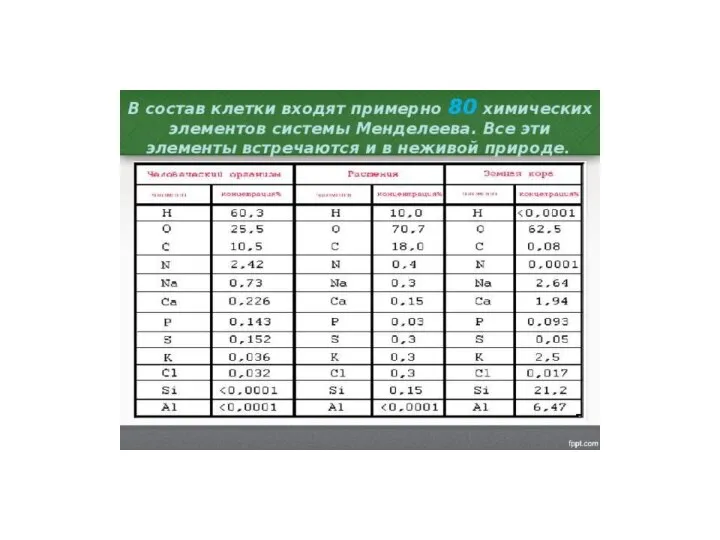 Состав клетки
Состав клетки Необратимый (совместный) гидролиз
Необратимый (совместный) гидролиз Аммиак NH3
Аммиак NH3 Химические свойства металлов
Химические свойства металлов Презентация на тему Процессы в растворах электролитическая диссоциация
Презентация на тему Процессы в растворах электролитическая диссоциация  9. Потомки светоносного элемента
9. Потомки светоносного элемента ЗАДАЧИ 9 класс
ЗАДАЧИ 9 класс Современные оборудования в лаборатории
Современные оборудования в лаборатории Химическое расследование. Химические свойства галогенов
Химическое расследование. Химические свойства галогенов Изомерия
Изомерия Элемент протактиний
Элемент протактиний Химические свойства металлов. Электрохимический ряд напряжения металлов
Химические свойства металлов. Электрохимический ряд напряжения металлов Добыча золота в России По теме «Внешние эффекты и права собственности»
Добыча золота в России По теме «Внешние эффекты и права собственности» AB-Polymerchemie Referenze
AB-Polymerchemie Referenze Порядок констант ССВ JHH в бензоле. Задачи
Порядок констант ССВ JHH в бензоле. Задачи Условия, замедляющие выход водорастворимых питательных веществ из удобрений на примере аммофоса
Условия, замедляющие выход водорастворимых питательных веществ из удобрений на примере аммофоса Азотная кислота
Азотная кислота Chimie bioorganique
Chimie bioorganique Бензол. Cвойства, реакции, применение
Бензол. Cвойства, реакции, применение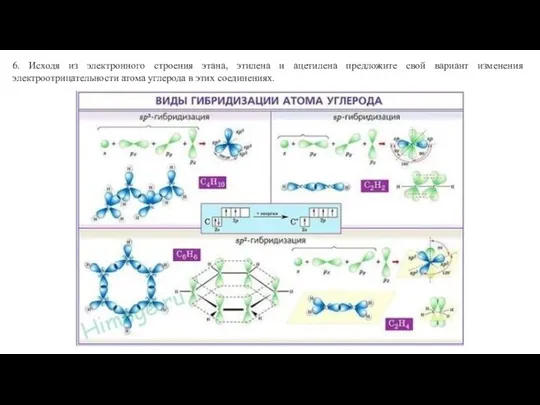 Виды гибридизации атома углерода
Виды гибридизации атома углерода Склероглюкан
Склероглюкан Презентация на тему Алюминий
Презентация на тему Алюминий  Практическая работа №1. Определение содержания нитратов в овощах и фруктах
Практическая работа №1. Определение содержания нитратов в овощах и фруктах Закон Авогадро
Закон Авогадро Презентация на тему Органическая химия. История развития
Презентация на тему Органическая химия. История развития  Влияние на скорость ферментативной реакции
Влияние на скорость ферментативной реакции Презентация на тему Атомы и молекулы
Презентация на тему Атомы и молекулы