Содержание
- 2. Общая формула гомологического ряда предельных углеводородов CnH2n+2 Названия всех предельных углеводородов заканчиваются на –ан Радикалы называются
- 3. Следующий представитель С3Н8 – пропан. Структурная формула Н3С-СН2-СН3. У пропана возможно образование уже двух изомерных радикалов,
- 4. Далее все по такому же принципу. Четвертый представитель, еще плюс -СН2 – бутан С4Н10. Если у
- 5. Изобутан тоже может дать 2 радикала. При отнятии атома водорода от бокового атома углерода получаем изобутил
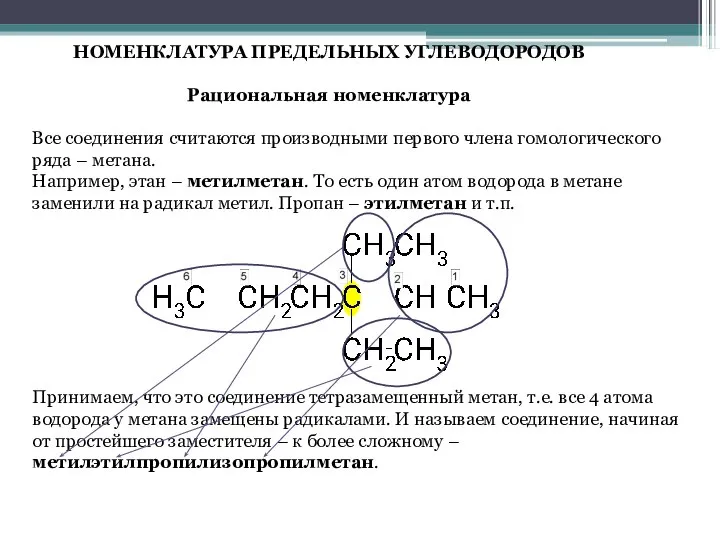
- 6. НОМЕНКЛАТУРА ПРЕДЕЛЬНЫХ УГЛЕВОДОРОДОВ Рациональная номенклатура Все соединения считаются производными первого члена гомологического ряда – метана. Например,
- 7. Систематическая номенклатура Выбирают наиболее длинную цепочку углеродных атомов, так называемую главную цепь. При этом у главной
- 8. МЕТОДЫ ПОЛУЧЕНИЯ ПРЕДЕЛЬНЫХ УГЛЕВОДОРОДОВ ЛАБОРАТОРНЫЕ Реакция Дюма CH3COONa (тв.) + NaOH(тв.) → CH4 + Na2CO3 2.
- 9. 5. Восстановление галогеналканов [H] R-Hal → R-H + H-Hal В качестве восстановителей применяются LiAlH4, NaBH4 Алкилиодиды
- 10. ПРОМЫШЛЕННЫЕ Метод Бергиуса Fe, 500°, 200 атм yC + xH2 −−−−−−−→ СnH2n+2 2. Метод Фишера-Тропша Fe+Ni,
- 11. Галогенирование hν СH4 + Cl2 → СH3-Cl + HCl хлорметан (метилхлорид) СH3Cl + Cl2 → СH2Cl2
- 12. 2. Реакция Коновалова СnH2n+2 + HNО3 → СnH2n+1-NO2 + H2O Условия реакции: 13%-ная азотная кислота, 100-120°С.
- 13. 4. Окисление (горение) СnH2n+2 + О2 → nCO2 + H2O + Q соли Mn, 180° C30H62-C40H82
- 15. Скачать презентацию






![5. Восстановление галогеналканов [H] R-Hal → R-H + H-Hal В качестве восстановителей](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1085144/slide-8.jpg)




 Электролиз. Правила электролиза
Электролиз. Правила электролиза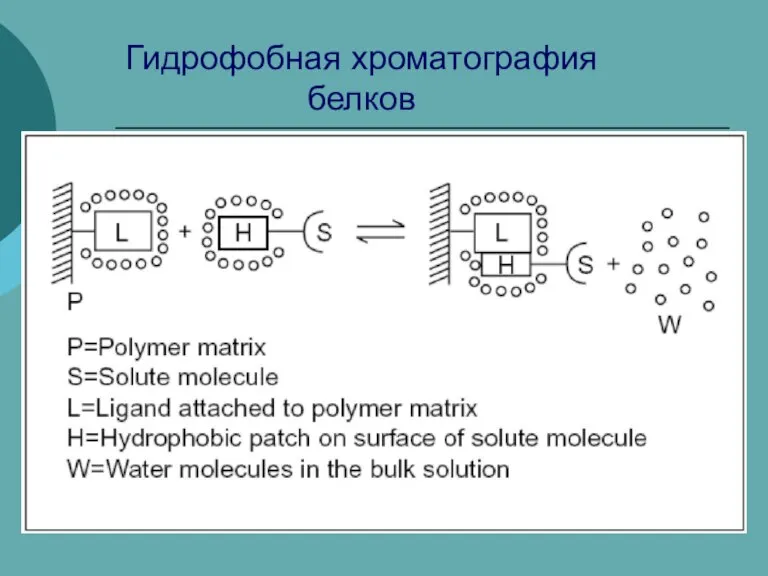 Гидрофобная хроматография белков
Гидрофобная хроматография белков 7609f31d31514fe19b6df19a98197139 (1)
7609f31d31514fe19b6df19a98197139 (1) Бикомпонентные покрытия
Бикомпонентные покрытия Сера и ее соединения
Сера и ее соединения Презентация на тему Строение атома Химическая связь
Презентация на тему Строение атома Химическая связь  Взаимодействие плазмы с поверхностью. Проблемы термоядерного реактора
Взаимодействие плазмы с поверхностью. Проблемы термоядерного реактора Определение времени прохождения диффузии
Определение времени прохождения диффузии Презентация на тему Сплавы металлов
Презентация на тему Сплавы металлов  Химия. Спирты
Химия. Спирты Углерод и его аллотропные модификации. Органическая химия - химия углерода
Углерод и его аллотропные модификации. Органическая химия - химия углерода Газообразные (газ)
Газообразные (газ) Химические свойства алкенов. Получение
Химические свойства алкенов. Получение Хлорорганические соединения
Хлорорганические соединения Химические элементы
Химические элементы Соли: получение
Соли: получение Азотная кислота
Азотная кислота Белки-1 2020
Белки-1 2020 Основания (Ме+n(ОН)-n)
Основания (Ме+n(ОН)-n) Расчётно-графическая работа по теме Мыловарение
Расчётно-графическая работа по теме Мыловарение Альдегиды. Получение и применение
Альдегиды. Получение и применение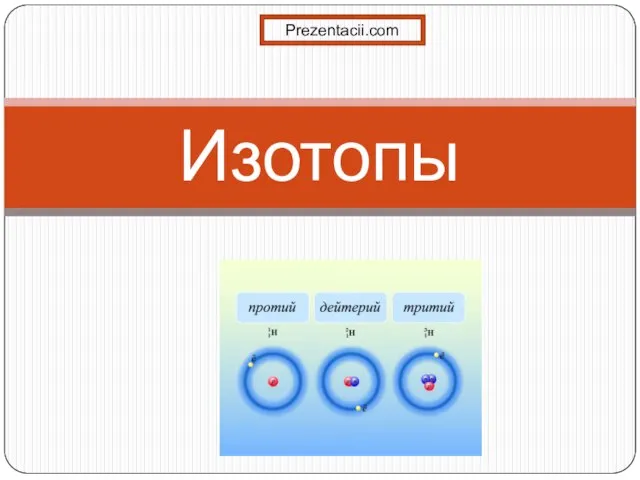 Презентация на тему Изотопы
Презентация на тему Изотопы  Типы химических реакций
Типы химических реакций Растительные жиры. Пальмовое масло
Растительные жиры. Пальмовое масло Химия в быту
Химия в быту Кристаллическое строение металлов и сплавов. Аморфные и кристаллические тела
Кристаллическое строение металлов и сплавов. Аморфные и кристаллические тела Алкены. Ҳимические свойства алкенов
Алкены. Ҳимические свойства алкенов Порядок в жидкостях
Порядок в жидкостях