Содержание
- 2. Содержание Классификация Строение Номенклатура Изомерия Физические свойства Гомологический ряд
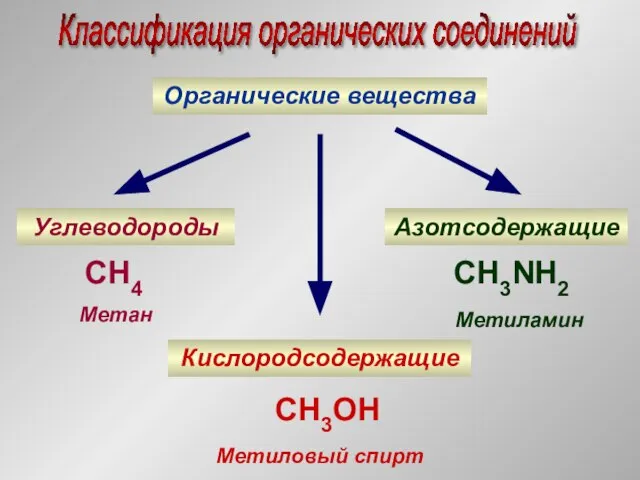
- 3. Классификация органических соединений Органические вещества Углеводороды Кислородсодержащие Азотсодержащие CH4 Метан CH3NH2 Метиламин CH3OH Метиловый спирт
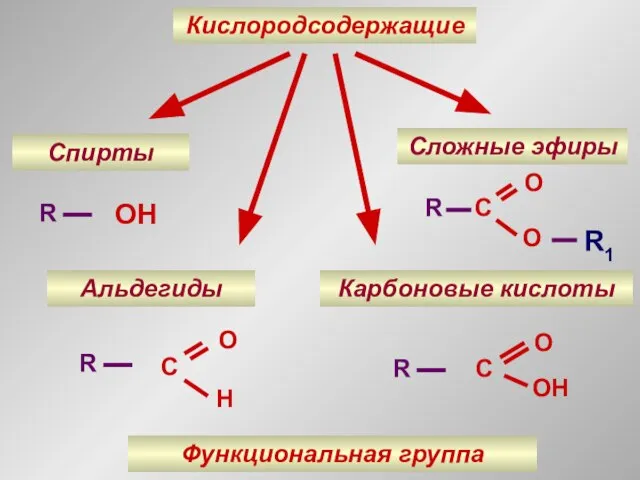
- 4. Кислородсодержащие Спирты Альдегиды Карбоновые кислоты Сложные эфиры OH Функциональная группа
- 5. Классификация спиртов. I. По количеству гидроксильных групп Одноатомные C2H5 OH Двухатомные H2С — OH | H2
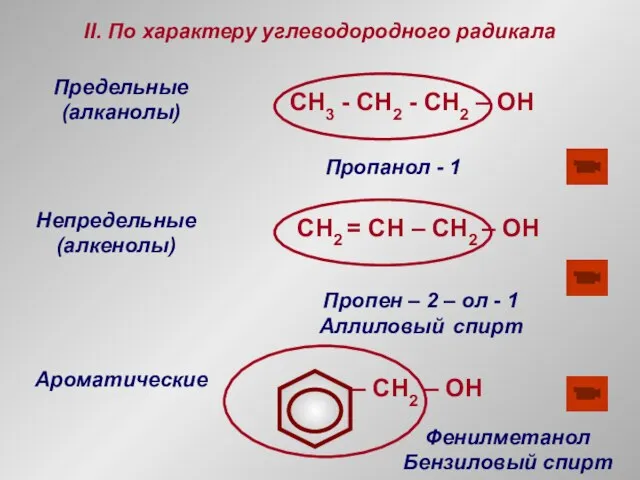
- 6. II. По характеру углеводородного радикала Предельные (алканолы) CH3 - СH2 - CH2 – OH Непредельные (алкенолы)
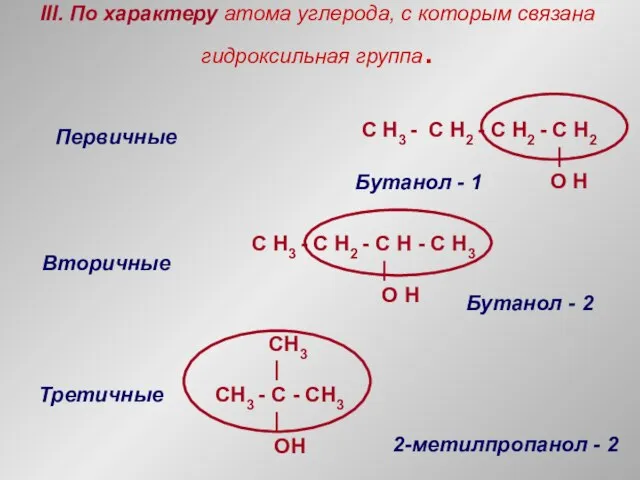
- 7. III. По характеру атома углерода, с которым связана гидроксильная группа. Первичные Вторичные Третичные C H3 -
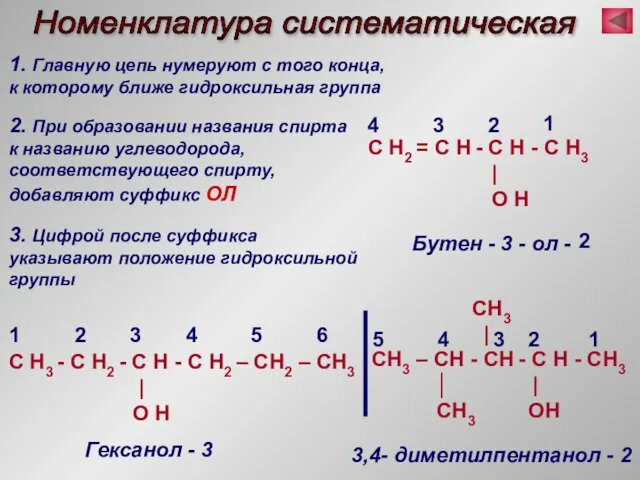
- 8. Номенклатура систематическая 1. Главную цепь нумеруют с того конца, к которому ближе гидроксильная группа C H2
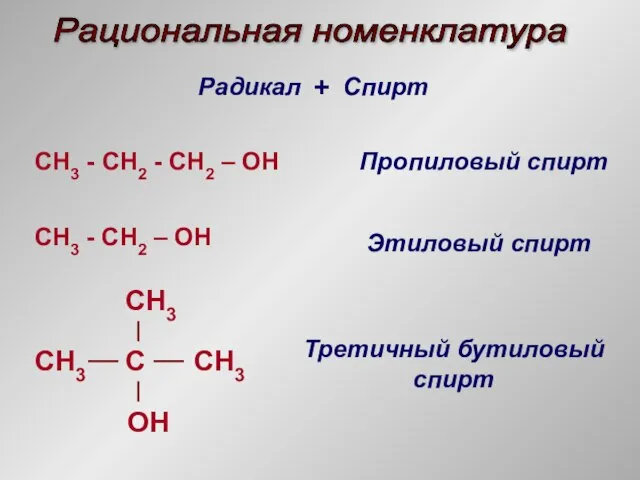
- 9. Рациональная номенклатура Радикал + Спирт CH3 - СH2 - CH2 – OH Пропиловый спирт CH3 -
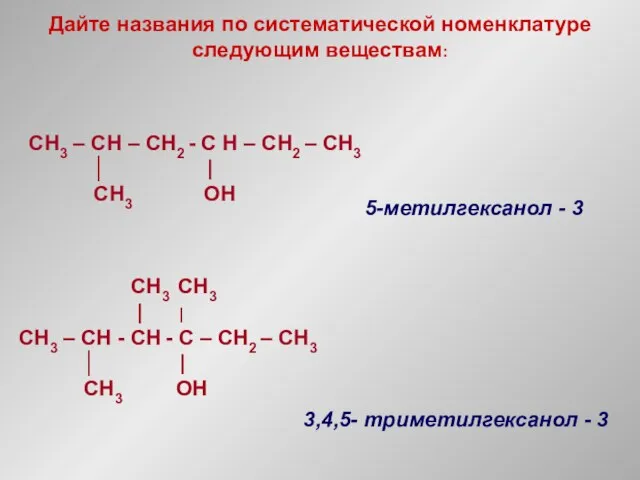
- 10. Дайте названия по систематической номенклатуре следующим веществам: CH3 – CH – CH2 - С H –
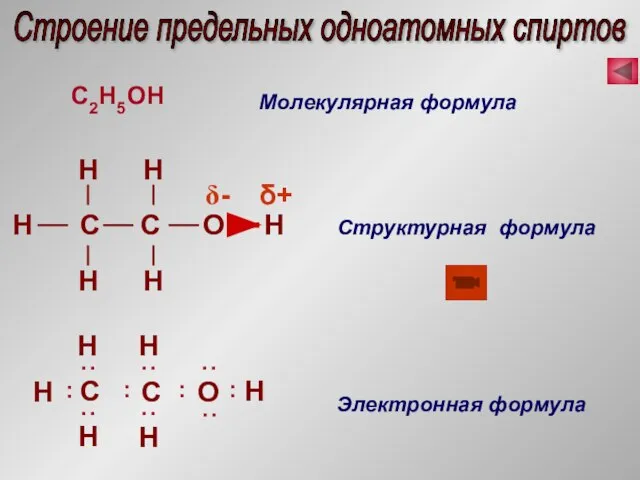
- 11. Строение предельных одноатомных спиртов Молекулярная формула Структурная формула Электронная формула δ+ δ-
- 12. Гомологический ряд CnH2n+1 OH Общая формула R OH CH3OH Метиловый спирт, метанол C2H5OH Этиловый спирт, этанол
- 13. Физические свойства и выше Как объяснить, что гомологический ряд предельных одноатомных спиртов начинается не газообразным углеводородом?
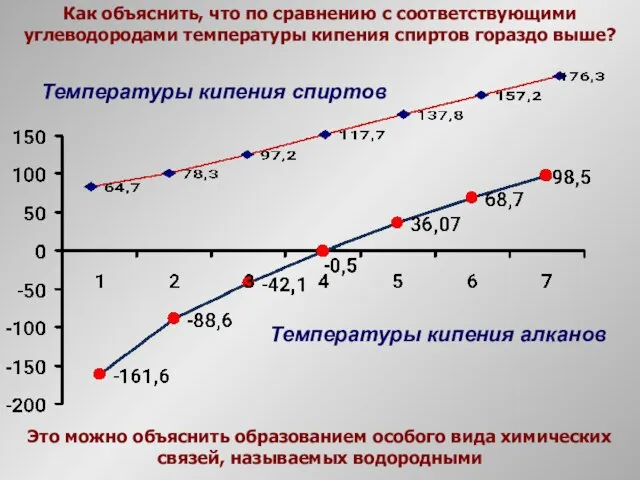
- 14. Как объяснить, что по сравнению с соответствующими углеводородами температуры кипения спиртов гораздо выше? Температуры кипения алканов
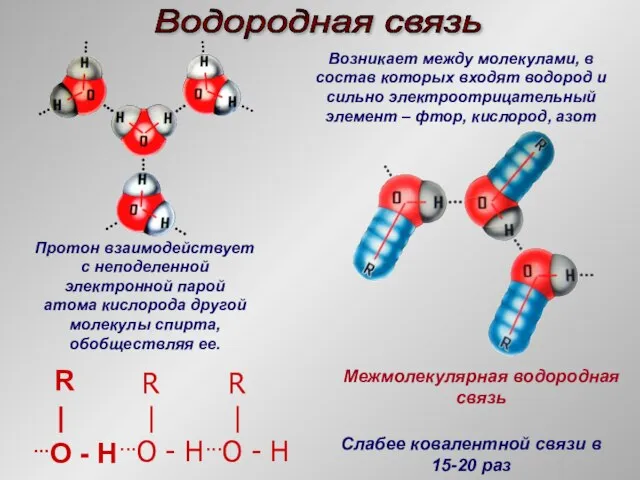
- 15. Водородная связь R | ...O - H R | ...O - H R | ...O -
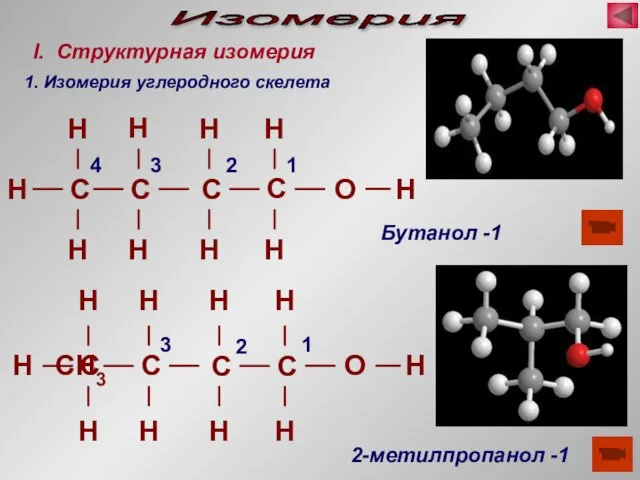
- 16. Изомерия H СH3 Бутанол -1 2-метилпропанол -1 I. Структурная изомерия 1. Изомерия углеродного скелета 1 2
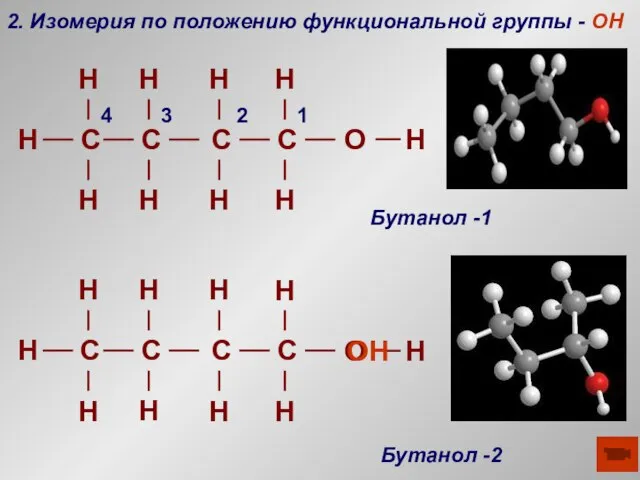
- 17. 2. Изомерия по положению функциональной группы - OH Бутанол -1 1 2 3 4 H OH
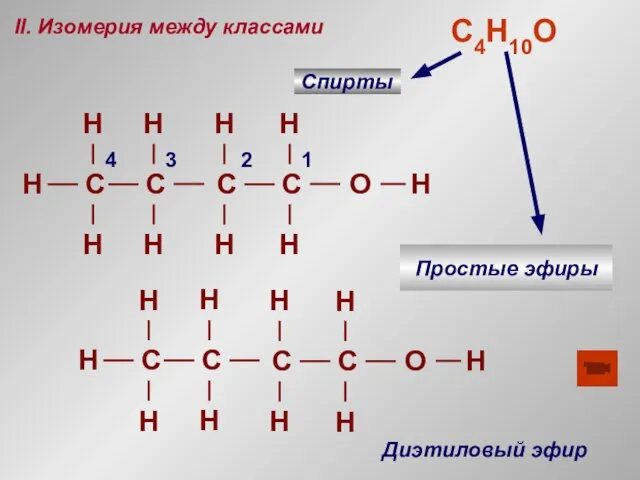
- 18. II. Изомерия между классами H Спирты 1 2 3 4 Диэтиловый эфир С4H10O Простые эфиры
- 20. Скачать презентацию




 Электролиз (катод)
Электролиз (катод) Минералы алюминия
Минералы алюминия Электролиз. Применение электролиза
Электролиз. Применение электролиза Химический состав живых организмов. Метаболизм
Химический состав живых организмов. Метаболизм Сера
Сера Алюминий. Из истории открытия
Алюминий. Из истории открытия Химическое сопротивление материалов
Химическое сопротивление материалов Селективная экстракция отдельных групп БАВ сверхкритическими флюидами
Селективная экстракция отдельных групп БАВ сверхкритическими флюидами Использование комбинаторных задач для подсчета вероятностей
Использование комбинаторных задач для подсчета вероятностей Химический опыт с горением борноэтилового эфира
Химический опыт с горением борноэтилового эфира Насыщенные жирные кислоты
Насыщенные жирные кислоты Презентация на тему Пластмасса
Презентация на тему Пластмасса  Химия в косметологии
Химия в косметологии Получение карбоновых кислот
Получение карбоновых кислот Азот. Аммиак. Соли аммония (1)
Азот. Аммиак. Соли аммония (1) Химия цвета
Химия цвета Валентность. Что же это такое?
Валентность. Что же это такое? ЛК 2_окислительно-восстановительные процессы
ЛК 2_окислительно-восстановительные процессы Пример выполнения проверочной работы по теме углеводороды
Пример выполнения проверочной работы по теме углеводороды Установка ЛЧ-35-11/600. Блок Гидроочистки
Установка ЛЧ-35-11/600. Блок Гидроочистки Свойства кислорода. Оксиды
Свойства кислорода. Оксиды Презентация на тему Химия в повседневной жизни человека
Презентация на тему Химия в повседневной жизни человека  Тотығу - тотықсыздану реакциясы
Тотығу - тотықсыздану реакциясы Углеводы: моно-, ди-, полисахариды
Углеводы: моно-, ди-, полисахариды Презентация на тему Природные источники углеводородов (9 класс)
Презентация на тему Природные источники углеводородов (9 класс)  Презентация на тему Угольная и кремниевая кислоты и их соли
Презентация на тему Угольная и кремниевая кислоты и их соли  Презентация на тему М.В. Ломоносов
Презентация на тему М.В. Ломоносов  Кристаллическая структура вещества. Характеристика вещества по формуле
Кристаллическая структура вещества. Характеристика вещества по формуле