Слайд 2 «Просто знать – еще не все,
знания нужно уметь использовать»

И.В.Гете
Слайд 3Ион аммония образован только неметаллами.
Так же, как и ионы металлов, он образует

свои соли.
Все соли аммония растворимы в воде.
Качественная реакция на ион аммония- действие щелочи при нагревании.
В состав пекарского порошка входит гидрокарбонат аммония, поэтому его используют в хлебопечении.
Нашатырь используют при паянии.
Агроному-почвоведу, а также любому дачнику необходимы знания по химии.
Без азота нет белка, без белка нет жизни.
Слайд 4 Цели урока
сформировать знания о характерных свойствах солей аммония,
ознакомить с представителями

этих солей и их применением,
развивать умения выделять главное, классифицировать, представлять результаты работы.
Слайд 5Соли аммо́ния — соли, содержащие одновалентный
ион аммония NH4+; по строению, цвету

и другим
свойствам они похожи на соответствующие соли калия.
Все соли аммония растворимы в воде, полностью диссоциируют в водном растворе.
Слайд 6 Химические свойства
1. Сильные электролиты (диссоциируют в водных растворах):

NH4Cl ↔ NH4 ++ Cl-
2. С кислотами (реакция обмена):
(NH4) 2CO3 + 2НCl → 2NH 4Cl + Н2O + CO2 ↑
2NH4+ + CO32- + 2H+ + 2Cl- → 2NH4+ + 2Cl- + Н2O + CO2 ↑
CO32- + 2H+ → Н2O + CO2 ↑
Слайд 7 Химические свойства
3. C солями (реакция обмена):
(NH4)2SO4 + Ba(NO3)2

→ BaSO4 ↓ + 2NH4NO3
2NH4+ + SO42- + Ba2+ + 2NO3- → BaSO4 ↓ + 2NH4+ + 2NO3-
Ba2+ + SO42- → BaSO4 ↓
4. При нагревании со щелочами выделяется аммиак (качественная реакция на ион аммония):
NH4Cl + NaOH → NaCl + NH3 ↑ + Н2O
Слайд 8Применение солей аммония
в пиротехнике;
в хлебопечении и кондитерской промышленности;
в сельском хозяйстве- удобрения;
при

паянии металлов (нашатырь- хлорид аммония);
электролит в сухих элементах (хлорид аммония).
Слайд 9применение солей аммония
Нитрат аммония NH4NО3 в смеси с порошками алюминия и угля

используют в качестве взрывчатого вещества - аммонала , который широко применяют при разработке горных пород.
Слайд 10применение солей аммония
Гидрокарбонат аммония NH4HCO3 и карбонат аммония (NH4)2CO3 применяют в кондитерском

деле, так как они легко разлагаются при нагревании и образуют газы, разрыхляющие тесто и делающие его пышным, например:
NH4HCO3 = NH3↑ + Н2O↑ + CO2↑
Слайд 11применение солей аммония
Соли аммония
используются
в качестве удобрений

Слайд 12применение солей аммония
Хлорид аммония NH4Cl используют при паянии, так как он очищает

поверхность металла от оксидной плёнки и к ней хорошо пристаёт припой.
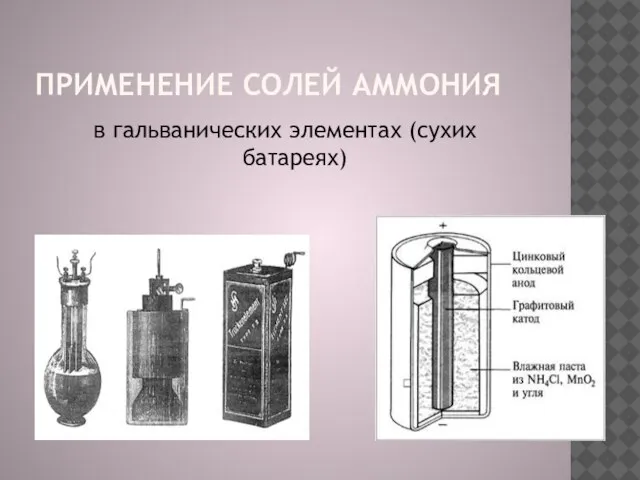
Слайд 13применение солей аммония
в гальванических элементах (сухих батареях)
Слайд 14применение солей аммония
Хлорид аммония применяется при изготовлении дымовых шашек

Слайд 15
получение солей аммония
Аммиак (или гидроксид аммония) + кислота.
NH3 + HNO3 =

NH4NO3
2NH4OH + H2SO4 =(NH4) 2SO4+ 2Н2O
Слайд 16Задания на развитие творческого мышления.
Предложите способ очистки поваренной соли от содержащейся в

ней примеси хлорида аммония.
Объясните, можно ли смешивать аммиачную селитру (нитрат аммония) с известью?
Слайд 17Заключение
Роль азотистых соединений в жизни человека и общества очень велика, а применении

разнообразно. Азот – основа жизни на Земле. На Земле постоянно происходят процессы превращения веществ живой и неживой природы. В результате этих превращений неорганические вещества неживой природы – соли аммония могут превращаться в сложные органические вещества – белки. А белки – это основа всего живого В белках содержится 18 % азота. Без азота нет белка, без белка нет жизни!
















 Ароматические углеводороды. Строение молекулы бензола. Физические свойства
Ароматические углеводороды. Строение молекулы бензола. Физические свойства Молекулярно-массовое распределение
Молекулярно-массовое распределение Изомерия. Виды изомерии
Изомерия. Виды изомерии Презентация на тему Ионные уравнения
Презентация на тему Ионные уравнения  Основания, состав и классификация
Основания, состав и классификация Типы кристаллических решеток. Тест
Типы кристаллических решеток. Тест СПИРТЫ, ФЕНОЛЫ
СПИРТЫ, ФЕНОЛЫ Химические методы анализа. Аналитические методы контроля в техносферной безопасности. Лекция 6
Химические методы анализа. Аналитические методы контроля в техносферной безопасности. Лекция 6 Теория электролитической диссоциации
Теория электролитической диссоциации Реакции ионного обмена составление ионных уравнений
Реакции ионного обмена составление ионных уравнений 01. Химический состав
01. Химический состав Алканы. Задания
Алканы. Задания Спирты. Непредельные спирты
Спирты. Непредельные спирты История развития химии
История развития химии Периодическая система химических элементов Д.И. Менделеева. Знаки химических элементов
Периодическая система химических элементов Д.И. Менделеева. Знаки химических элементов Цинк (Zn). Свойства
Цинк (Zn). Свойства Предельные одноатомные спирты
Предельные одноатомные спирты Физическая химия растворов электролитов
Физическая химия растворов электролитов Основания. 8 класс
Основания. 8 класс Kristālisku vielu uzbūve
Kristālisku vielu uzbūve Соединения серы
Соединения серы Строение атома. Химия, 8 класс
Строение атома. Химия, 8 класс Органическая химия. Йенс Якоб Берцелиус (1779 - 1848)
Органическая химия. Йенс Якоб Берцелиус (1779 - 1848) Типы химических реакций. Класс оксиды
Типы химических реакций. Класс оксиды Формы существования химических элементов. Формы существования химических элементов
Формы существования химических элементов. Формы существования химических элементов lektsia_7
lektsia_7 Предмет органической химии
Предмет органической химии Хром. Месторождения
Хром. Месторождения