Содержание
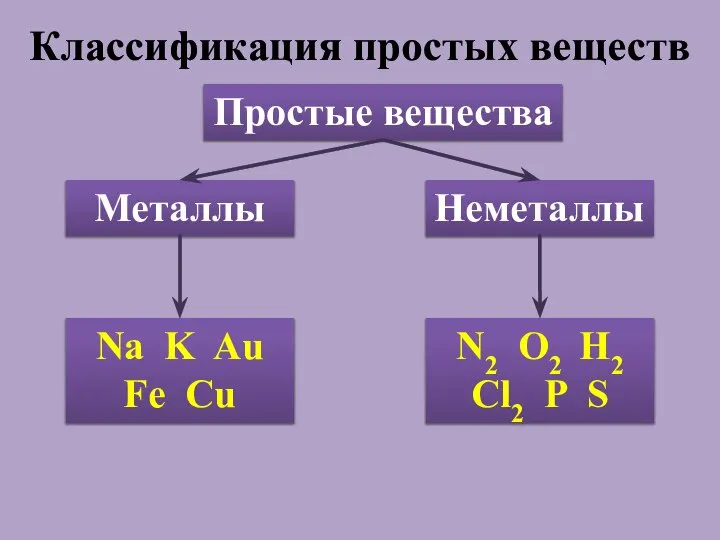
- 2. Классификация простых веществ Простые вещества Металлы Неметаллы Na K Au Fe Cu N2 O2 H2 Cl2
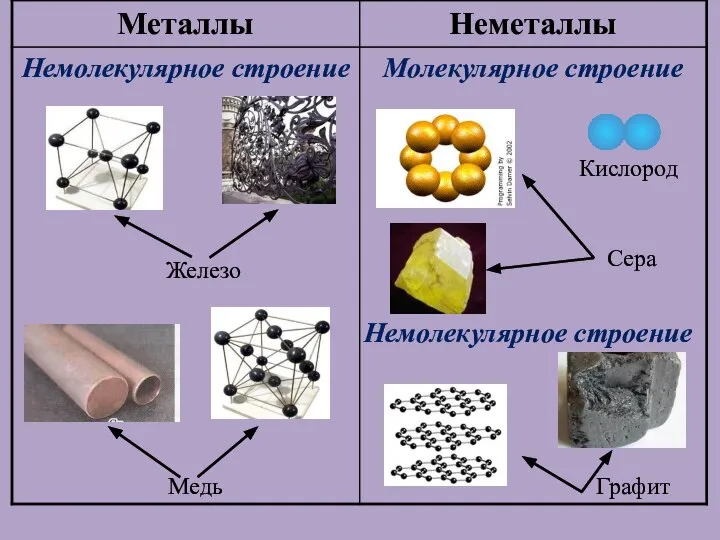
- 3. Немолекулярное строение Графит Кислород Сера Медь Железо
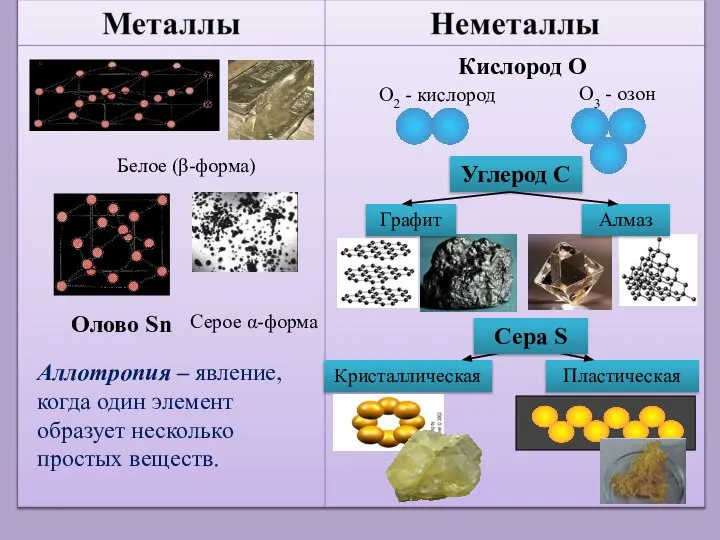
- 4. Кислород О Углерод С Кристаллическая Пластическая Олово Sn Серое α-форма Белое (β-форма) Сера S
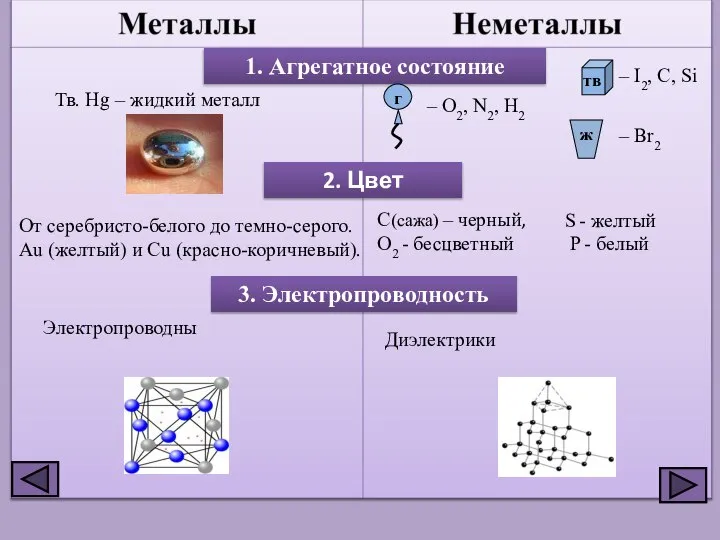
- 5. 1. Агрегатное состояние Тв. Hg – жидкий металл – O2, N2, H2 – I2, C, Si
- 6. От серебристо-белого до серого бериллий германий литий золото графит мышьяк алмаз кремний сера фосфор медь
- 7. 4. Твердость / мягкость Пластичные (Au, Ag, Cu, Al и др.), кроме. Sn (серое). Хрупкие (S,
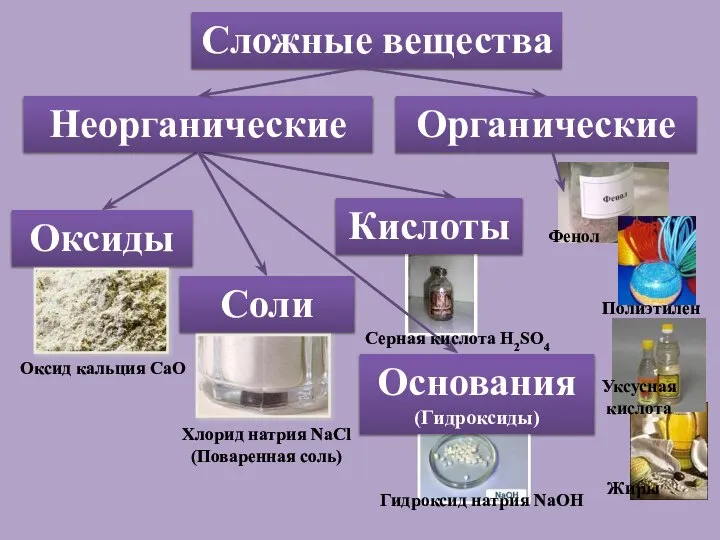
- 8. Сложные вещества Оксиды Соли Оксид кальция СаО Хлорид натрия NaCl (Поваренная соль) Кислоты Гидроксид натрия NaОН
- 9. Сложные вещества состоят из атомов разных химических элементов В химических реакциях могут разлагаться с образованием нескольких
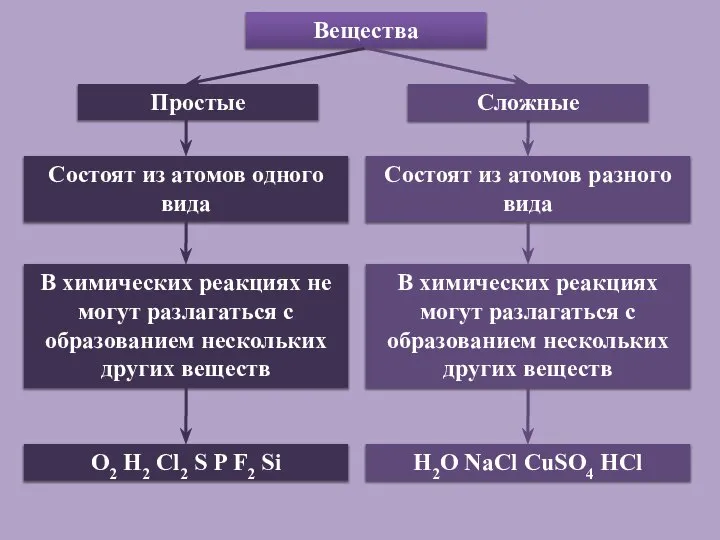
- 10. Вещества Простые Состоят из атомов одного вида Состоят из атомов разного вида В химических реакциях не
- 12. Аллотро́пия (от др.-греч. αλλος — «другой», τροπος — «поворот, свойство») — существование одного и того же
- 13. Просты́е вещества́ — вещества, состоящие исключительно из атомов одного химического элемента (в отличие от сложных веществ).
- 14. Сложные вещества — это химические вещества, которые состоят из атомов двух или более химических элементов. Сложными
- 15. Смесь — Продукт смешения, механического соединения каких-либо веществ. Например: горючая смесь, гелиево-кислородная смесь. Молоко Воздух
- 17. Скачать презентацию








 Получение металлов в промышленности. Чёрная металлургия
Получение металлов в промышленности. Чёрная металлургия Изучение ТЭД и ОВР в школьном курсе химии
Изучение ТЭД и ОВР в школьном курсе химии Исследование n-метилольных производных аллантоина методом тонкослойной хроматографии
Исследование n-метилольных производных аллантоина методом тонкослойной хроматографии Этиленовые углеводороды (алкены, олефины)
Этиленовые углеводороды (алкены, олефины) Презентация на тему Витамин C
Презентация на тему Витамин C  История создания термометра: как придумали первый градусник?
История создания термометра: как придумали первый градусник? Бирюза. Характеристики минерала
Бирюза. Характеристики минерала Responsible Aluminium Framework
Responsible Aluminium Framework Презентация на тему М.В. Ломоносов
Презентация на тему М.В. Ломоносов 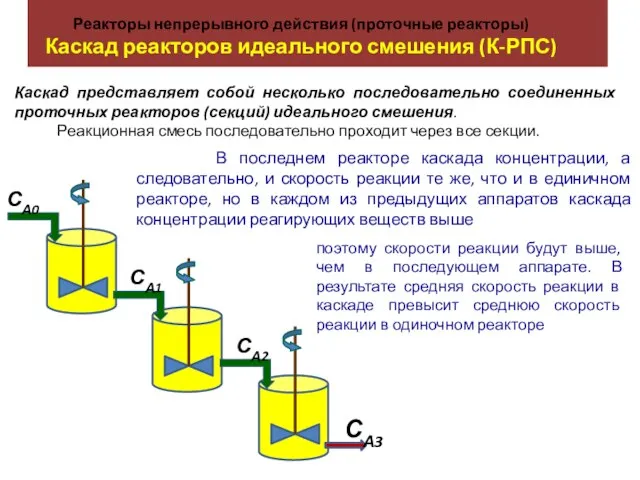 Реакторы непрерывного действия (проточные реакторы). Каскад реакторов идеального смешения (К-РПС)
Реакторы непрерывного действия (проточные реакторы). Каскад реакторов идеального смешения (К-РПС) Основные понятия химии
Основные понятия химии Тесты для самопроверки
Тесты для самопроверки Химия в нашем доме. Введение в курс. Урок №1
Химия в нашем доме. Введение в курс. Урок №1 Профессии, связанне с химией
Профессии, связанне с химией Презентация на тему Полимеры
Презентация на тему Полимеры  Окисление этанола оксидом меди
Окисление этанола оксидом меди Натуральный каучук
Натуральный каучук Ð¥ÐÐÐЧÐСÐÐÐ Ð ÐÐÐÐÐÐСÐÐ1
Ð¥ÐÐÐЧÐСÐÐÐ Ð ÐÐÐÐÐÐСÐÐ1 Титан. История открытия титана
Титан. История открытия титана Названия и формулы кислот
Названия и формулы кислот Железо от начала времен до конца средних веков
Железо от начала времен до конца средних веков Металлическая, водородная, Ван-дер-ваальсова химические связи
Металлическая, водородная, Ван-дер-ваальсова химические связи Взаимодействие плазмы с поверхностью. Проблемы термоядерного реактора
Взаимодействие плазмы с поверхностью. Проблемы термоядерного реактора Клей
Клей Презентация на тему Жидкое состояние вещества
Презентация на тему Жидкое состояние вещества  Соли. Применение солей
Соли. Применение солей Строение комплексных соединений. Лекция 4
Строение комплексных соединений. Лекция 4 Презентация на тему Обратимость химических реакций. Химическое равновесие
Презентация на тему Обратимость химических реакций. Химическое равновесие