Содержание
- 2. И
- 3. Соли как производные кислот и оснований
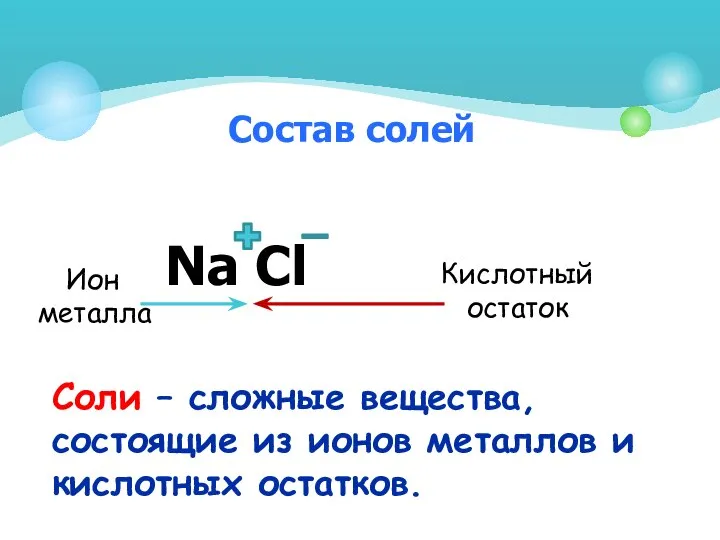
- 4. Состав солей Nа Сl Соли – сложные вещества, состоящие из ионов металлов и кислотных остатков. Ион
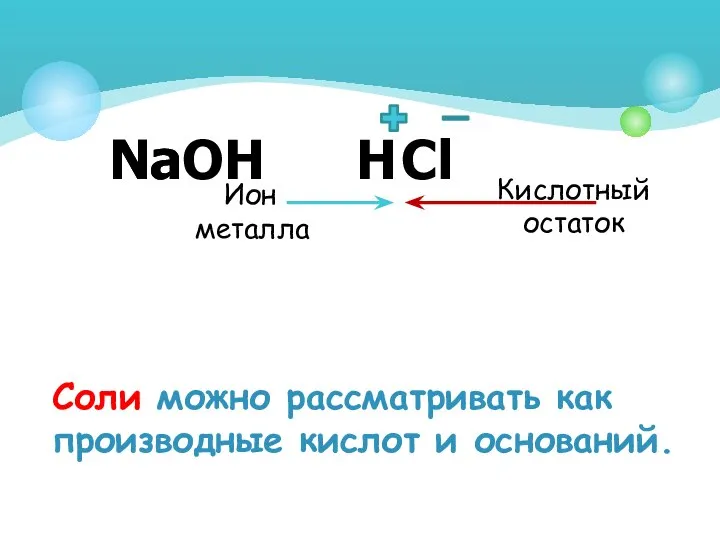
- 5. Nа ОН Н Сl Nа Соли можно рассматривать как производные кислот и оснований. Ион металла Кислотный
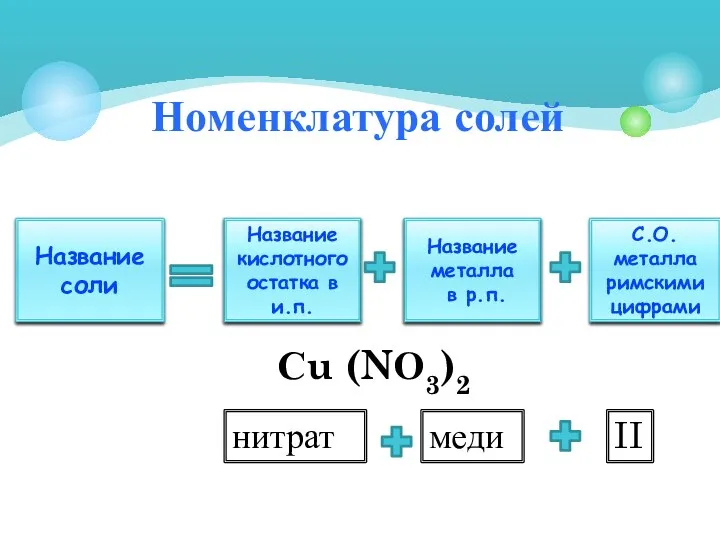
- 6. Номенклатура солей Название кислотного остатка в и.п. Название соли Название металла в р.п. С.О. металла римскими
- 7. Назовите следующие соли Li2SО4 − FеSО3 − Ва(NО3)2 − Nа2S − Zn3(РО4) 2 −
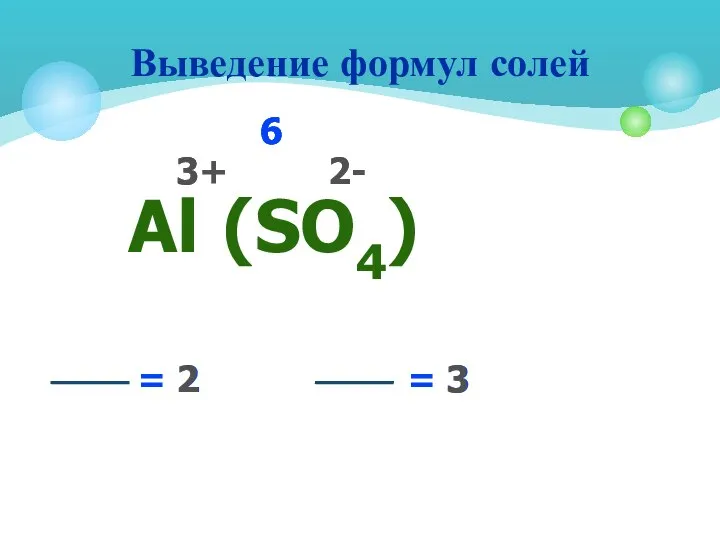
- 8. Выведение формул солей Аl (SО4) 3+ 2- 6 6 3 = 2 2 6 2 =
- 9. Карбоната натрия – Сульфата железа (III) – Хлорида цинка (II) – Иодид алюминия – Фосфат меди
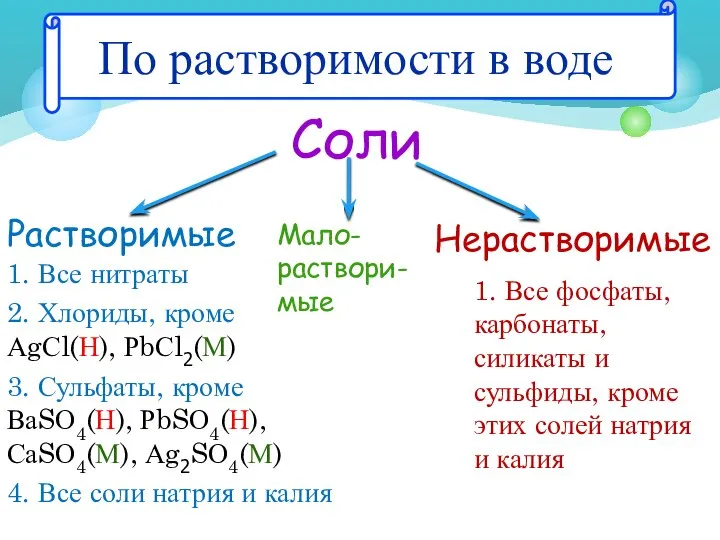
- 10. По растворимости в воде Соли Растворимые Нерастворимые 1. Все нитраты 2. Хлориды, кроме АgСl(Н), РbСl2(М) 3.
- 11. NaCl - хлорид натрия Обыкновенная поваренная соль, ежедневно принимаемая нами в пищу. Также широко используется в
- 12. CaCO3 - карбонат кальция Столь привычный каждому стоящему у доски школьнику мел, добываемый из карьеров. А
- 14. Скачать презентацию






 Рівноваги у розчинах електролітів
Рівноваги у розчинах електролітів Карбоновые кислоты
Карбоновые кислоты Структура к свойства веществ
Структура к свойства веществ Циклоалканы
Циклоалканы Получение бутандиола, как способ переработки природного газа
Получение бутандиола, как способ переработки природного газа Презентация на тему Мыло. Синтетические моющие средства
Презентация на тему Мыло. Синтетические моющие средства  Великие ученые общей и неорганической химии
Великие ученые общей и неорганической химии Алюминий и его соединения
Алюминий и его соединения Строение электронных оболочек атомов. Электроны в атоме
Строение электронных оболочек атомов. Электроны в атоме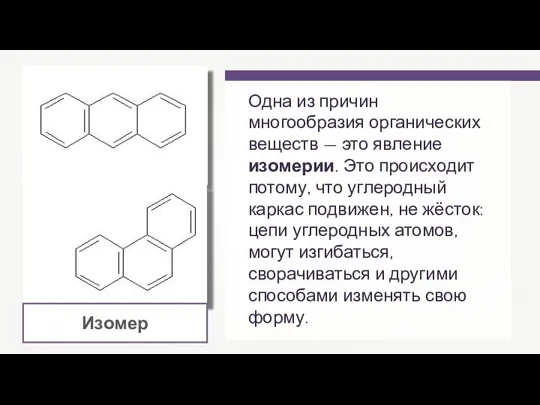 Номенклатура и изомерия алкенов
Номенклатура и изомерия алкенов Карбоновые кислоты
Карбоновые кислоты Презентация на тему Щавелевая кислота
Презентация на тему Щавелевая кислота  Строение атома. Распределение электронов
Строение атома. Распределение электронов Химическая кинетика
Химическая кинетика Парафины. Алканы
Парафины. Алканы Вирощування кристалів солей
Вирощування кристалів солей Электрокинетические явления. Электрофорез. Макро- и микроэлектрофорез. Лекция 9
Электрокинетические явления. Электрофорез. Макро- и микроэлектрофорез. Лекция 9 Простые эфиры и перекиси
Простые эфиры и перекиси Сахароза (С12Н22О11)
Сахароза (С12Н22О11) Сахар-рафинад
Сахар-рафинад Признаки химических реакций
Признаки химических реакций Химия. 8 класс. Подготовка к контрольной работе
Химия. 8 класс. Подготовка к контрольной работе «СберСтарЭнерго» «ЖИДКАЯ РЕЗИНА»
«СберСтарЭнерго» «ЖИДКАЯ РЕЗИНА» каталитические системы на основе металлоценов и метилалюмоксана в реакциях непредельных соединений с изобутиланами
каталитические системы на основе металлоценов и метилалюмоксана в реакциях непредельных соединений с изобутиланами Алкадиены. Закрепление пройденного материала
Алкадиены. Закрепление пройденного материала Плавленые сыры без фосфатов
Плавленые сыры без фосфатов Аналитические методы в современных исследованиях химии
Аналитические методы в современных исследованиях химии Оксиды и основания
Оксиды и основания