Содержание
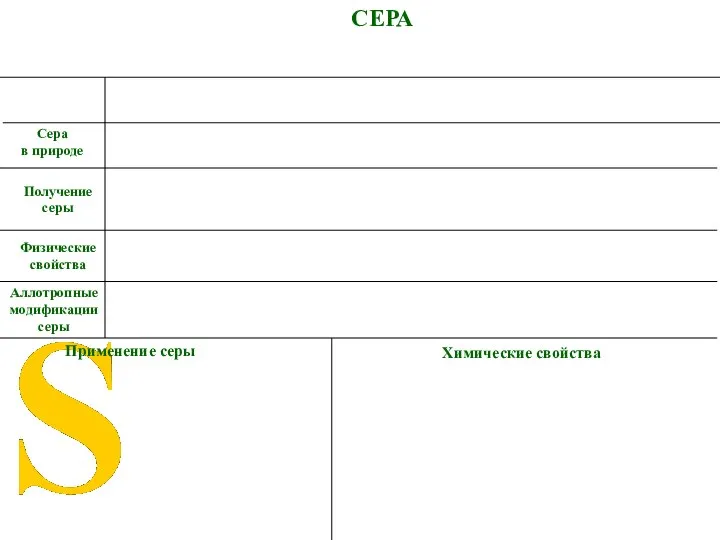
- 2. СЕРА Аллотропные модификации серы Применение серы Сера в природе Физические свойства Химические свойства Получение серы
- 3. Чтобы изучить свойства вещества необходимо знать его электронное строение Лайнус Полинг
- 4. ПЛАН ХАРАКТЕРИСТИКИ 1. Название, химический символ и относительная атомная масса элемента. 2. Атомный (порядковый) номер. 3.
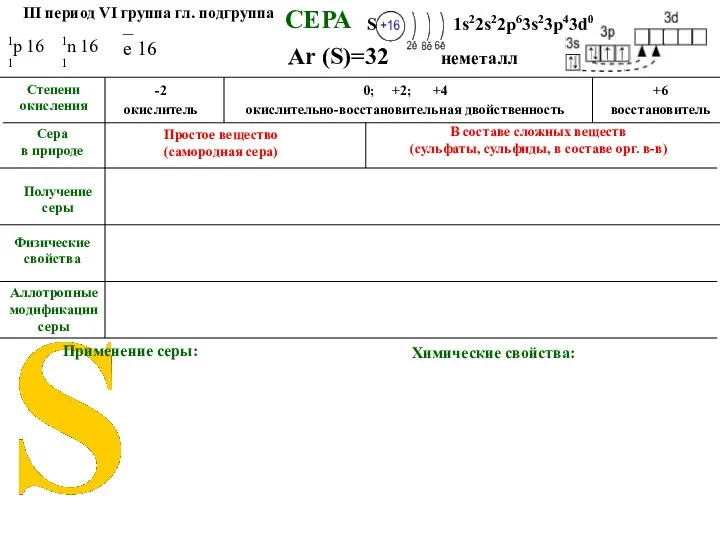
- 5. СЕРА Аллотропные модификации серы Ar (S)=32 Сера в природе Применение серы Химические свойства неметалл III период
- 6. Французский химик. Один из основоположников классической химии. Ввел в химию строгие количественные методы исследования. Доказал сложный
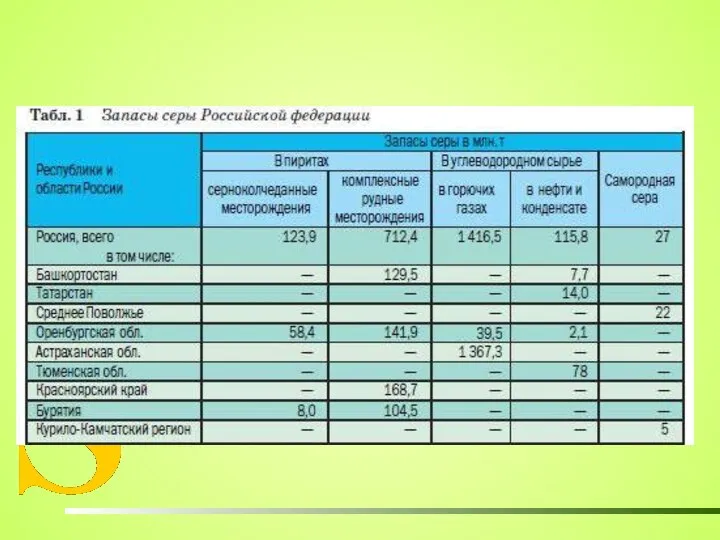
- 7. СЕРА В ПРИРОДЕ «Нет ни единой руды, нет почти ни единого камня, который бы через взаимное
- 8. ПРИРОДНЫЕ МЕСТОРОЖДЕНИЯ СЕРЫ
- 10. СЕРА Аллотропные модификации серы Ar (S)=32 Применение серы: Степени окисления Сера в природе Получение серы Простое
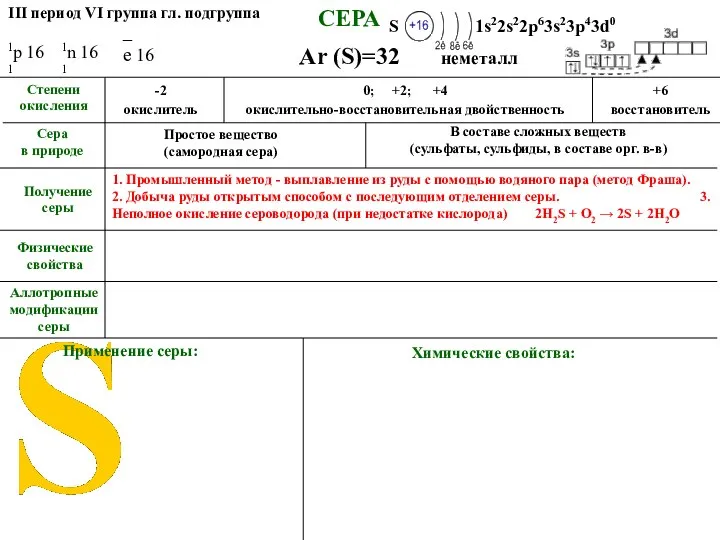
- 11. ПОЛУЧЕНИЕ СЕРЫ Метод Фраша. Выплавление серы под землёй с помощью водяного пара и выкачивание на поверхность
- 12. СЕРА Аллотропные модификации серы Ar (S)=32 Применение серы: Степени окисления Сера в природе Простое вещество (самородная
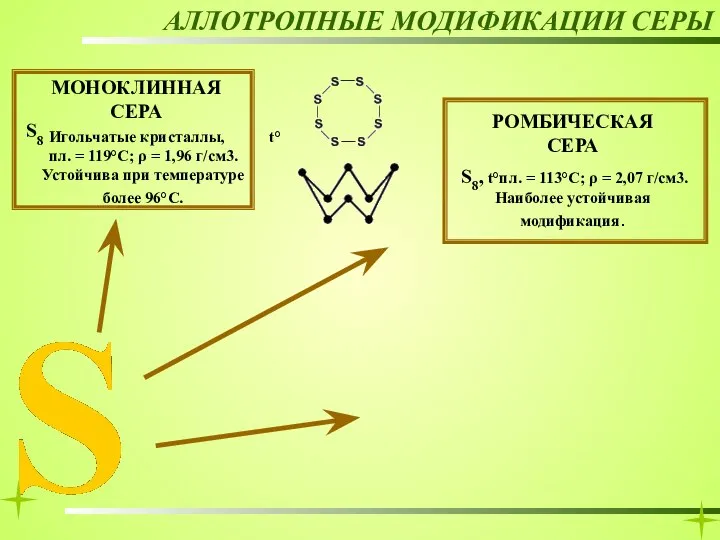
- 13. КРИСТАЛЛИЧЕСКАЯ СЕРА
- 14. СЕРА Светло-желтое хрупкое твердое вещество, имеет специфический запах, tпл = 112,8 °C, tкип = 444,674 °C,
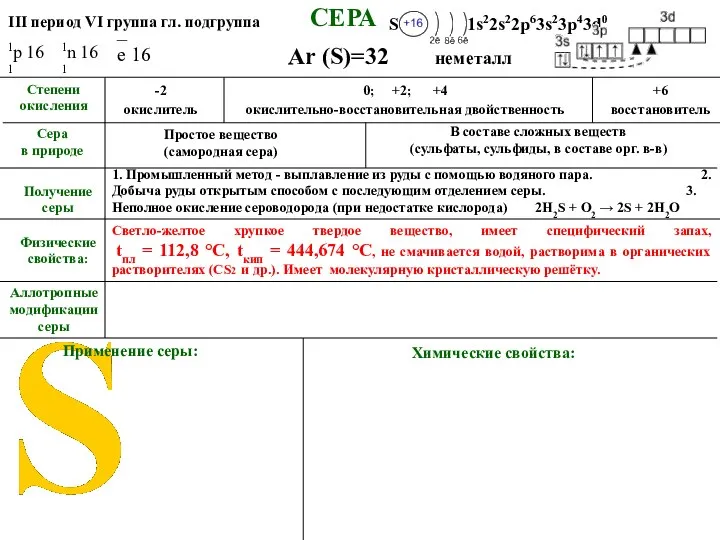
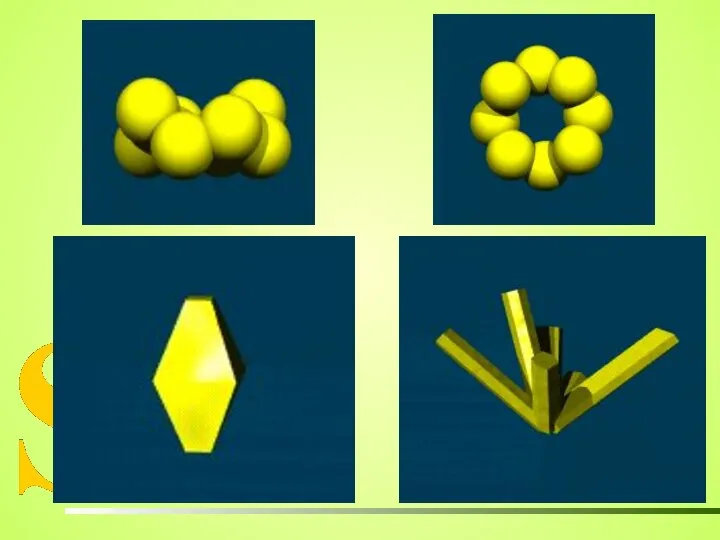
- 15. РОМБИЧЕСКАЯ СЕРА АЛЛОТРОПНЫЕ МОДИФИКАЦИИ СЕРЫ МОНОКЛИННАЯ СЕРА Игольчатые кристаллы, t°пл. = 119°C; ρ = 1,96 г/см3.
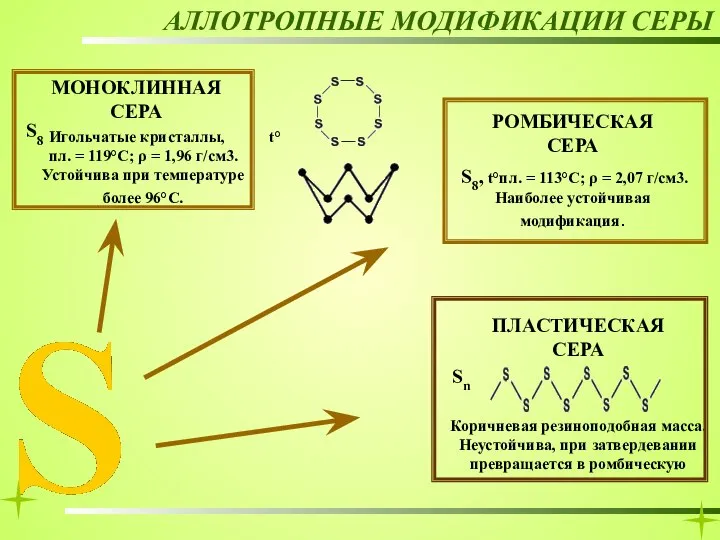
- 17. РОМБИЧЕСКАЯ СЕРА АЛЛОТРОПНЫЕ МОДИФИКАЦИИ СЕРЫ МОНОКЛИННАЯ СЕРА ПЛАСТИЧЕСКАЯ СЕРА Игольчатые кристаллы, t°пл. = 119°C; ρ =
- 18. СЕРА Светло-желтое хрупкое твердое вещество, в чистом виде без запаха, tпл = 112,8 °C, tкип =
- 19. ХИМИЧЕСКИЕ СВОЙСТВА СЕРЫ ВЗАИМОДЕЙСТВИЕ С МЕТАЛЛАМИ Hg + S = HgS (при н.у. медленно) 2Al +
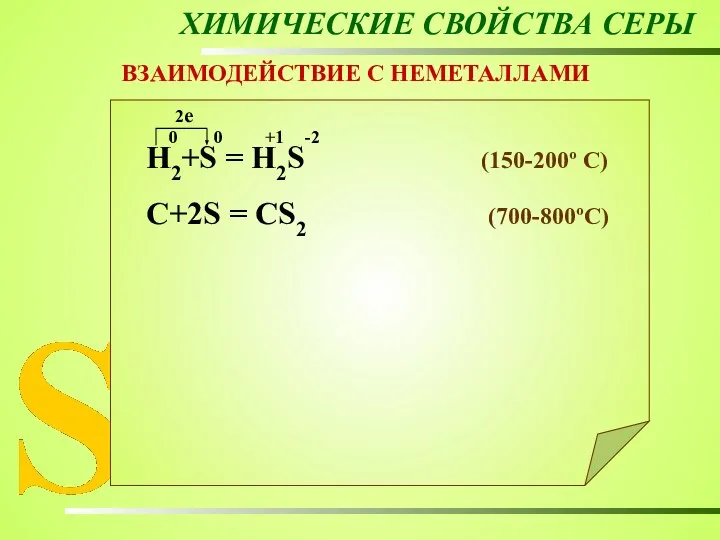
- 20. ХИМИЧЕСКИЕ СВОЙСТВА СЕРЫ ВЗАИМОДЕЙСТВИЕ С НЕМЕТАЛЛАМИ Н2+S = Н2S (150-200º C) C+2S = CS2 (700-800ºC) 0
- 21. СЕРА Светло-желтое хрупкое твердое вещество, в чистом виде без запаха, tпл = 112,8 °C, tкип =
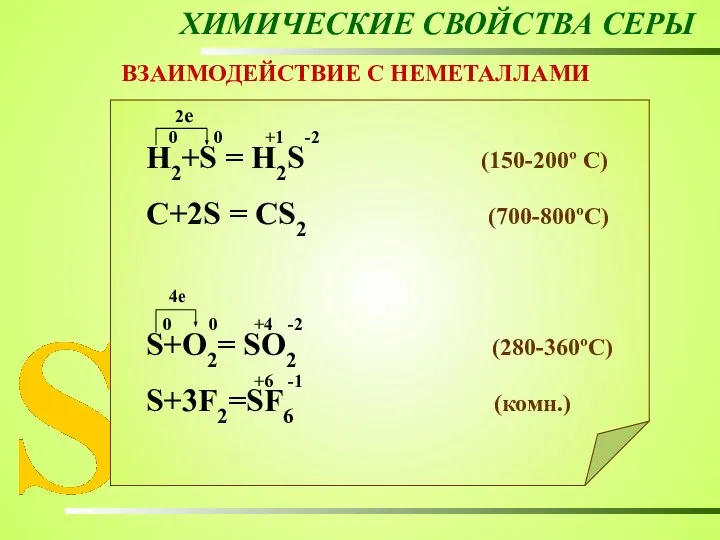
- 22. ХИМИЧЕСКИЕ СВОЙСТВА СЕРЫ ВЗАИМОДЕЙСТВИЕ С НЕМЕТАЛЛАМИ Н2+S = Н2S (150-200º C) C+2S = CS2 (700-800ºC) S+O2=
- 23. СЕРА Светло-желтое хрупкое твердое вещество, в чистом виде без запаха, tпл = 112,8 °C, tкип =
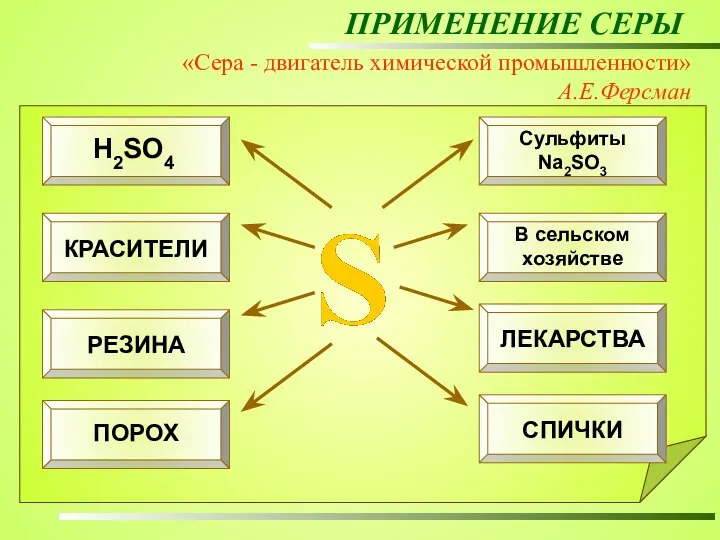
- 24. ПРИМЕНЕНИЕ СЕРЫ «Сера - двигатель химической промышленности» А.Е.Ферсман Для того чтобы изготовить автомобиль, нужно израсходовать около
- 25. БИОЛОГИЧЕСКАЯ РОЛЬ СЕРЫ Жизненно важный элемент для высших организмов, составная часть многих белков, концентрируется в волосах.
- 26. СЕРА Светло-желтое хрупкое твердое вещество, в чистом виде без запаха, tпл = 112,8 °C, tкип =
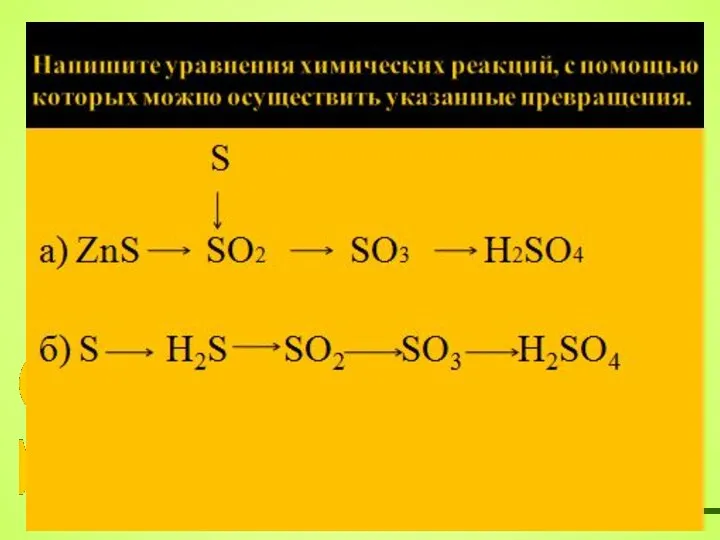
- 28. Задача: Каков объём (н.у.) а) сернистого газа получится при обжиге на воздухе 120г пирита FeS2; б)
- 30. Скачать презентацию















 Фуллерены (шары Бакминстера)
Фуллерены (шары Бакминстера) Алюминий и его органические производные
Алюминий и его органические производные Презентация на тему Кристаллические решетки 9 класс
Презентация на тему Кристаллические решетки 9 класс  Энергетический обмен
Энергетический обмен Ионная связь
Ионная связь Свойства солей, оксидов, оснований
Свойства солей, оксидов, оснований Генетические ряды Fe2+ и Fе3+. Качественные реакции на Fе2+ и Fе3+
Генетические ряды Fe2+ и Fе3+. Качественные реакции на Fе2+ и Fе3+ Презентация на тему Йод
Презентация на тему Йод  Роль Хеуорса, Фишера, Лемье в изучении структуры углеводов
Роль Хеуорса, Фишера, Лемье в изучении структуры углеводов Конструкционные и специальные материалы холодильной техники
Конструкционные и специальные материалы холодильной техники Перициклические реакции
Перициклические реакции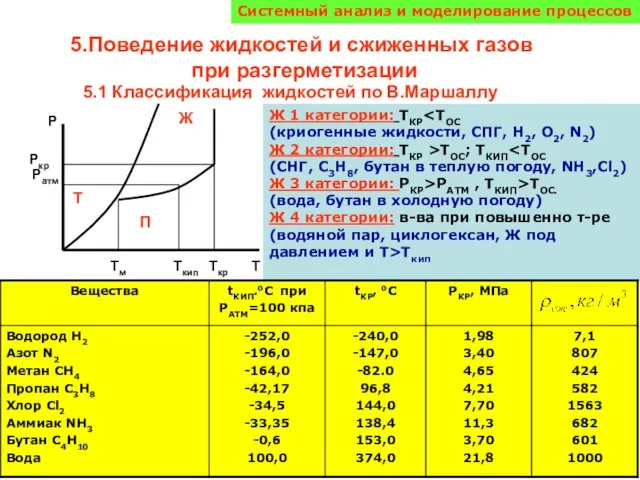 Поведение жидкостей и сжиженных газов при разгерметизации
Поведение жидкостей и сжиженных газов при разгерметизации Контроль качества лекарственных средств, производных карбоновых кислот и аминокислот
Контроль качества лекарственных средств, производных карбоновых кислот и аминокислот Получение армированных фотополимерных композиций
Получение армированных фотополимерных композиций Group 6 Cations
Group 6 Cations Русские ученые и топонимы в периодической системе химических элементов Д.И. Менделеева
Русские ученые и топонимы в периодической системе химических элементов Д.И. Менделеева Пищевые кислоты
Пищевые кислоты Предельные углеводороды. Алканы, насыщенные углеводороды, парафины, циклоалканы
Предельные углеводороды. Алканы, насыщенные углеводороды, парафины, циклоалканы Полиамиды (ПА)
Полиамиды (ПА) Окислители в пиросоставах
Окислители в пиросоставах Вебинар. Гидролиз солей
Вебинар. Гидролиз солей Совместимость материалов
Совместимость материалов Молярная масса вещества
Молярная масса вещества Композитные материалы
Композитные материалы Типы химической связи
Типы химической связи Презентация на тему Законы газового состояния вещества
Презентация на тему Законы газового состояния вещества  Development of the system of concepts on the topic redox reactions in the school course of inorganic chemistry
Development of the system of concepts on the topic redox reactions in the school course of inorganic chemistry Аммиак: состав, строение, свойства, применение
Аммиак: состав, строение, свойства, применение