Слайд 2Если число электронов на внешнем уровне атома максимальное, то такой уровень называется

завершённым. Такие атомы не вступают в химическое взаимодействие при обычных условиях. Это благородные газы, находящиеся в главной подгруппе 8 группы Периодической системы. Внешние электронные уровни атомов других хим. элементов являются незавершенными.
Электроны внешнего энергетического уровня являются валентными. При взаимодействии этих электронов образуется химическая связь
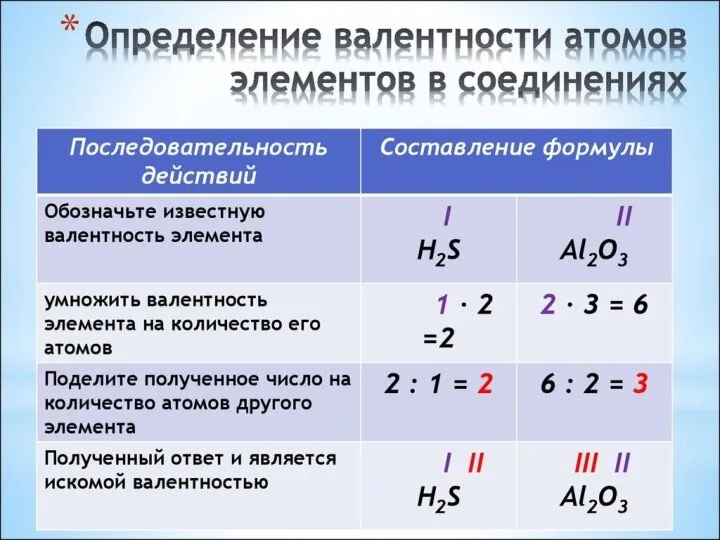
Слайд 3Валентность (от лат. «valentia» - сила) - способность атома присоединять или замещать определенное число других

атомов или атомных групп с образованием химической связи. Обозначается римскими цифрами.
У металлов главных групп Периодической системы валентность равна номеру группы.
У неметаллов высшая валентность элемента равна номеру его группы в Периодической системе Д.И. Менделеева. Низшая валентность находится как разница между числом 8 и номером группы, в которой расположен данный элемент.
!Валентность водорода всегда принимают за 1.
!Кислород всегда проявляет в своих соединениях валентность 2.
!Валентность алюминия всегда равна 3
Слайд 4Na2O
I
II
2
НОК
2/1 = 2 2/2 = 1 (не пишется)

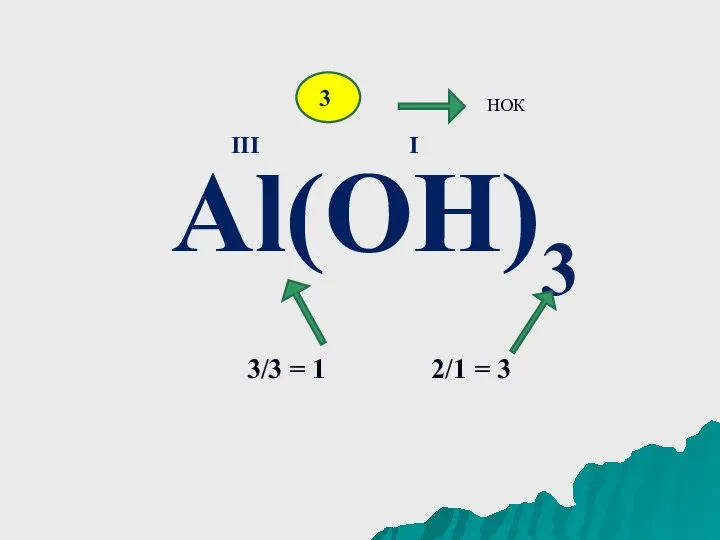
Слайд 5Al(OH)3
III
I
3
НОК
3/3 = 1 2/1 = 3
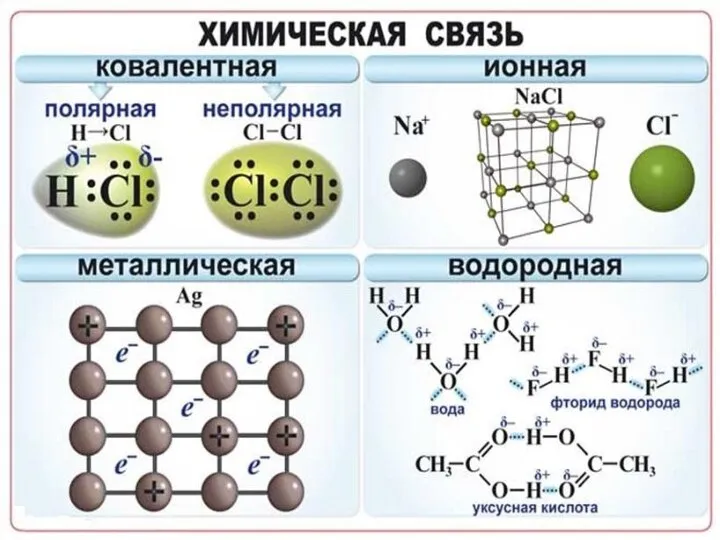
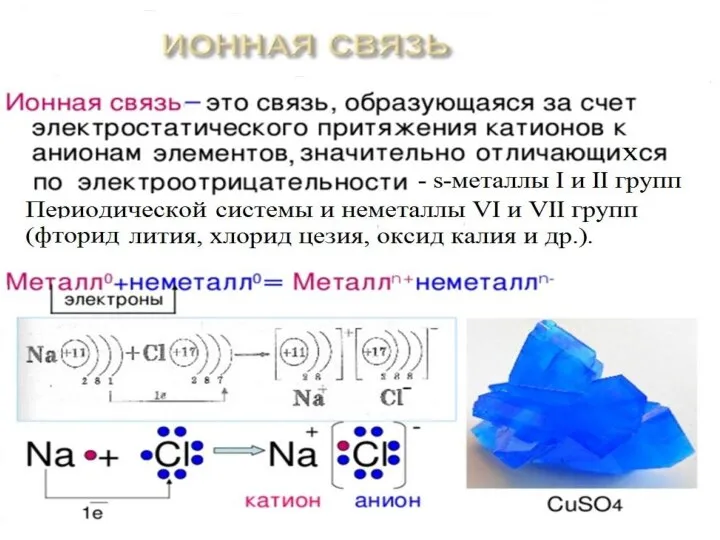
Слайд 7Химическая связь - взаимодействие атомов, связывающее их в единую устойчивую систему (молекулу,

ион, кристалл и др.)
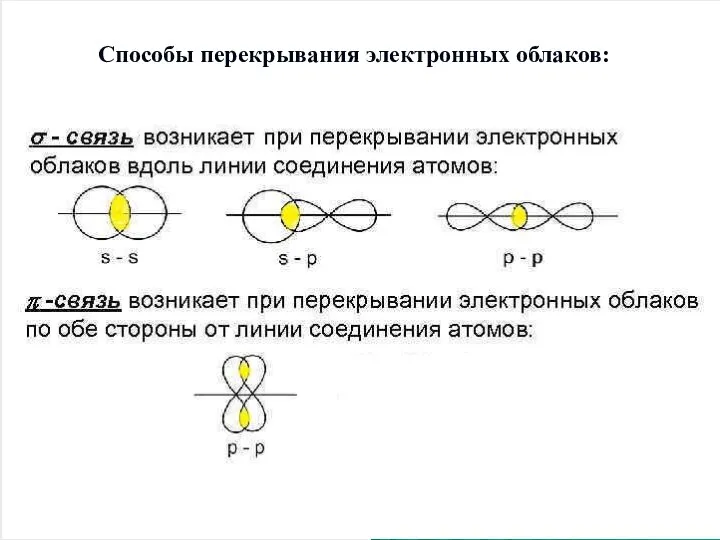
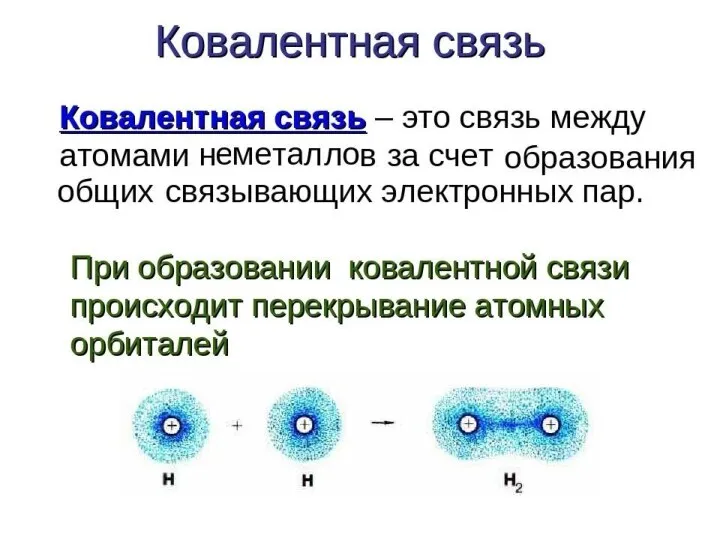
Слайд 10Способы перекрывания электронных облаков:
Слайд 11Характеристики ковалентной связи:
Энергия связи – энергия, которую необходимо затратить для разрыва данной

связи. Измеряется в кДж/моль. Зависит от радиуса перекрывающихся облаков.
Кратность связи – число химических связей между двумя атомами. Её можно показать сплошной линией между атомами либо точками. Чем больше кратность связи, тем прочнее связь.
Длина связи – расстояние между ядрами атомов в молекуле. Измеряется в нм.
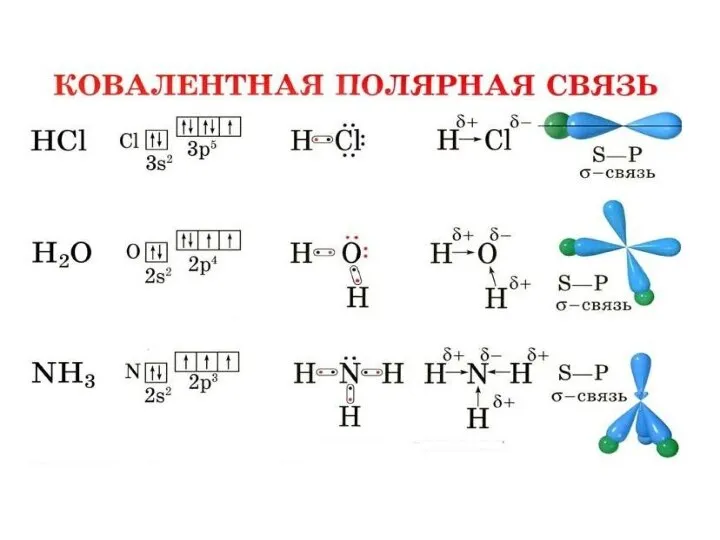
Полярность связи – смещение общей электронной плотности к более электроотрицательному атому. В зависимости от этого ковалентная связь делится на полярную и неполярную
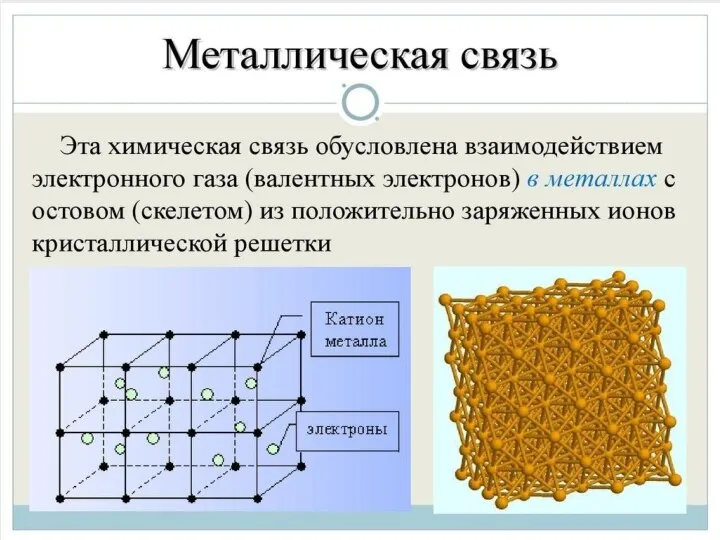
Слайд 16Металлическая связь - химическая связь в металлах и их сплавах. Данным видом
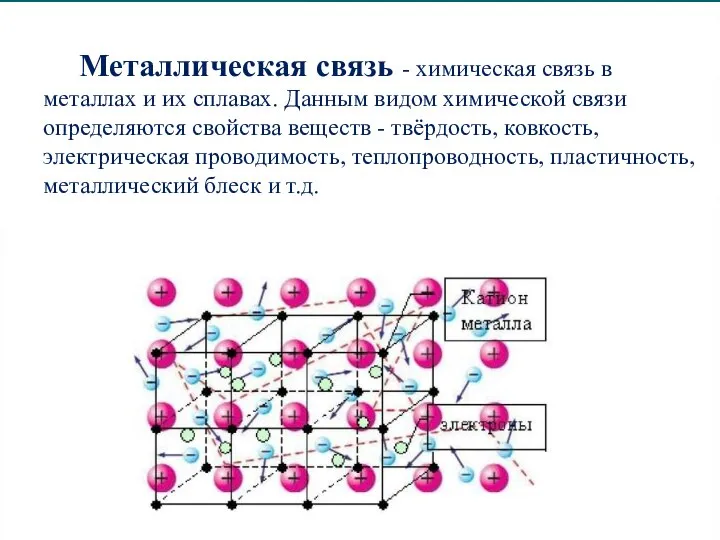
химической связи определяются свойства веществ - твёрдость, ковкость, электрическая проводимость, теплопроводность, пластичность, металлический блеск и т.д.
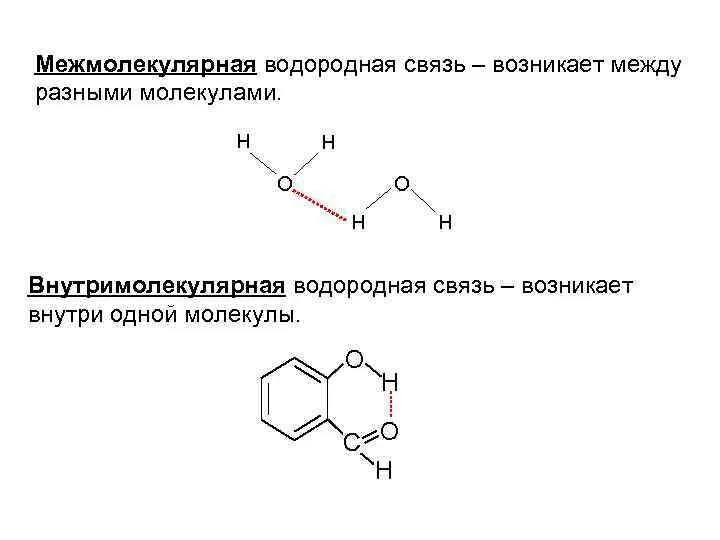
Слайд 20Наличие водородной связи обуславливает физические и химические свойства вещества - высокие температуры

плавления и кипения, хорошую растворимость, высокую испаряемость. Связь слабая и легко рвётся, но множество таких связей способно породить силу, на которой, в буквальном смысле, держится всё живое. Соединения с водородной связью - спирты, карбоновые кислоты, амины, аминокислоты, белки, вода, аммиак, фтороводород













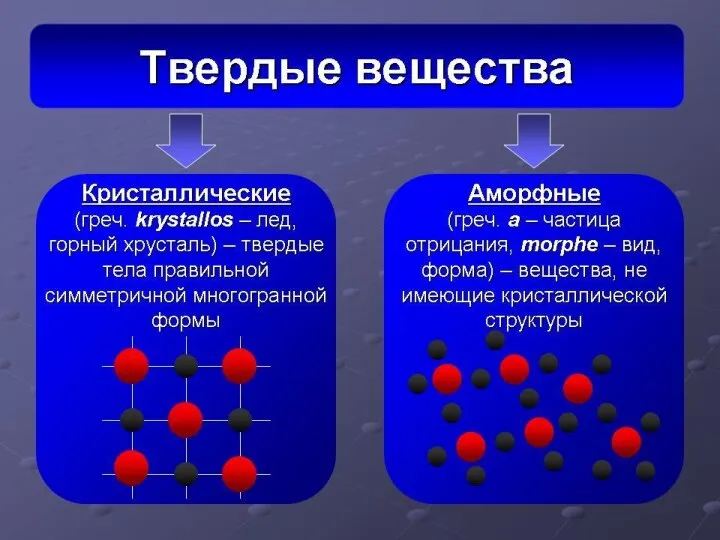

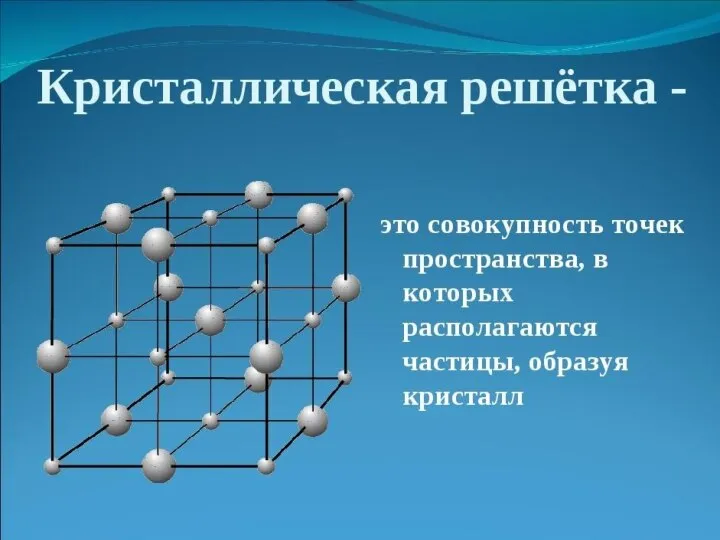
 Получение функциональных плёнок на основе TiO2
Получение функциональных плёнок на основе TiO2 Протолитические буферные системы. Буферные системы организма, их взаимодействие
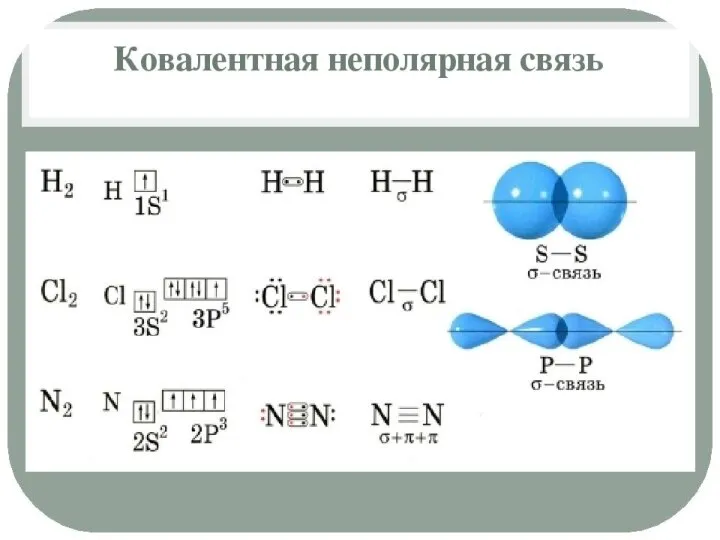
Протолитические буферные системы. Буферные системы организма, их взаимодействие Ковалентная неполярная связь
Ковалентная неполярная связь Потенциометрические анализаторы Поверка рН - метра
Потенциометрические анализаторы Поверка рН - метра Амины. Аминокислоты. Белки. (Лекция 8)
Амины. Аминокислоты. Белки. (Лекция 8) Химический тренажер
Химический тренажер Электролитическая диссоциация. 9 класс
Электролитическая диссоциация. 9 класс Степень окисления
Степень окисления Всё о нефти. Часть 5
Всё о нефти. Часть 5 Презентация на тему Минеральные удобрения
Презентация на тему Минеральные удобрения  Проведение лабраторных общеклинических исследований
Проведение лабраторных общеклинических исследований Ацилирование. Лекция 4
Ацилирование. Лекция 4 Закономерности процессов тепло- и газообмена на пожаре
Закономерности процессов тепло- и газообмена на пожаре Презентация на тему Органическая химия. История развития
Презентация на тему Органическая химия. История развития  Способы получения металлов
Способы получения металлов Открытый урок по химии в 8 классе по теме: «Первоначальные химические понятия». Учитель химии ГБОУ СОШ № 650 Безверхова Олеся Влад
Открытый урок по химии в 8 классе по теме: «Первоначальные химические понятия». Учитель химии ГБОУ СОШ № 650 Безверхова Олеся Влад Исследование физико-химических свойств щавелевой кислоты
Исследование физико-химических свойств щавелевой кислоты Природные источники углеводородов
Природные источники углеводородов Ковалентная химическая связь
Ковалентная химическая связь Минералы
Минералы Составление ионных уравнений
Составление ионных уравнений Теоретические основы органической химии. Лекция 25
Теоретические основы органической химии. Лекция 25 Щелочноземельные металлы
Щелочноземельные металлы Железо и его сплавы
Железо и его сплавы Неметаллы. Особенности электронного строения атомов НМ
Неметаллы. Особенности электронного строения атомов НМ Стехиометрические законы химии
Стехиометрические законы химии Метаболизм азота
Метаболизм азота Общая химия. Основные понятия
Общая химия. Основные понятия