Содержание
- 2. Фенолы и ароматические спирты Соединения, в которых гидроксильная группа непосредственно связана с ароматическим кольцом, называются фенолами
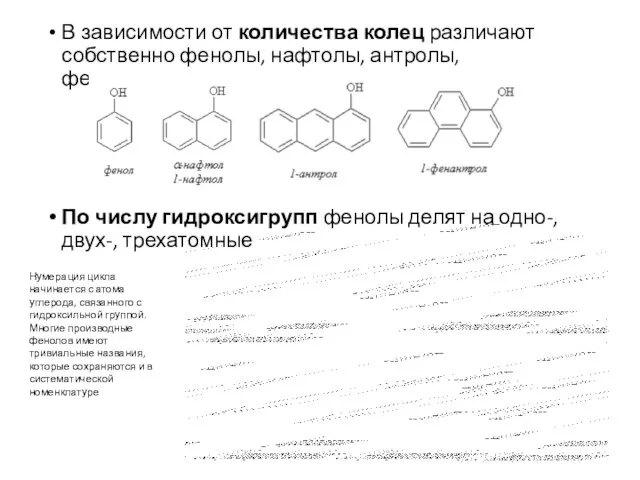
- 3. В зависимости от количества колец различают собственно фенолы, нафтолы, антролы, фенантролы По числу гидроксигрупп фенолы делят
- 4. Нахождение в природе В свободном состоянии фенолы редко встречаются в природных объектах. Фенол присутствует в листьях
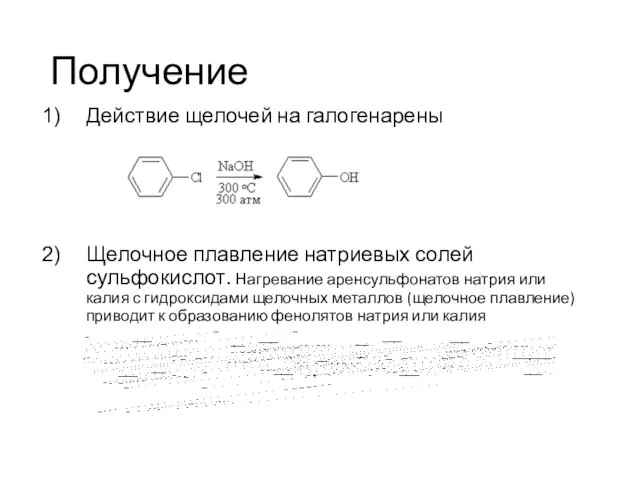
- 5. Получение Действие щелочей на галогенарены Щелочное плавление натриевых солей сульфокислот. Нагревание аренсульфонатов натрия или калия с
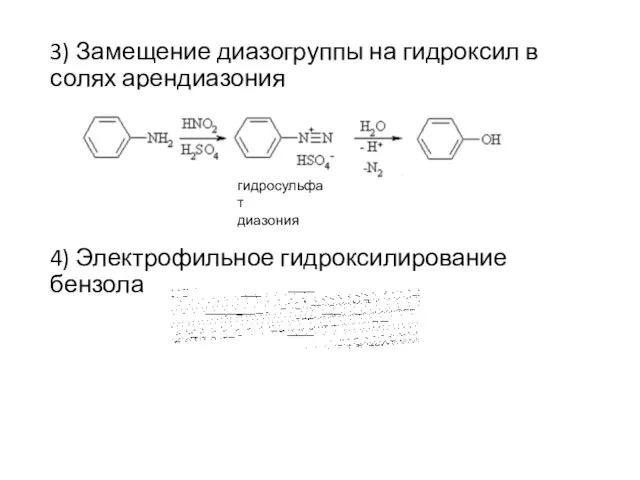
- 6. 3) Замещение диазогруппы на гидроксил в солях арендиазония 4) Электрофильное гидроксилирование бензола гидросульфат диазония
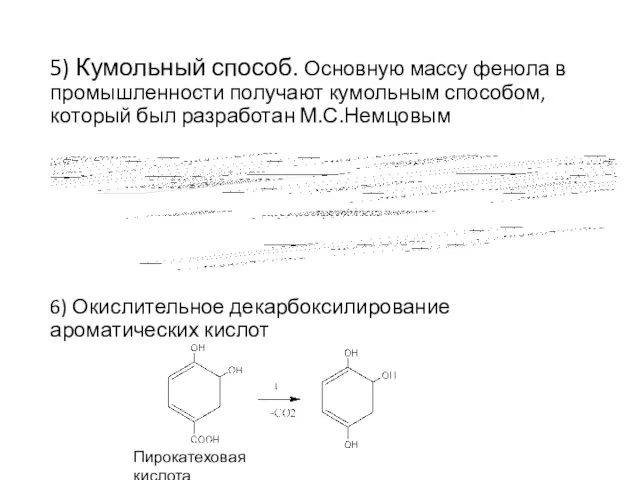
- 7. 5) Кумольный способ. Основную массу фенола в промышленности получают кумольным способом, который был разработан М.С.Немцовым 6)
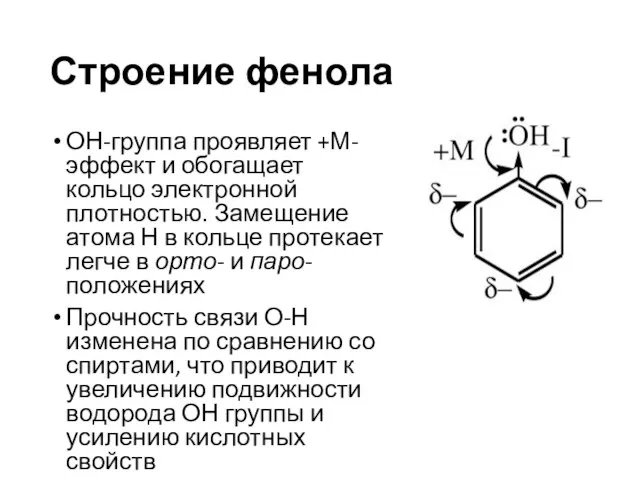
- 8. Строение фенола ОН-группа проявляет +М-эффект и обогащает кольцо электронной плотностью. Замещение атома Н в кольце протекает
- 9. Химические свойства 1) Кислотно-основные свойства Сам фенол значительно более сильная кислота, чем любой спирт и вода.
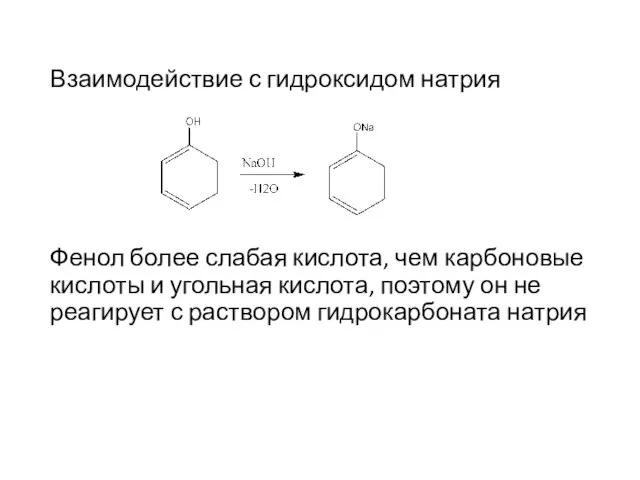
- 10. Взаимодействие с гидроксидом натрия Фенол более слабая кислота, чем карбоновые кислоты и угольная кислота, поэтому он
- 11. 2) Нуклеофильность фенолов и фенолят-ионов Фенольный гидроксил проявляет слабый нуклеофильный характер, тогда как анионы фенолов являются
- 12. Арилирование Ацилирование. В присутствии оснований фенолы подвергаются ацилированию ангидридами кислот и ацилгалогенидами Под действием AlCl3 эфиры
- 13. 3) Замещение гидроксила галогенами Протекает лишь в жестких условиях при действии галогенангидридов неорганических кислот 4) Замещение
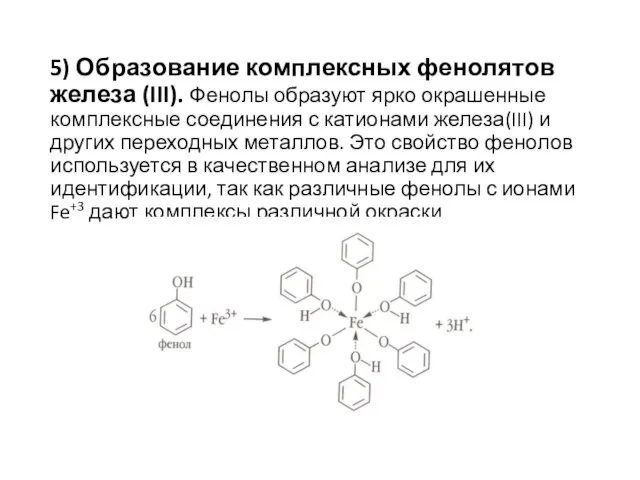
- 14. 5) Образование комплексных фенолятов железа (III). Фенолы образуют ярко окрашенные комплексные соединения с катионами железа(III) и
- 15. 6) Окисление. Фенол и многие замещенные фенолы при хранении постепенно окисляются кислородом воздуха, образуя сложную смесь
- 16. 7) Электрофильное замещение в ароматическом кольце. Гидроксильная группа ориентирует вступление электрофильного реагента в орто- и пара-положения
- 17. Сульфирование Алкилирование Ацилирование
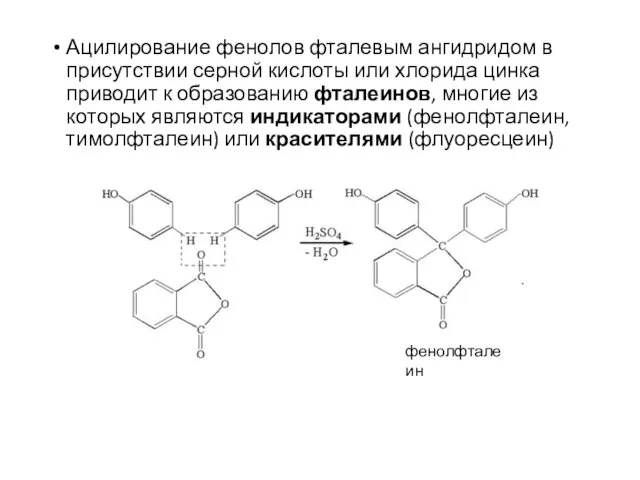
- 18. Ацилирование фенолов фталевым ангидридом в присутствии серной кислоты или хлорида цинка приводит к образованию фталеинов, многие
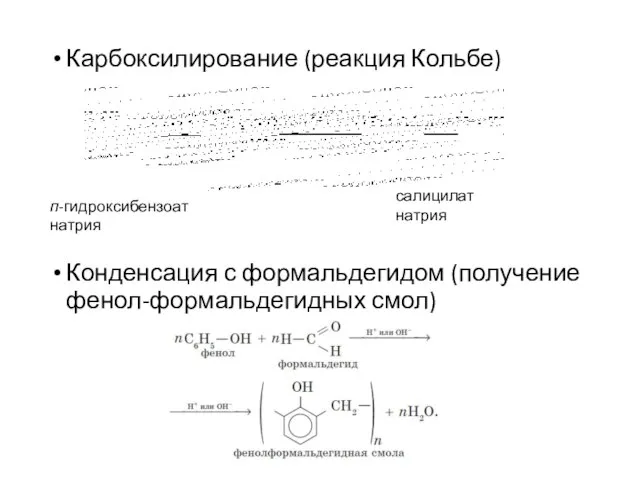
- 19. Карбоксилирование (реакция Кольбе) Конденсация с формальдегидом (получение фенол-формальдегидных смол) салицилат натрия п-гидроксибензоат натрия
- 20. Хиноны К хинонам относятся циклические сопряженные дикарбонильные соединения
- 21. Хиноны широко распространены в природе в качестве пигментов и биологически активных веществ, играющих важную роль в
- 22. Получение Реакции окисления
- 23. Химические свойства Образование молекулярных комплексов с электроноизбыточными соединениями Реакции присоединения. Характерны реакции 1,4-присоединения. Хиноны присоединяют галогенводородные
- 24. 3) Реакция с гидроксиламином. Образуются моно- или диоксимы 4) Реакция Дильса-Альдера. Хиноны в качестве диенофилов вступают
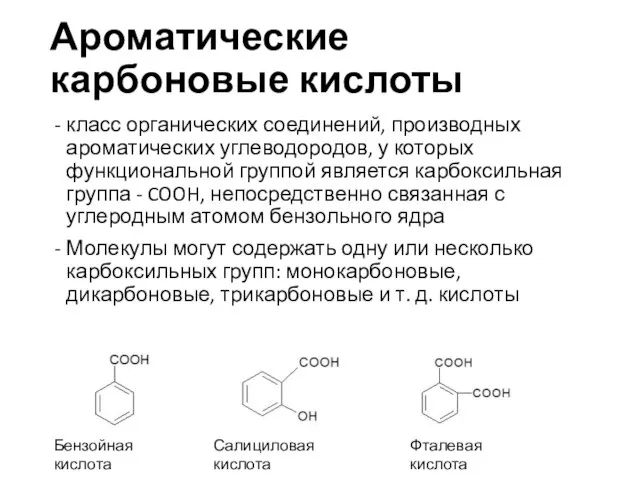
- 25. Ароматические карбоновые кислоты класс органических соединений, производных ароматических углеводородов, у которых функциональной группой является карбоксильная группа
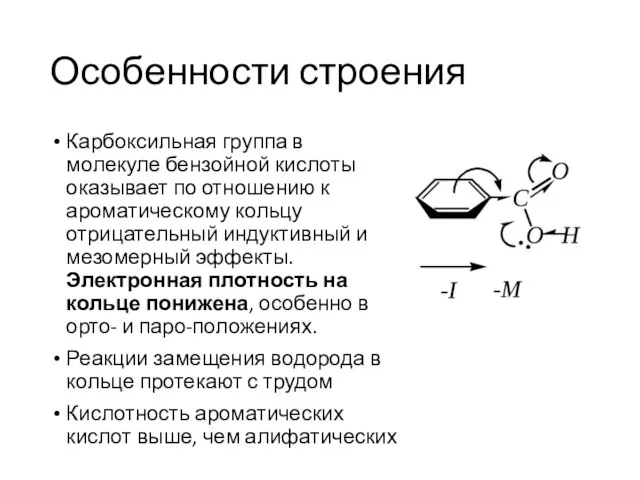
- 26. Особенности строения Карбоксильная группа в молекуле бензойной кислоты оказывает по отношению к ароматическому кольцу отрицательный индуктивный
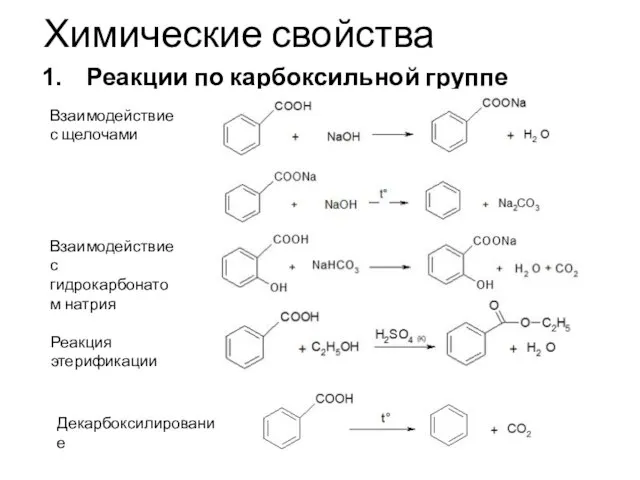
- 27. Химические свойства Реакции по карбоксильной группе Взаимодействие с щелочами Взаимодействие с гидрокарбонатом натрия Реакция этерификации Декарбоксилирование
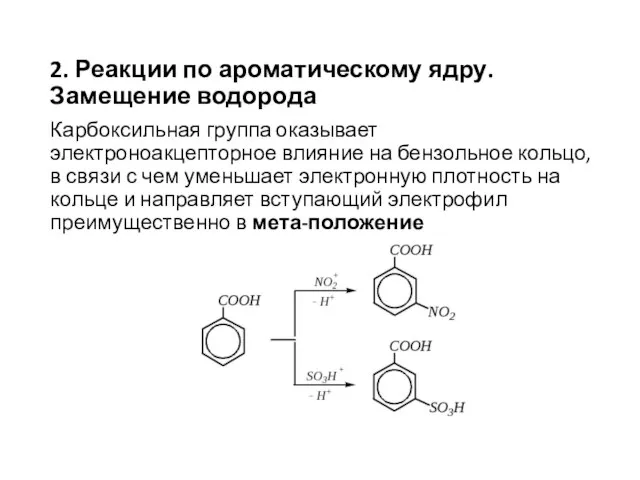
- 28. 2. Реакции по ароматическому ядру. Замещение водорода Карбоксильная группа оказывает электроноакцепторное влияние на бензольное кольцо, в
- 30. Скачать презентацию














 Соли, их классификация и свойства
Соли, их классификация и свойства Поликарбонат мономерлері
Поликарбонат мономерлері Презентация на тему Химические реакции 11 класс
Презентация на тему Химические реакции 11 класс  Скорость химических реакций
Скорость химических реакций Презентация на тему Получение галогенов. Биологическое значение и применение галогенов
Презентация на тему Получение галогенов. Биологическое значение и применение галогенов  Bool-doser team
Bool-doser team Экспериментальные методы изучения кинетики химических реакции
Экспериментальные методы изучения кинетики химических реакции Молярный объем
Молярный объем Правила работы и хранения щелочных металлов. Утилизация остатков щелочных металлов
Правила работы и хранения щелочных металлов. Утилизация остатков щелочных металлов Описание молекул
Описание молекул 9 класс Урок №8. Аминокислоты. Белки. Составитель презентации – учитель химии МОУ СОШ г. Холма Насонова Т.А.
9 класс Урок №8. Аминокислоты. Белки. Составитель презентации – учитель химии МОУ СОШ г. Холма Насонова Т.А. Л-1-5
Л-1-5 История создания периодической таблицы
История создания периодической таблицы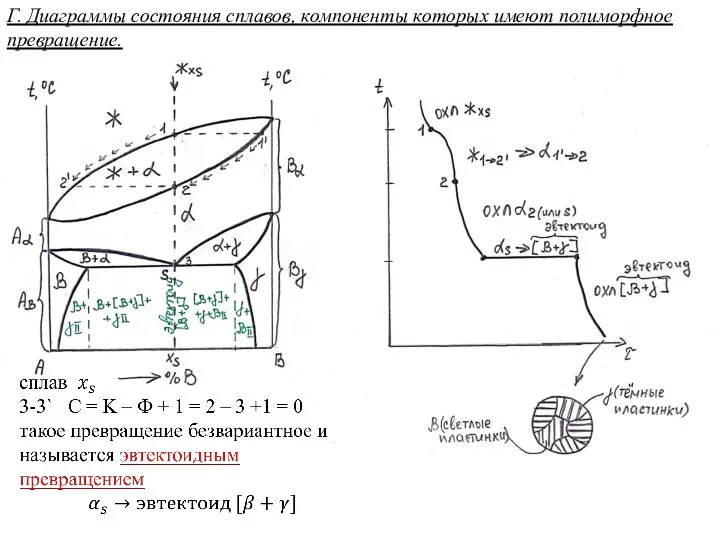 Диаграммы состояния сплавов, компоненты которых имеют полиморфное превращение
Диаграммы состояния сплавов, компоненты которых имеют полиморфное превращение Презентация на тему Биополимеры
Презентация на тему Биополимеры 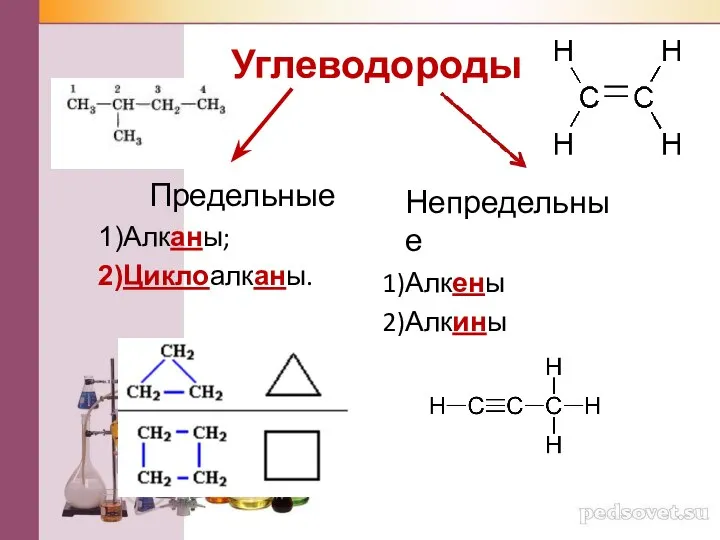 Углеводороды
Углеводороды Презентация на тему Самородки
Презентация на тему Самородки  Способы получения чистых веществ в лаборатории
Способы получения чистых веществ в лаборатории Биохимия статическая, динамическая, функциональная
Биохимия статическая, динамическая, функциональная Окислительно-восстановительные реакции
Окислительно-восстановительные реакции Обобщение и подготовка к химии 8 класс
Обобщение и подготовка к химии 8 класс Химия функциональных материалов. Адсорбция
Химия функциональных материалов. Адсорбция Презентация Продукции Opet (3)
Презентация Продукции Opet (3) Щелочные металлы
Щелочные металлы Метаболизм липидов
Метаболизм липидов Метан биогенный, абиогенный
Метан биогенный, абиогенный Дисперсные системы
Дисперсные системы Электролитическая диссоциация. Урок химии в 8 классе
Электролитическая диссоциация. Урок химии в 8 классе