Содержание
- 2. ЦЕЛЬ ИЗУЧЕНИЯ МАТЕРИАЛА Дать понятия: степени окисления элементов в простых и сложных веществах; о восстановителях и
- 3. СОДЕРЖАНИЕ Окислительно-восстановительные реакции (ОВР) Степень окисления. Правила расчета степени окисления Основные понятия Окислительно-восстановительные свойства соединений Составление
- 4. ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ РЕАКЦИИ (ОВР) Два типа химических реакций реакции обмена ─ реакции, протекающие без изменения степеней окисления
- 5. СТЕПЕНЬ ОКИСЛЕНИЯ Габдуллин А.Н., Никоненко Е.А. Окислительно-восстановительные реакции
- 6. ВЫСШАЯ И НИЗШАЯ СТЕПЕНИ ОКИСЛЕНИЯ МЕТАЛЛОВ Номер группы в периодической системе равен числу валентных электронов атома
- 7. ВЫСШАЯ И НИЗШАЯ СТЕПЕНИ ОКИСЛЕНИЯ НЕМЕТАЛЛОВ Высшая степень окисления неметаллов равна номеру группы (исключение составляют кислород
- 8. ПРАВИЛА РАСЧЕТА СТЕПЕНИ ОКИСЛЕНИЯ Габдуллин А.Н., Никоненко Е.А. Окислительно-восстановительные реакции
- 9. С.о. в сложных веществах: атомов элементов IA подгруппы +1 (Na+, K+); IIA подгруппы +2 (Be+2, Mg+2,
- 10. ПРИМЕРЫ РАСЧЕТА СТЕПЕНИ ОКИСЛЕНИЯ Расчет с. о. хлора в хлорате калия KClO4 Степень окисления кислорода −2
- 11. ОСНОВНЫЕ ПОНЯТИЯ Восстановитель (Red) − частица (атом, молекула, ион), которая отдает электроны. Окислитель (Ox) – частица
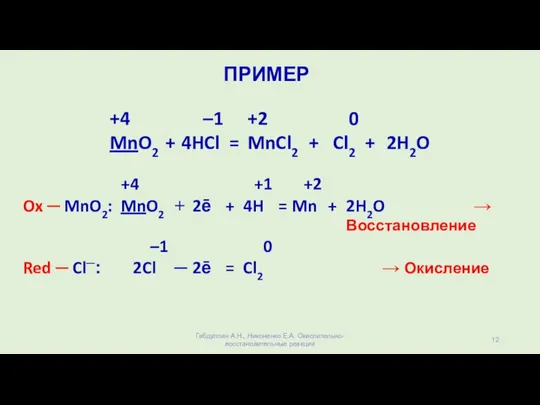
- 12. ПРИМЕР Габдуллин А.Н., Никоненко Е.А. Окислительно-восстановительные реакции
- 13. ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ СВОЙСТВА СОЕДИНЕНИЙ Габдуллин А.Н., Никоненко Е.А. Окислительно-восстановительные реакции
- 14. ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ СВОЙСТВА СОЕДИНЕНИЙ Только восстановителями являются: металлы: Na0, Ca0, Al0, Fe0… простые отрицательно заряженные ионы: Cl−,
- 15. ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ СВОЙСТВА СОЕДИНЕНИЙ Габдуллин А.Н., Никоненко Е.А. Окислительно-восстановительные реакции
- 16. СОСТАВЛЕНИЕ УРАВНЕНИЙ ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫХ РЕАКЦИЙ Для реакций, протекающих в растворах электролитов, используют метод электронно-ионного баланса: количество отданных
- 17. СОСТАВЛЕНИЕ УРАВНЕНИЙ ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫХ РЕАКЦИЙ Электронно-ионная схема: 2 Al0 ─ 3ē = Al3+ 3 2H+ + 2ē
- 18. ОВР В КИСЛОЙ СРЕДЕ Как правило, кислая среда создается добавлением разбавленной H2SO4: K2Cr2O7 + Na2SO3 +
- 19. ОВР В КИСЛОЙ СРЕДЕ Рассчитываем степени окисления атомов элементов, которые ее изменяют. Определяем окислитель (Ox) и
- 20. ОВР В КИСЛОЙ СРЕДЕ Записываем схемы переходов: Уравниваем число атомов элементов, изменяющих степень окисления и указываем
- 21. Cr2O72–+ 3SO32– + 14Н+ + 3Н2О → 2Cr3+ + 3SO42– + 6Н+ + 7Н2О Cr2O72–+ 3SO32–
- 22. ОВР В ЩЕЛОЧНОЙ СРЕДЕ Обычно среда создается добавлением гидроксида натрия или калия. В растворе присутствуют ионы
- 23. ПРИМЕР ОВР В ЩЕЛОЧНОЙ СРЕДЕ 2CrO2– + ClO3–+ 8ОН– + 3Н2О = 2CrO42– + Cl– +
- 24. ОВР В НЕЙТРАЛЬНОЙ СРЕДЕ В нейтральной среде недостающие атомы кислорода и водорода в левой части полуреакций
- 25. 3Mn2+ + 2MnO4─ + 10Н2О = 5MnO2 + 12Н+ + 8ОН– 8Н2О + 4H+ ПРИМЕР ОВР
- 26. ПРАВИЛА ИСПОЛЬЗОВАНИЯ СРЕДЫ Габдуллин А.Н., Никоненко Е.А. Окислительно-восстановительные реакции
- 27. ВЫВОДЫ Окислительно-восстановительные реакции − реакции, в которых изменяются степени окисления атомов элементов, входящих в состав реагирующих
- 28. ВЫВОДЫ Для вывода коэффициентов в уравнениях ОВР, протекающих в кислой, щелочной и нейтральной средах, используют метод
- 30. Скачать презентацию


























 Кислород Общая характеристика, получение и свойства
Кислород Общая характеристика, получение и свойства Комплексонометрическое титрование. Часть 2. Лекция 6
Комплексонометрическое титрование. Часть 2. Лекция 6 Классификация веществ. Урок №7
Классификация веществ. Урок №7 Химия. Решение задач
Химия. Решение задач Ионные уравнения реакций
Ионные уравнения реакций Перекрывающиеся гены
Перекрывающиеся гены Полиморфизм. Аморфные вещества
Полиморфизм. Аморфные вещества Молярный объем газов
Молярный объем газов Фосфор - светоносный
Фосфор - светоносный Lipidy
Lipidy Класс оксиды
Класс оксиды Жиры. Сложные эфиры
Жиры. Сложные эфиры Нефть: состав, свойства и переработка
Нефть: состав, свойства и переработка Алканы. Способы получения алканов. Химические свойства алканов
Алканы. Способы получения алканов. Химические свойства алканов Искусственные полимеры
Искусственные полимеры Радиоактивный распад. Чернобыль
Радиоактивный распад. Чернобыль Ионная полимеризация
Ионная полимеризация Презентация на тему Виды кристаллических решеток
Презентация на тему Виды кристаллических решеток  Кислородосодержащие органические вещества
Кислородосодержащие органические вещества Метаболизм триацилглицеринов
Метаболизм триацилглицеринов Фтор. Биологическое значение, соединения и применение
Фтор. Биологическое значение, соединения и применение Общая химия. Основные понятия
Общая химия. Основные понятия Различные варианты заданий ЕГЭ по теме Электролиз
Различные варианты заданий ЕГЭ по теме Электролиз Химические структуры
Химические структуры Разработка методов синтеза гомогенных катализаторов оксосинтеза бутиловых спиртов
Разработка методов синтеза гомогенных катализаторов оксосинтеза бутиловых спиртов Химия - неотъемлемая часть жизни
Химия - неотъемлемая часть жизни Периодический закон. Периодическая таблица химических элементов. 8 класс
Периодический закон. Периодическая таблица химических элементов. 8 класс Презентация на тему Аммиак
Презентация на тему Аммиак